Tamanho e Participação do Mercado de Teste Pré-Natal Não Invasivo
Análise do Mercado de Teste Pré-Natal Não Invasivo pela Mordor Intelligence
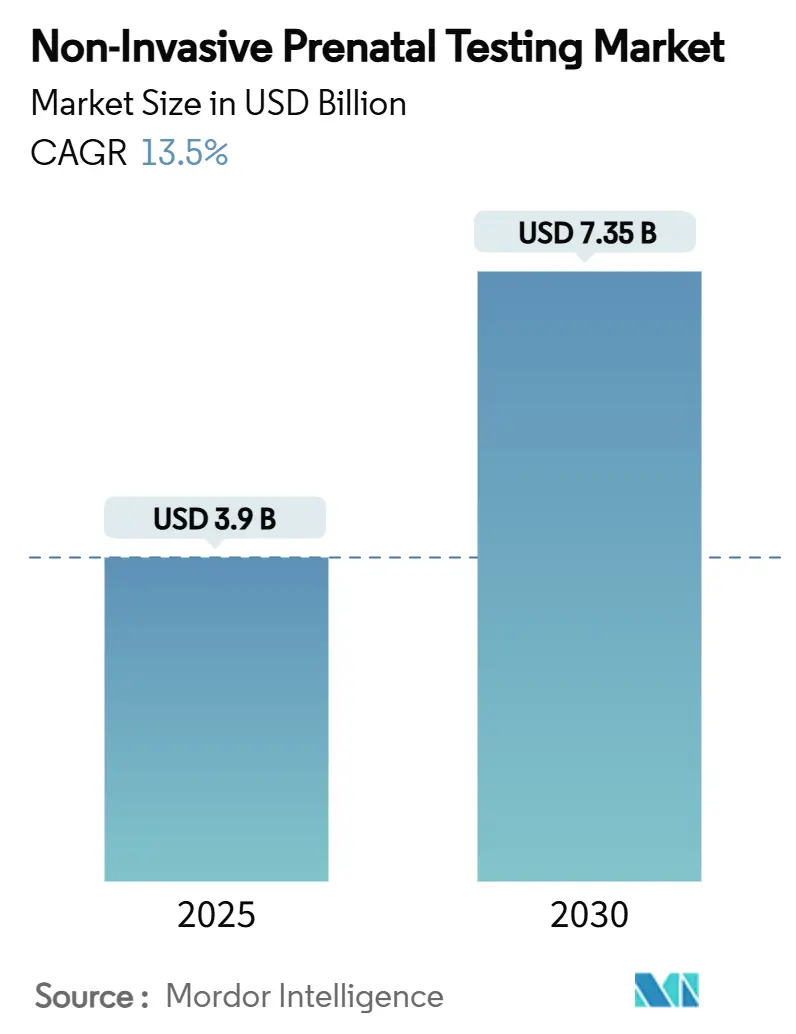
O tamanho do mercado de teste pré-natal não invasivo foi de USD 3,90 bilhões em 2025 e está previsto para alcançar USD 7,35 bilhões até 2030, resultando numa robusta TCAC de 13,50% durante o período. Diretrizes clínicas mais amplas agora recomendam triagem de DNA livre de células para toda gravidez, enquanto políticas de pagadoras estão facilitando obstáculos de autorização prévia, impulsionando expansão de volume através de categorias de risco. Custos de sequenciamento despencaram e fluxos de trabalho automatizados estão reduzindo tempos de resposta, tornando testes mais acessíveis para mercados emergentes. A regra final da FDA de 2024 sobre testes desenvolvidos em laboratório estabeleceu conformidade transicional que paradoxalmente acelerou a adoção porque grandes laboratórios comerciais agiram rapidamente para padronizar processos. Ao mesmo tempo, canais diretos ao consumidor estão se expandindo paralelamente às redes de encaminhamento médico, refletindo crescente disposição entre pais expectantes em pagar do próprio bolso por percepção genética precoce.
Principais Conclusões do Relatório
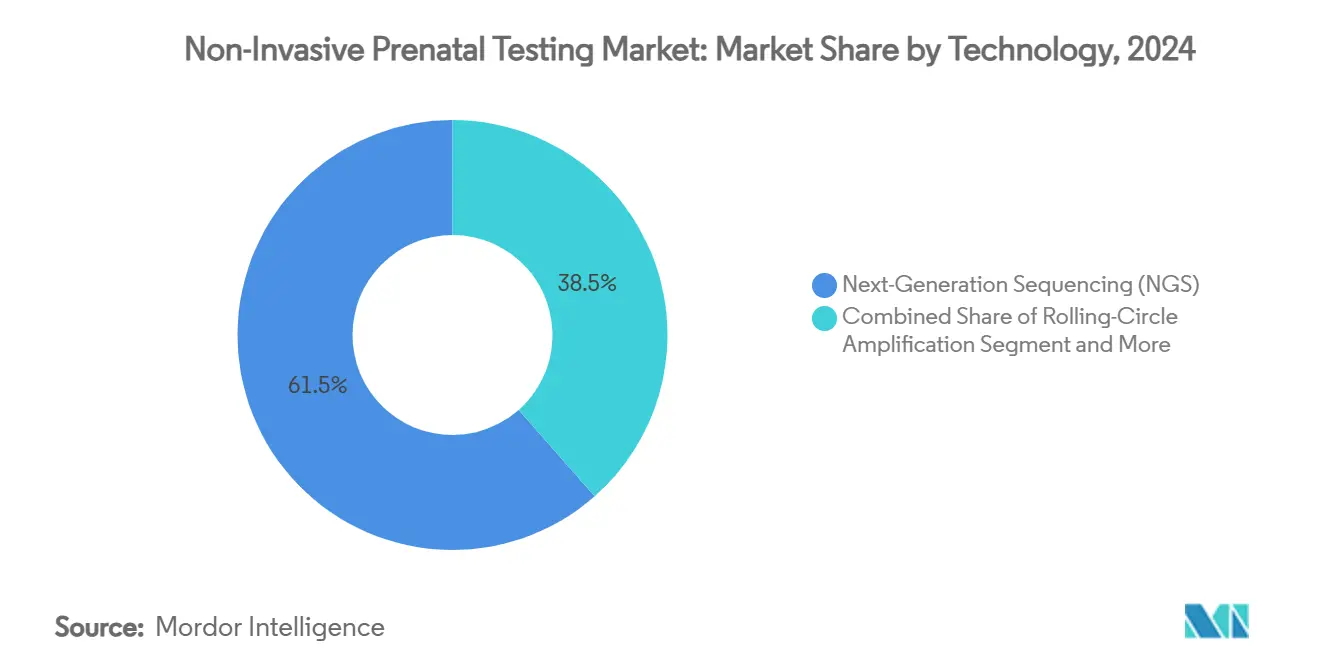
- Por tecnologia, sequenciamento de nova geração representou 61,51% da participação do mercado de teste pré-natal não invasivo em 2024, enquanto amplificação por círculo rolante está projetada para registrar 15,65% de TCAC até 2030.
- Por tipo de teste, triagem de cfDNA de genoma completo deteve 49,53% do tamanho do mercado de teste pré-natal não invasivo em 2024, enquanto painéis de microdeleção estão avançando a 14,85% de TCAC até 2030.
- Por geografia, América do Norte liderou com 45,25% da participação de receita em 2024; Ásia-Pacífico está prevista para registrar a maior TCAC de 16,45% durante 2025-2030.
- Por janela gestacional, o segmento de 10-12 semanas comandou 69,62% da participação do tamanho do mercado de teste pré-natal não invasivo em 2024, enquanto testes além de 24 semanas está na trilha para 16,85% de TCAC.
- Por usuário final, hospitais e centros de parto representaram 51,25% da participação do mercado de teste pré-natal não invasivo em 2024; institutos de pesquisa e clínicas de FIV representam o canal de crescimento mais rápido com 14,45% de TCAC.
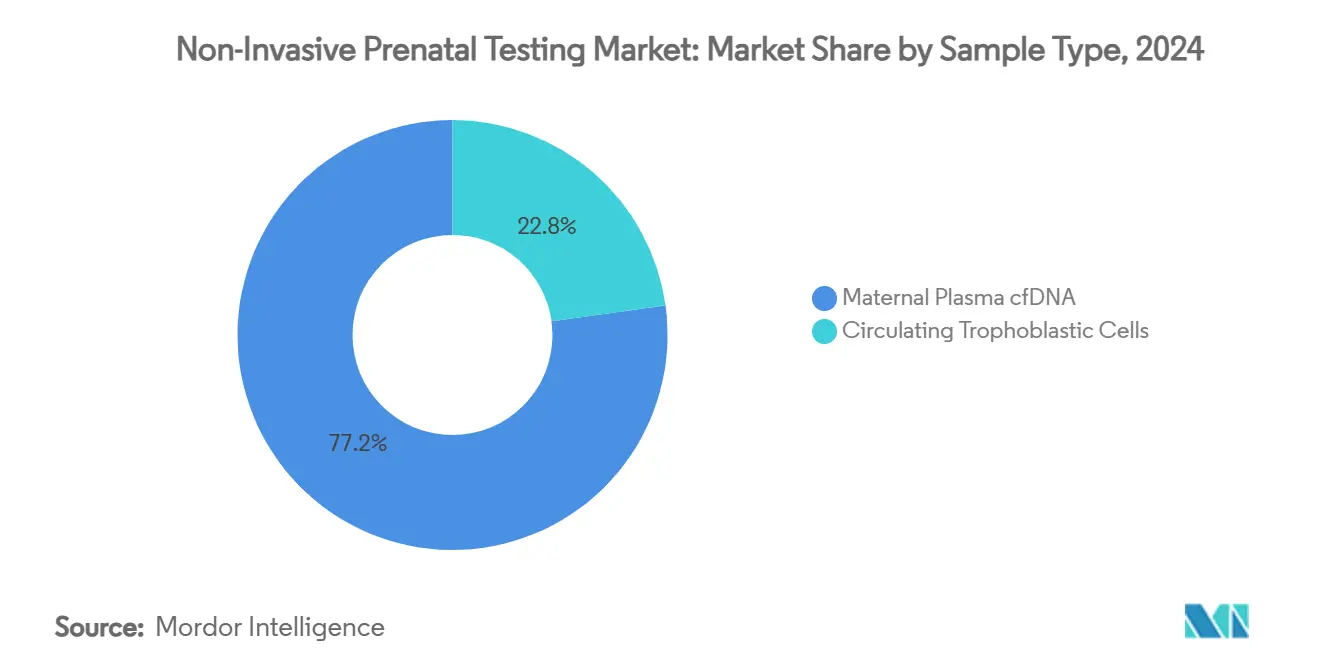
- Por tipo de amostra, cfDNA do plasma materno reteve 77,25% da participação do tamanho do mercado em 2024, porém células trofoblásticas circulantes estão acelerando a 14,55% de TCAC.
- Por componente, kits e reagentes capturaram 60,15% do tamanho do mercado em 2024; serviços está previsto para avançar a 14,35% de TCAC no mesmo horizonte.
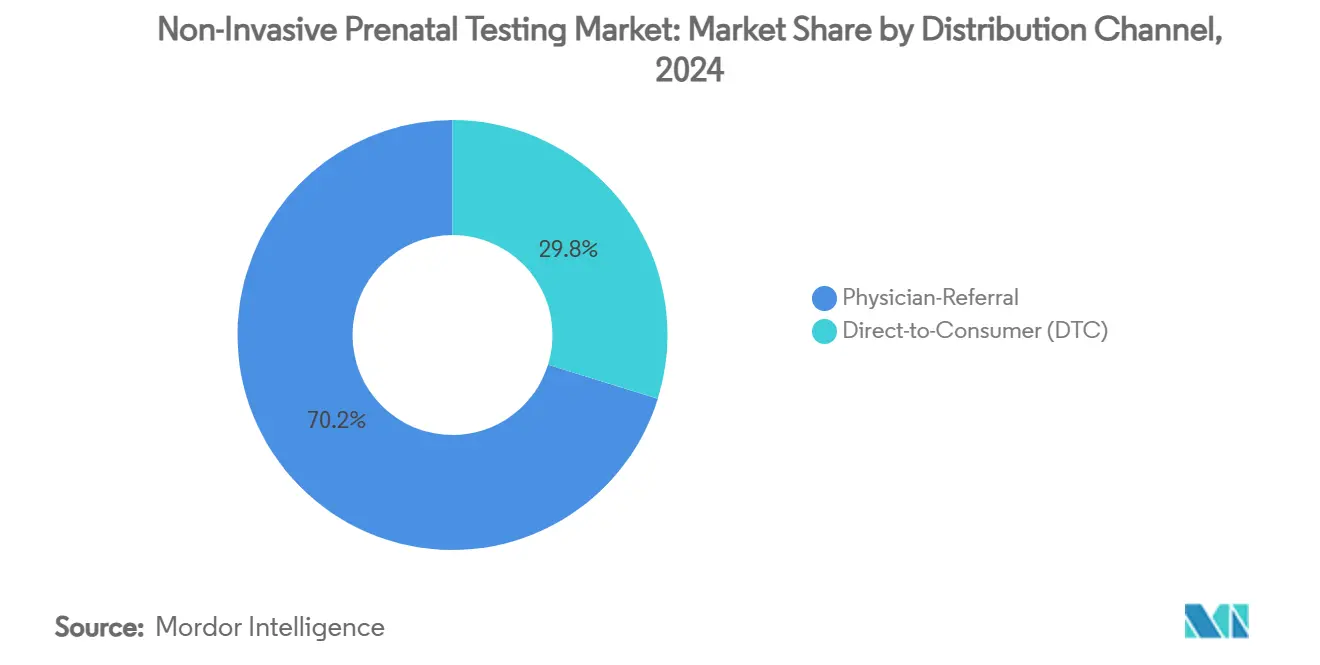
- Por canal de distribuição, vias de encaminhamento médico detiveram 70,25% da receita em 2024, enquanto vendas diretas ao consumidor estão traçando 18,55% de TCAC até 2030.
- Por aplicação, triagem da síndrome de Down representou 48,25% da participação em 2024, porém diagnósticos da síndrome de Turner estão subindo a 15,65% de TCAC no horizonte de previsão.
Tendências e Insights do Mercado Global de Teste Pré-Natal Não Invasivo
Análise do Impacto dos Impulsionadores
| Impulsionador | (~) % Impacto na Previsão de TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Aumento da idade materna global | +2.8% | Mercados desenvolvidos mundialmente | Longo prazo (≥ 4 anos) |
| Migração de triagem invasiva para cfDNA | +3.2% | América do Norte & Europa | Prazo médio (2-4 anos) |
| Menores custos de sequenciamento e automação | +2.5% | Global; mais rápido na Ásia-Pacífico | Curto prazo (≤ 2 anos) |
| Expansão de reembolso para risco médio | +2.1% | América do Norte & Europa; emergente em APAC | Prazo médio (2-4 anos) |
| Endossos de diretrizes do primeiro trimestre | +1.9% | Global | Prazo médio (2-4 anos) |
| Painéis de portador plus pré-natal combinados | +1.0% | Principalmente América do Norte & Europa | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Aumento da Idade Materna Global Aumentando Prevalência de Aneuploidia
Idade materna avançada impulsiona maior risco basal para anormalidades cromossômicas, causando volumes de triagem pré-natal a subir constantemente em economias desenvolvidas. Recomendações universais de diretrizes emitidas em 2024 removeram o limiar de risco baseado em idade e reposicionaram testes de cfDNA como triagem de primeira linha para toda gravidez[1]American College of Obstetricians and Gynecologists, "Screening for Fetal Chromosomal Abnormalities: ACOG Practice Bulletin Summary, Number 226," acog.org. Hospitais estão vendo menos procedimentos invasivos porque pais expectantes optam por um exame de sangue que não carrega risco de aborto espontâneo, abrindo um fluxo de receita previsível para laboratórios. Grandes estudos de coorte confirmam que sensibilidade do teste permanece consistente através de grupos etários mesmo que valor preditivo positivo se desloque para cima com a idade. Pagadoras acham a economia atrativa porque detecção precoce reduz custos de tratamento vitalício, e laboratórios aproveitam o volume confiável para negociar preços de reagentes em massa.
Mudança de Procedimentos Invasivos para Triagem de cfDNA por Segurança
Amniocentese e amostragem de vilo coriônico ambas carregam risco tangível de aborto espontâneo, causando ansiedade que torna alternativas não invasivas atrativas. Auditorias clínicas mostram que adoção de cfDNA corta volumes de procedimentos invasivos em até 80%, porém confirmação diagnóstica permanece disponível quando resultados indicam alta probabilidade de anormalidade. Obstetras notam menor exposição médico-legal, enquanto seguradoras veem menos reivindicações relacionadas a complicações ligadas a procedimentos. A abordagem baseada em sangue permite reteste rápido se amostras iniciais forem inadequadas, melhorando a experiência do paciente. Importante, vantagens de segurança ressoam em gravidezes de risco médio onde análises históricas de custo-benefício favoreciam nenhum teste.
Queda dos Custos de Sequenciamento e Automação Reduzindo Preços de Testes
Custos de sequenciamento do genoma caíram de USD 100 milhões em 2001 para USD 500 em 2023, e roteiros apontam para USD 10 por genoma dentro da década. Plataformas de alto rendimento, como NovaSeq X, cortam consumo de reagentes enquanto "laboratórios escuros" totalmente automatizados encolhem despesas de mão de obra. Químicas emergentes como amplificação por círculo rolante funcionam à temperatura ambiente, eliminando termocicladores caros. À medida que intensidade de capital cai, hospitais de nível médio na África, Sudeste Asiático e América Latina podem integrar testes sem construir mega-laboratórios, empurrando o mercado de teste pré-natal não invasivo mais profundamente em regiões mal atendidas.
Expansão de Reembolso para Gravidezes de Risco Médio
UnitedHealthcare removeu requisitos de autorização prévia em abril de 2025, citando forte evidência do mundo real de utilidade clínica em todas as categorias de gravidez. TRICARE seguiu o exemplo, criando precedente para cobertura universal do setor público. Agências estaduais do Medicaid estão emitindo novos códigos CPT, e leis de paridade de pagadoras privadas estão se espalhando através de jurisdições dos EUA. Seguradoras estatutárias europeias começaram a reembolsar casos de risco médio após análises de custo-efetividade mostrarem economias líquidas. Governos em mercados da Ásia-Pacífico, como Coreia do Sul, estão pilotando subsídios, sinalizando que cobertura universal está ganhando impulso mundialmente.
Análise do Impacto das Restrições
| Restrição | (~) % Impacto na Previsão de TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Questões éticas e regulamentares | -1.8% | Ásia-Pacífico e jurisdições globais selecionadas | Longo prazo (≥ 4 anos) |
| Infraestrutura laboratorial limitada | -2.2% | Ásia-Pacífico, MEA, América Latina | Prazo médio (2-4 anos) |
| Precisão em gravidezes gêmeas e FIV | -1.1% | Centros de fertilidade globais | Curto prazo (≤ 2 anos) |
| Utilidade incerta de painéis de microdeleção | -1.5% | América do Norte & Europa | Prazo médio (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Preocupações Éticas e Regulamentares sobre Achados Incidentais / Seleção de Sexo
A Lei PCPNDT da Índia criminaliza divulgação de sexo fetal, forçando provedores a redesenhar relatórios para conformidade local. Formuladores de políticas se preocupam que painéis em expansão possam revelar não-paternidade ou câncer materno, levantando complexidades de consentimento. O estudo Early IDENTIFY mostrou que metade dos casos não-reportáveis mascarava malignidades maternas, provocando debate sobre obrigações de dever-de-avisar[2]GenomeWeb, "Early IDENTIFY Trial Results Suggest Half of Women With Non-Reportable NIPT Result Have Cancer," genomeweb.com. Conselhos de bioética recomendam lançamentos incrementais de testes com aconselhamento aprimorado, porém restrições específicas por região retardam cronogramas comerciais. Vendedores devem, portanto, navegar uma colcha de retalhos de regras de divulgação que limitam economias de escala transfronteiriças.
Infraestrutura Laboratorial Limitada e Expertise em Bioinformática em Mercados Emergentes
Criar um laboratório molecular do zero envolve suítes condicionadas por energia, sequenciadores de alto custo e sistemas de qualidade ISO 13485, obstáculos que retardam adoção através de grande parte da África e partes do Sudeste Asiático. O primeiro serviço baseado em hospital da Tailândia levou múltiplos anos para alcançar acreditação completa mesmo com apoio externo de doadores. Bioinformatas qualificados são escassos, e retenção de talentos é desafiada por competição global. Governos estão começando a financiar centros regionais de genômica, mas até que lacunas de infraestrutura se fechem, envio de amostras importadas permanecerá necessário, limitando tempos de resposta e restringindo o mercado de teste pré-natal não invasivo em nações de menor renda.
Análise de Segmento
Por Tecnologia: Dominância do NGS Enfrenta Alternativas Emergentes
Em 2024, sequenciamento de nova geração comandou 61,51% da participação do mercado de teste pré-natal não invasivo, cimentando sua reputação por amplitude analítica e escalabilidade. Amplificação por círculo rolante, no entanto, está acelerando a 15,65% de TCAC, seu fluxo de trabalho de temperatura ambiente adequando ambientes com recursos limitados. O tamanho do mercado de teste pré-natal não invasivo para ensaios baseados em NGS está projetado para crescer constantemente à medida que laboratórios aproveitam plataformas legadas para lidar com complexidade crescente de testes. Enquanto isso, químicas mais simples desbloqueiam novos segmentos de clientes que carecem de orçamentos de capital para sequenciadores de alta gama.
PCR digital e ensaios habilitados por CRISPR estão entrando em programas piloto, visando quantificação mais rigorosa de fração fetal e especificidade aprimorada. Enrijecimento regulamentário pode inicialmente beneficiar fornecedores entrincheirados de NGS cujos sistemas já atendem padrões de qualidade, porém preços disruptivos de RCA ou metodologias isotérmicas poderiam girar decisões de compra à medida que volumes de mercados emergentes escalam.
Nota: Participações de segmento de todos os segmentos individuais disponíveis mediante compra do relatório
Por Tipo de Teste: Triagem de Genoma Completo Lidera Expansão
Testes de cfDNA de genoma completo detiveram 49,53% do tamanho do mercado de teste pré-natal não invasivo em 2024, favorecidos por sua cobertura cromossômica abrangente. Painéis de microdeleção estão registrando vigorosa TCAC de 14,85%, beneficiando-se de evidência contínua de que detecção mais ampla de variantes adiciona valor clínico em casos selecionados. Ensaios apenas de aneuploidia permanecem populares onde pagadoras reembolsam um menu limitado, mas sua participação relativa está diminuindo à medida que diretrizes evoluem.
Triagens monogênicas e de status de portador combinadas poderiam redesenhar limites de mercado fundindo planejamento reprodutivo com vigilância pré-natal. Porém reembolso permanece o fator limitante; sem endosso de pagadora, economia de pagamento próprio limitará adoção de curto prazo apesar da crescente curiosidade do consumidor.
Por Janela Gestacional: Teste Precoce Domina
A janela de 10-12 semanas reivindicou 69,62% da participação em 2024 à medida que triagem do primeiro trimestre se tornou protocolo obstétrico padrão. Laboratórios frequentemente pré-agendam coletas durante visitas rotineiras de ultrassom, garantindo eficiência logística e alta adesão do paciente. Testes realizados após 24 semanas, embora uma base pequena, estão crescendo 16,85% anualmente graças a necessidades de manejo de gravidez tardia como anomalias inexplicadas em exames do terceiro trimestre.
Clínicos preferem resultados precoces para latitude de tomada de decisão, mas aplicações de estágio tardio oferecem garantia em gravidezes complexas onde triagem anterior foi perdida ou inconclusiva. Fornecedores estão refinando ensaios para permanecer sensíveis apesar da fração fetal em declínio à medida que gestação avança, assim ampliando volume endereçável.
Por Tipo de Amostra: Plasma Materno Domina
Plasma materno representou 77,25% das amostras em 2024, sustentado por kits de extração validados e automação escalável. Captura de células trofoblásticas circulantes, embora promissora, ainda fica para trás devido a menor rendimento e complexidade técnica. Protocolos de enriquecimento que isolam magneticamente fragmentos de DNA fetal aumentam sensibilidade para variantes de número de cópias, o que fortalece incumbência do plasma.
Bibliotecas de nova geração agora requerem menos etapas manuais, e fluxos de trabalho certificados ISO reduzem variabilidade lote-a-lote. À medida que autoridades regulamentares apertam teste de proficiência, métodos estabelecidos baseados em plasma provavelmente reterão dominância clínica sobre matrizes experimentais no prazo médio.
Por Componente: Kits e Reagentes Lideram Receita
Kits e reagentes geraram 60,15% da receita de 2024, tornando consumíveis o motor econômico para laboratórios. Contratos de serviço e leasing de instrumentos estão subindo a 14,35% de TCAC à medida que clientes buscam custos previsíveis sobre grandes desembolsos de capital. Plataformas integradas que agrupam consumíveis, analíticos e manutenção reduzem complexidade de aquisição, um ponto de venda para administradores hospitalares.
Materiais de referência e controles de qualidade de terceiros estão ganhando tração após novas regras de acreditação obrigarem proficiência externa. Fornecedores que oferecem soluções de pilha completa-kits, software e suporte-tendem a prender clientes por ciclos multianuais, sustentando fluxos de receita recorrentes.
Por Usuário Final: Hospitais Mantêm Liderança
Hospitais e centros de parto capturaram 51,25% da participação do mercado de teste pré-natal não invasivo em 2024 à medida que obstetras encaminharam a maioria dos testes através de laboratórios internos ou parceiros. Institutos de pesquisa e clínicas de FIV estão expandindo 14,45% anualmente, integrando triagem genética em vias de reprodução assistida. Laboratórios diagnósticos independentes servem como absorvedores de choque de capacidade, lidando com excesso quando laboratórios hospitalares alcançam limites de rendimento.
Parcerias comerciais entre grupos de FIV e grandes laboratórios de referência estão proliferando, misturando dados de endocrinologia reprodutiva com analíticos pré-natais. A estrutura de colaboração acelera inovação em teste genético pré-implantação e reforça efeitos de rede do ecossistema de teste.
Por Canal de Distribuição: Encaminhamento Médico Domina
Rotas de encaminhamento médico trouxeram 70,25% da receita de 2024, refletindo integração profunda da triagem de cfDNA no cuidado pré-natal rotineiro. Plataformas diretas ao consumidor, no entanto, mostram 18,55% de TCAC, impulsionadas por marketing digital e aconselhamento tele-genético. Modelos híbridos estão emergindo onde consumidores fazem pedidos online mas amostras são coletadas em clínicas parceiras, misturando conveniência com supervisão médica.
Reguladores examinam players DTC para garantir que interpretação de resultados atenda padrões clínicos. À medida que supervisão se aperta, alianças entre marcas DTC e laboratórios de referência acreditados são esperadas para se multiplicar, desfocando limites de canal tradicionais.
Por Aplicação: Triagem da Síndrome de Down Lidera
Triagem da síndrome de Down deteve 48,25% da participação em 2024 e permanece o ponto de entrada para a maioria das práticas obstétricas. Ensaios da síndrome de Turner, beneficiando-se de analíticos aprimorados de cromossomos sexuais, estão escalando a 15,65% de TCAC, sinalizando apetite por percepção mais ampla do cariótipo fetal. Painéis das síndromes de Edwards e Patau permanecem parte de ofertas agrupadas de trissomia, contribuindo receita constante embora de crescimento mais lento.
Crescimento futuro depende do reconhecimento de seguros de painéis multi-condição como padrão de cuidado, o que elevaria adoção de testes agrupados enquanto comprime procedimentos independentes.
Análise Geográfica
América do Norte reteve 45,25% da participação de receita em 2024 graças ao alinhamento de pagadoras, redes de laboratório estabelecidas e forte apoio de sociedades profissionais. A remoção em abril de 2025 da autorização prévia por uma seguradora nacional líder sublinha ímpeto em direção ao acesso sem atrito. O financiamento província-por-província do Canadá continua a causar disparidade de adoção, porém volume nacional cresce à medida que pagamento privado preenche lacunas do setor público. Hospitais privados do México estão integrando capacidade local de sequenciamento, embora reembolso permaneça limitado a segmentos de pagamento próprio.
Europa reflete um mosaico de modelos de política que equilibram ética com objetivos universais de saúde. O Serviço Nacional de Saúde do Reino Unido implanta cfDNA como triagem contingente de segundo nível, enquanto Alemanha e França reembolsam testes de primeira linha para indicações definidas. Itália e Espanha estão expandindo pilotos de nível regional para cobertura completa. Ênfase continental em aconselhamento genético e consentimento cria infraestrutura de apoio robusta, embora a maior custo administrativo por teste.
Ásia-Pacífico é o corredor de crescimento com 16,45% de TCAC. Clusters de genômica apoiados pelo governo da China e grande coorte de nascimento sustentam economias de escala que reduzem preços por teste[3]Illumina, "Illumina Has Become a Powerhouse of the Chinese Genomics Industry," illumina.com. Projeto de demonstração multi-centro do Japão validou desempenho clínico, catalisando adoção de seguradora privada. Paisagem de dupla regulação da Índia-centros de laboratório modernos em metrópoles versus limitações PCPNDT na divulgação de sexo-cria adoção regional desigual. Austrália opera em modelo de pagamento próprio com média de AUD 500-800 (USD 330-530), embora revisões de política estejam em andamento para integrar testes no Medicare Benefits Schedule.
Panorama Competitivo
Concentração de mercado é moderada, com players estabelecidos aproveitando pipelines proprietários de bioinformática e contratos de reembolso. Aquisição de USD 52,5 milhões da Natera dos ativos de saúde reprodutiva da Invitae consolidou IP de ensaio e contas hospitalares. Illumina e Tempus forjaram parceria AI-genômica para acelerar interpretação de variantes em escala. Roche está co-desenvolvendo sequenciamento SBX com Broad Clinical Labs, visando cortar tempos de execução para ensaios de genoma completo.
Vetores competitivos se inclinam para precisão analítica e amplitude de menu ao invés de preço sozinho porque regras de pagadora dependem de utilidade clínica. Regulação FDA de testes desenvolvidos em laboratório imporá custos de conformidade que pequenos laboratórios regionais podem lutar para atender, potencialmente provocando maior consolidação. Em mercados emergentes, startups locais competem em resposta rápida e aconselhamento culturalmente adequado, embora escalar além de limites provinciais permaneça desafiador.
Entrantes diretos ao consumidor exploram canais de mídia social para ganhar reconhecimento de marca, porém muitos dependem de laboratórios certificados CLIA estabelecidos para processamento de laboratório úmido. À medida que supervisão se aperta, alianças estratégicas são esperadas para se aprofundar entre marcas DTC e incumbentes, criando modelos híbridos que expandem alcance do consumidor enquanto salvaguardam rigor analítico.
Líderes da Indústria de Teste Pré-Natal Não Invasivo
-
Centogene NV
-
F. Hoffmann-La Roche Ltd.
-
Eurofins Scientific SE
-
Revvity, Inc.
-
BGI Genomics Co. Ltd
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes da Indústria
- Maio de 2025: Roche anunciou colaboração com Broad Clinical Labs para acelerar adoção de tecnologia de sequenciamento SBX para recém-nascidos criticamente doentes, focando na integração de sequenciamento de genoma completo na prática clínica rotineira.
- Abril de 2025: UnitedHealthcare eliminou requisitos de autorização prévia para teste pré-natal não invasivo através de múltiplos planos, incluindo planos comerciais e comunitários. Esta mudança de política afeta procedimentos de teste de DNA fetal livre de células e visa simplificar acesso à saúde para membros e provedores.
Escopo do Relatório do Mercado Global de Teste Pré-Natal Não Invasivo
Conforme o escopo do relatório, teste pré-natal não invasivo (NIPT), que também é chamado triagem pré-natal não invasiva (NIPS), é um método para determinar o risco de que o feto nascerá com certas anormalidades genéticas. É baseado em análise de DNA livre de células (cfDNA) no sangue materno. Este teste analisa pequenos fragmentos de DNA circulando no sangue de uma mulher grávida. NIPT analisa a informação genética contida neste DNA para triagem de uma série de anormalidades.
O mercado de teste pré-natal não invasivo é segmentado em componentes, aplicações, usuários finais e geografia. Por componente, o mercado é segmentado em instrumentos, kits e reagentes, e serviços. Por aplicação, o mercado é segmentado em síndrome de Down (trissomia 21), síndrome de Edwards (trissomia 18), síndrome de Patau (trissomia 13), síndrome de Turner, e outras aplicações. Por usuário final, o mercado é segmentado em hospitais e laboratórios diagnósticos. Por geografia, o mercado é segmentado em América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África, e América do Sul. O relatório oferece o valor (em USD Bilhão) para os segmentos acima.
| Sequenciamento de Nova Geração (NGS) |
| Amplificação por Círculo Rolante |
| Microarray |
| PCR em Tempo Real |
| Outras Tecnologias |
| Triagem de Aneuploidia |
| Triagem de Microdeleção / Microduplicação |
| Triagem de cfDNA de Genoma Completo |
| Genotipagem Rh-D |
| Teste de Doença Monogênica |
| 10-12 Semanas |
| 13-24 Semanas |
| Maior que 24 Semanas |
| cfDNA do Plasma Materno |
| Células Trofoblásticas Circulantes |
| Instrumentos |
| Kits e Reagentes |
| Serviços |
| Hospitais e Centros de Parto |
| Laboratórios Diagnósticos |
| Clínicas de FIV e Fertilidade |
| Institutos de Pesquisa |
| Encaminhamento Médico |
| Direto ao Consumidor (DTC) |
| Síndrome de Down (Trissomia 21) |
| Síndrome de Edwards (Trissomia 18) |
| Síndrome de Patau (Trissomia 13) |
| Síndrome de Turner |
| Outras Anormalidades Cromossômicas |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Resto da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Resto do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Tecnologia | Sequenciamento de Nova Geração (NGS) | |
| Amplificação por Círculo Rolante | ||
| Microarray | ||
| PCR em Tempo Real | ||
| Outras Tecnologias | ||
| Por Tipo de Teste | Triagem de Aneuploidia | |
| Triagem de Microdeleção / Microduplicação | ||
| Triagem de cfDNA de Genoma Completo | ||
| Genotipagem Rh-D | ||
| Teste de Doença Monogênica | ||
| Por Janela Gestacional | 10-12 Semanas | |
| 13-24 Semanas | ||
| Maior que 24 Semanas | ||
| Por Tipo de Amostra | cfDNA do Plasma Materno | |
| Células Trofoblásticas Circulantes | ||
| Por Componente | Instrumentos | |
| Kits e Reagentes | ||
| Serviços | ||
| Por Usuário Final | Hospitais e Centros de Parto | |
| Laboratórios Diagnósticos | ||
| Clínicas de FIV e Fertilidade | ||
| Institutos de Pesquisa | ||
| Por Canal de Distribuição | Encaminhamento Médico | |
| Direto ao Consumidor (DTC) | ||
| Por Aplicação | Síndrome de Down (Trissomia 21) | |
| Síndrome de Edwards (Trissomia 18) | ||
| Síndrome de Patau (Trissomia 13) | ||
| Síndrome de Turner | ||
| Outras Anormalidades Cromossômicas | ||
| Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Resto do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Questões-Chave Respondidas no Relatório
Quão grande é a demanda global por triagem pré-natal de DNA livre de células hoje?
O tamanho do mercado de teste pré-natal não invasivo foi USD 3,90 bilhões em 2025 e está projetado para alcançar USD 7,35 bilhões até 2030, refletindo 13,50% de TCAC.
Por que custos de sequenciamento são tão fundamentais para preços futuros?
Inovações em reagentes e instrumentos já cortaram custos de genoma completo para cerca de USD 500, e roteiros em direção a USD 10 por genoma permitirão laboratórios precificarem testes mais competitivamente, desbloqueando demanda em regiões de menor renda.
Qual região mostra a perspectiva de crescimento mais rápida?
Ásia-Pacífico lidera com previsão de 16,45% de TCAC até 2030 à medida que China, Japão, Índia e Austrália expandem reembolso e capacidade laboratorial local.
Qual janela clínica captura mais volume de teste?
Aproximadamente 69,62% dos testes são coletados entre 10 e 12 semanas de gestação porque triagem do primeiro trimestre agora aparece em diretrizes obstétricas padrão.
Como NIPT direto ao consumidor difere de testes ordenados por médico?
Plataformas DTC fazem marketing diretamente para pais expectantes online, mas a maioria ainda processa amostras em laboratórios de referência acreditados; crescimento é rápido a 18,55% de TCAC, porém supervisão regulamentária está se apertando para garantir aconselhamento adequado.
Qual condição cromossômica permanece a aplicação primária?
Síndrome de Down (Trissomia 21) permanece a aplicação líder, representando 48,25% da receita de 2024, embora painéis estejam se ampliando para incluir cromossomos sexuais e síndromes de microdeleção.
Página atualizada pela última vez em:



