Tamanho e Participação do Mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos
Análise do Mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos pela Mordor Intelligence
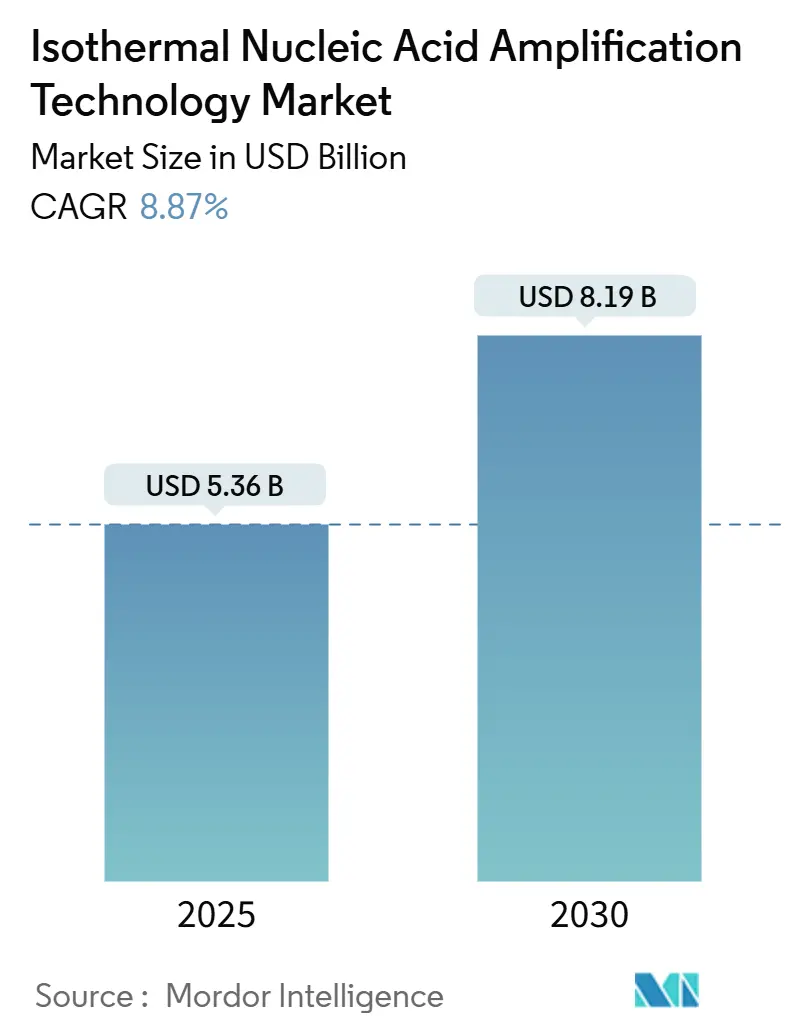
O tamanho do Mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos está estimado em USD 5,36 bilhões em 2025, e deve atingir USD 8,19 bilhões até 2030, a uma TCAC de 8,87% durante o período de previsão (2025-2030).
O crescimento é impulsionado pela amplificação de temperatura constante, que elimina a necessidade de termocicladores volumosos e suporta testes rápidos no ponto de atendimento. Os hospitais implantam plataformas INAAT em unidades de emergência para reduzir o tempo de resposta dos resultados de horas para minutos, enquanto os fornecedores de reagentes beneficiam-se de vendas estáveis de consumíveis com alta margem. Os fabricantes estão integrando microfluídica, reagentes liofilizados e detecção colorimétrica que reduzem os custos por teste e ampliam o uso em ambientes fora do laboratório. A adoção na Ásia-Pacífico acelera à medida que aprovações simplificadas de dispositivos encurtam o tempo de comercialização, enquanto a América do Norte lidera em receita devido às estruturas de reembolso estabelecidas.
Principais Destaques do Relatório
- Por tecnologia, a Amplificação Isotérmica Mediada por Loop (LAMP) liderou com 44,34% de participação na receita em 2024 e está projetada para registrar uma TCAC de 13,36% até 2030.
- Por produto, reagentes e consumíveis representaram 63,56% da receita de 2024, enquanto os instrumentos devem expandir a uma TCAC de 11,24% até 2030.
- Por aplicação, os testes de doenças infecciosas detiveram 53,56% da participação do mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos em 2024; oncologia e biópsia líquida estão previstas para crescer a uma TCAC de 16,11%.
- Por usuário final, hospitais e laboratórios de referência detiveram 56,78% de participação em 2024; locais de ponto de atendimento estão projetados para crescer a uma TCAC de 11,64%.
- Por região, a América do Norte capturou 35,67% da receita em 2024, enquanto a Ásia-Pacífico deve registrar uma TCAC de 15,64% até 2030.
Tendências e Insights do Mercado Global de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos
Análise de Impacto dos Direcionadores
| Direcionador | (~) % Impacto na Previsão TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Adoção de Doenças Infecciosas no Ponto de Atendimento | +2.1% | Global, com ganhos iniciais na América do Norte e UE | Médio prazo (2-4 anos) |
| Envelhecimento Populacional e Carga de Doenças Crônicas | +1.8% | Global, concentrado em mercados desenvolvidos | Longo prazo (≥ 4 anos) |
| Mudança de Fluxo de Trabalho de PCR para INAAT | +1.5% | Núcleo APAC, expansão para MEA | Médio prazo (2-4 anos) |
| Economia de Custo Menor por Teste | +1.3% | Global, acelerado em mercados emergentes | Curto prazo (≤ 2 anos) |
| Cartuchos Microfluídicos Movidos a Bateria | +0.9% | América do Norte e UE, expandindo para APAC | Longo prazo (≥ 4 anos) |
| Especificidade de Ensaio Aprimorada por CRISPR | +0.7% | Global, liderado por instituições de pesquisa | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Adoção de doenças infecciosas no ponto de atendimento
Departamentos de emergência agora dependem de painéis respiratórios INAAT que entregam respostas de qualidade laboratorial em minutos, aumentando o fluxo de pacientes e a administração de antibióticos. A autorização da FDA do Xpert HCV da Cepheid em junho de 2024 permite diagnóstico de hepatite C na mesma visita a partir de uma amostra de sangue da ponta do dedo, um marco que remove a perda de seguimento de múltiplas visitas.[1]U.S. Food and Drug Administration, "FDA Authorizes First Point-of-Care Hepatitis C Test," fda.gov A precisão dos resultados permanece equivalente ao PCR enquanto reações de temperatura constante adequam-se a dispositivos portáteis movidos a bateria úteis em ambientes com recursos limitados.
Envelhecimento populacional e carga de doenças crônicas
Populações acima de 65 anos demandam verificações regulares de biomarcadores para infecções e recorrência de câncer. Sistemas de biópsia líquida baseados em INAAT podem detectar doença residual mínima com 94,1% de sensibilidade, permitindo monitoramento domiciliar ou em clínicas comunitárias.[2]Nature Communications, "Portable Dragonfly Platform Enables Field Molecular Diagnostics," nature.com A integração com plataformas de telemedicina otimiza a revisão de resultados, reduzindo visitas hospitalares desnecessárias e diminuindo custos do sistema.
Mudança de fluxo de trabalho de PCR para INAAT
Laboratórios clínicos que fazem a transição para LAMP relatam 60% menos tempo prático porque as etapas de extração são simplificadas e as reações funcionam em uma única configuração de 60-65°C.[3]Frontiers in Cellular and Infection Microbiology, "Automation-Compatible LAMP Workflows Reduce Hands-On Time," frontiersin.org Copos de reagente liofilizado são enviados em temperatura ambiente e se encaixam em linhas de automação existentes, mantendo alto rendimento enquanto reduzem necessidades de manutenção típicas de termocicladores.
Economia de custo menor por teste
Os custos de capital de instrumentos caem aproximadamente 40% quando aquecedores de temperatura constante substituem cicladores de múltiplas zonas. Leituras colorimétricas removem óptica cara, empurrando custos por teste de alto volume abaixo de USD 5 para alvos respiratórios. A estabilidade de reagentes em temperatura ambiente reduz 20-30% dos gastos com cadeia fria em economias emergentes, acelerando a implantação.
Análise de Impacto das Restrições
| Restrição | (~) % Impacto na Previsão TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Competição de Plataformas PCR e DCR | -1.9% | Global, mais forte em mercados estabelecidos | Médio prazo (2-4 anos) |
| Lacunas de Conscientização e Reembolso | -1.4% | América do Norte e UE principalmente | Curto prazo (≤ 2 anos) |
| Volatilidade de Suprimento de Enzimas para Reagentes Bst | -0.8% | Global, aguda em regiões com restrição de suprimento | Curto prazo (≤ 2 anos) |
| Rigorosas Barreiras de Evidência CLIA-Waiver / IVDR | -1.1% | América do Norte e domínios regulamentares da UE | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Competição de Plataformas PCR e DCR
A infraestrutura PCR estabelecida representa custos significativos de mudança para laboratórios que investiram em plataformas de ciclagem térmica, sistemas automatizados de manuseio de amostras e programas de treinamento de técnicos otimizados para fluxos de trabalho de amplificação tradicionais. Plataformas PCR digitais intensificam ainda mais a competição oferecendo capacidades de quantificação absoluta que o INAAT atualmente não consegue igualar, particularmente em aplicações que requerem monitoramento preciso de carga viral ou análise de variação de número de cópias. Diretores de laboratório citam preocupações com perturbação do fluxo de trabalho ao avaliar a adoção do INAAT, pois procedimentos existentes de controle de qualidade, validações regulamentares e competências da equipe se alinham com metodologias PCR.
Lacunas de conscientização e reembolso
O reconhecimento pelos pagadores de saúde da utilidade clínica do INAAT fica atrás das capacidades da tecnologia, criando incertezas de reembolso que limitam a adoção em ambientes de saúde sensíveis ao custo. O programa MolDX do Medicare requer evidências clínicas extensas demonstrando precisão diagnóstica e melhorias nos resultados dos pacientes antes de estabelecer políticas de cobertura para novas tecnologias de diagnóstico molecular. O processo de geração de evidências normalmente requer 18-24 meses de coleta de dados clínicos, durante os quais os desenvolvedores de INAAT devem financiar estudos sem resultados de reembolso garantidos. A conscientização médica sobre as capacidades do INAAT permanece limitada fora das especialidades de doenças infecciosas, com muitos clínicos optando por testes baseados em PCR familiares apesar das vantagens potenciais em tempo de resposta e implantação no ponto de atendimento.
Análise de Segmentos
Por Tecnologia: Dominância LAMP Impulsiona Inovação
O LAMP capturou 44,34% do mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos em 2024 e está previsto para crescer a 13,36% TCAC até 2030. A metodologia visa seis regiões gênicas, conferindo alta especificidade sem ciclagem térmica. Abordagens complementares como HDA e NEAR abordam casos de uso de baixa temperatura, enquanto TMA mantém valor na triagem sanguínea onde a detecção de RNA importa.
A inovação de detecção está reformulando o mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos à medida que os desenvolvedores combinam LAMP com sistemas CRISPR-Cas para alcançar sensibilidade attomolar em 30 minutos. Tiras de fluxo lateral colorimétricas integram-se diretamente em cartuchos, ampliando a adoção em clínicas que carecem de leitores de fluorescência.
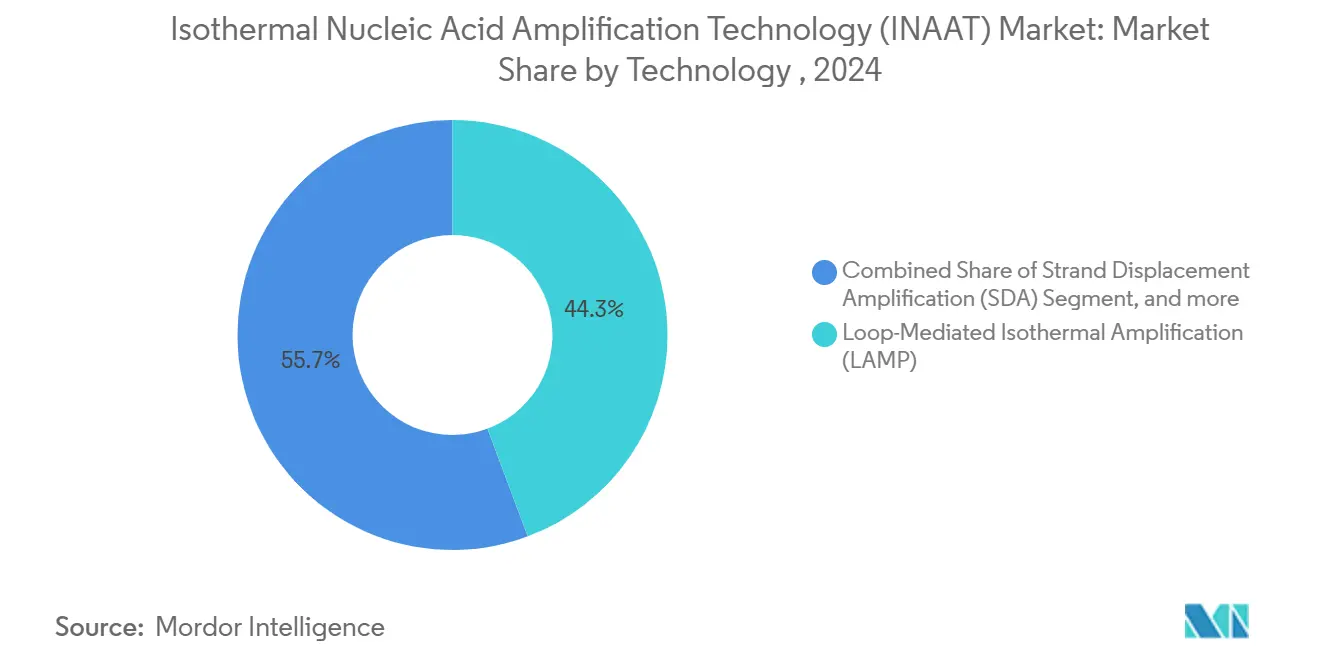
Nota: Participações de segmentos de todos os segmentos individuais disponíveis mediante compra do relatório
Por Produto: Receitas de Reagentes Financiam Inovação de Instrumentos
Reagentes e consumíveis geraram 63,56% da receita de 2024, fornecendo fluxo de caixa recorrente que subsidia P&D. A resiliência do suprimento de polimerase Bst permanece crítica porque sustenta a maioria dos kits INAAT. Os instrumentos devem expandir 11,24% anualmente à medida que fornecedores incorporam microfluídica e extração em uma etapa, evidenciado pelo cartucho de 30 minutos da iPonatic alcançando automação completa do fluxo de trabalho.
A inovação de instrumentos foca em integração e miniaturização, com fabricantes desenvolvendo plataformas portáteis que combinam preparação de amostras, amplificação e detecção em formatos de cartucho de uso único. O sistema iPonatic exemplifica essa tendência, entregando testes completos de ácidos nucleicos dentro de 30 minutos usando extração em temperatura ambiente e capacidades de detecção integradas. A integração microfluídica permite manuseio preciso de fluidos e controle térmico enquanto reduz o consumo de reagentes e riscos de contaminação, embora a complexidade de fabricação e considerações de custo limitem a adoção a aplicações de alto valor.
Por Aplicação: Emergência da Oncologia Desafia Dominância de Doenças Infecciosas
Os testes de doenças infecciosas retiveram 53,56% da receita em 2024, mas perderão participação relativa à medida que a oncologia ganha uma TCAC de 16,11%. A autorização da FDA em 2024 do teste ColoSense de RNA fecal da Geneoscopy confirma o papel do INAAT na triagem não invasiva de câncer. Centros de sangue também dependem do TMA para encurtar períodos de janela viral, sublinhando amplo foco patogênico.
A tração oncológica exemplifica a capacidade do mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos de abordar vigilância contínua, detectando DNA tumoral circulante antes que modalidades de imagem possam confirmar recidiva. Segmentos de segurança alimentar e veterinária adicionam diversidade explorando a tolerância do INAAT para matrizes complexas, apoiando diagnósticos de campo onde laboratórios de cultura são escassos.
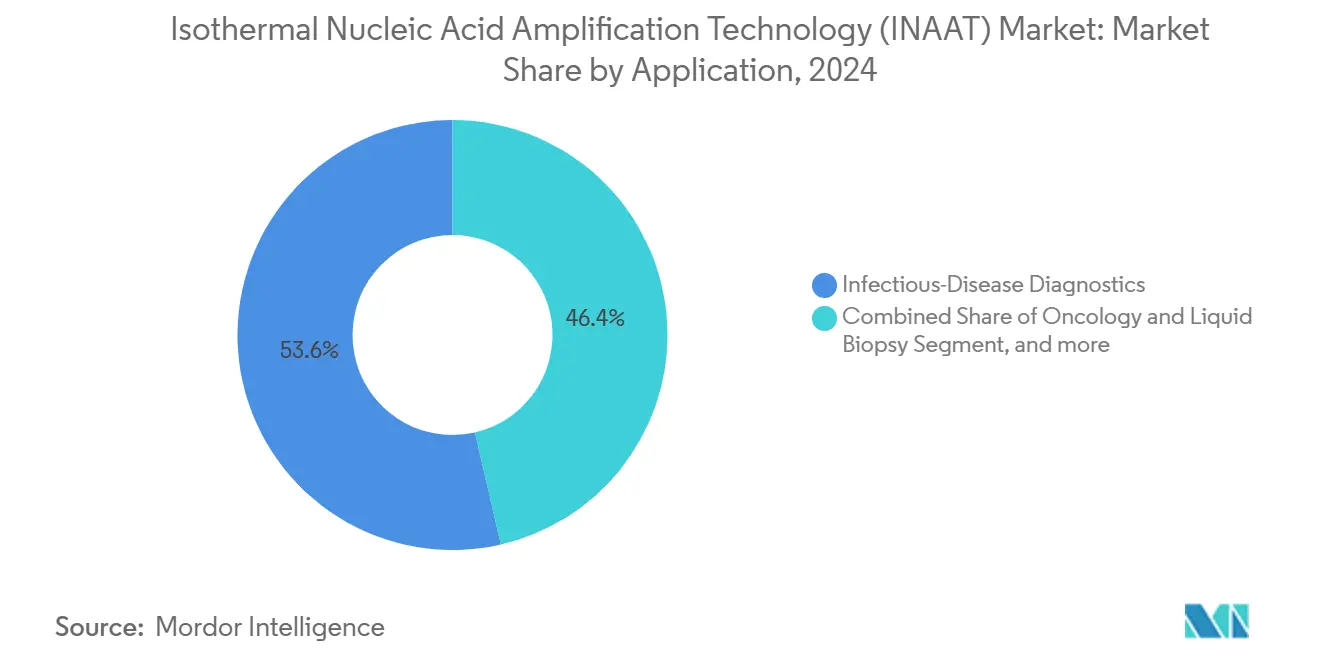
Nota: Participações de segmentos de todos os segmentos individuais disponíveis mediante compra do relatório
Por Usuário Final: Adoção no Ponto de Atendimento Acelera
Hospitais e laboratórios de referência juntos detiveram 56,78% da receita em 2024, aproveitando a infraestrutura molecular existente. Unidades de emergência usam painéis respiratórios de trinta minutos para triar pacientes rapidamente, melhorando o gerenciamento de leitos. Laboratórios de referência adicionam INAAT para testes STAT para se diferenciar de concorrentes PCR de rotina.
Clínicas descentralizadas e cadeias de atendimento urgente devem crescer a 11,64% TCAC, auxiliadas por analisadores baseados em cartuchos que precisam de treinamento mínimo. A estação portátil Dragonfly demonstrou resposta confiável a surtos em regiões remotas sem energia elétrica. Centros acadêmicos continuam a semear avanços que parceiros comerciais escalam, reforçando o ciclo de inovação em todo o mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos.
Análise Geográfica
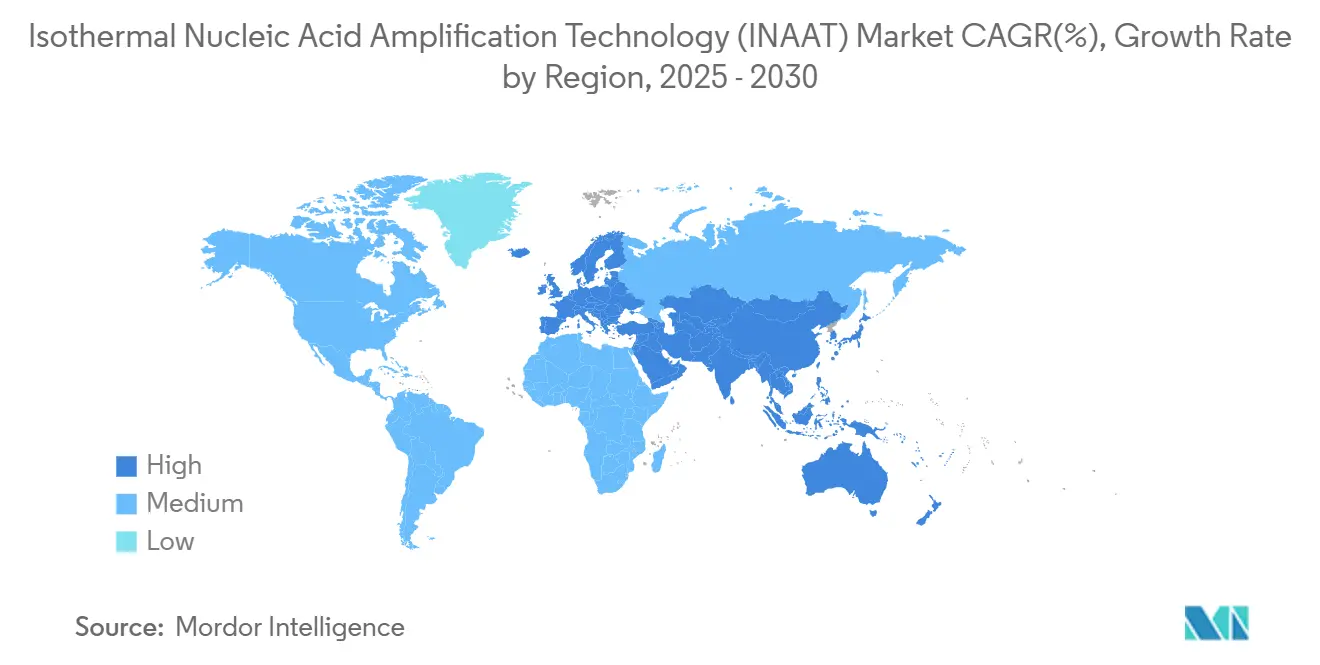
A América do Norte lidera com 35,67% da receita em 2024, sustentada por caminhos da FDA como regras de isenção CLIA que trazem painéis respiratórios de quinze minutos para clínicas fda.gov. A cobertura de seguro extensiva permite que hospitais adotem INAAT sem perturbação orçamentária. Financiamento de pesquisa e capital de risco robusto aceleram lançamentos domésticos de dispositivos.
A Ásia-Pacífico é o motor de crescimento, prevista a 15,64% TCAC. A NMPA da China encurtou cronogramas de revisão de 24 para 12 meses, atraindo multinacionais para localizar a produção nmpa.gov.cn. A população idosa do Japão estimula diagnósticos domiciliares, enquanto programas de saúde pública da Índia adquirem kits INAAT acessíveis para vigilância de tuberculose e dengue. A fabricação local reduz o risco cambial e garante suprimento durante perturbações globais.
A Europa cresce de forma constante à medida que o IVDR harmoniza padrões, embora inovadores menores enfrentem barreiras de evidência mais altas para marcação CE. Alemanha e Reino Unido ancoram a demanda através de redes hospitalares fortes e produção de pesquisa translacional. Políticas de contenção de custos favorecem sistemas de temperatura constante que economizam energia e trabalho comparados ao PCR.
Cenário Competitivo
O mercado permanece moderadamente fragmentado. Abbott, Roche e Qiagen aproveitam redes de clientes instaladas para venda cruzada de cartuchos INAAT, enquanto especialistas de jogo puro como Meridian Bioscience e Molbio Diagnostics focam na amplitude de ensaios. A participação de USD 105 milhões da Bio-Rad na Geneoscopy ilustra a tendência de grandes empresas se associarem para acelerar o lançamento de ensaios oncológicos.
Aquisições expandem capacidades de ponto de atendimento: a bioMérieux comprou a SpinChip Diagnostics em janeiro de 2025 por EUR 111 milhões, adicionando uma plataforma de marcadores cardíacos de 10 minutos que complementa seu conjunto de testes respiratórios. A vantagem competitiva depende da expertise regulamentária porque os pagadores exigem dossiês robustos de utilidade clínica antes que os reembolsos fluam.
Oportunidades de espaço branco persistem em diagnósticos de campo ultra-rápidos e em regiões de baixa infraestrutura onde ensaios de temperatura constante superam o PCR. Fornecedores combinando INAAT com CRISPR ou interpretação de resultados habilitada por IA poderiam garantir nichos premium antes que incumbentes reengenheirem seus portfólios.
Líderes da Indústria de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos
-
Becton Dickinson and Company
-
BioMérieux SA
-
Quidel Corporation
-
Qiagen N.V.
-
Tecan Genomics Inc.
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica

Desenvolvimentos Recentes da Indústria
- Janeiro de 2025: bioMérieux completou aquisição da SpinChip Diagnostics por EUR 111 milhões (USD 116 milhões), obtendo acesso à plataforma inovadora de diagnósticos por imunoensaio projetada para testes no ponto de atendimento com entrega de resultados em 10 minutos a partir de amostras de sangue total. A aquisição fortalece o portfólio de ponto de atendimento da bioMérieux com tecnologia direcionada a marcadores cardíacos para diagnóstico de infarto do miocárdio, com primeiro lançamento de produto esperado em 2026 após marcação CE sob IVDR.
- Janeiro de 2025: Geneoscopy fechou rodada de financiamento Série C de USD 105 milhões liderada pela Bio-Rad Laboratories para apoiar a comercialização do teste de triagem de câncer colorretal ColoSense e avançar o pipeline de diagnósticos de doença inflamatória intestinal. O investimento aproveita a tecnologia PCR Digital por Gotículas da Bio-Rad para aprimorar sensibilidade e especificidade do teste enquanto expande acesso ao mercado através de canais de distribuição estabelecidos.
- Junho de 2024: FDA concedeu autorização de comercialização à Cepheid para o teste Xpert HCV e Sistema GeneXpert Xpress, estabelecendo o primeiro teste de RNA de hepatite C no ponto de atendimento capaz de detectar RNA HCV a partir de amostras de sangue da ponta do dedo com aproximadamente 60 minutos de tempo de resposta. A autorização permite abordagens de testar-e-tratar que abordam barreiras de testes de múltiplas etapas resultando em infecções não tratadas.
- Maio de 2024: FDA aprovou o dispositivo ColoSense da Geneoscopy para detecção qualitativa de marcadores de RNA associados à neoplasia colorretal e hemoglobina oculta em amostras de fezes, marcando o primeiro teste fecal baseado em RNA para adultos de 45 anos ou mais em risco médio para câncer colorretal. A aprovação inclui requisitos de estudo pós-mercado com inscrição de 12.500 sujeitos ao longo de 36 meses para confirmar eficácia clínica.
Escopo do Relatório Global do Mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos
Conforme o escopo do relatório, as tecnologias de amplificação de ácidos nucleicos são usadas no campo da biologia molecular e tecnologias de DNA recombinante. Essas técnicas são usadas como métodos líderes na detecção e análise de um pequeno número de ácidos nucleicos. Os protocolos de tecnologia de amplificação isotérmica de ácidos nucleicos são variados e têm muitas vantagens, pois é extremamente rápida e não requer termocicladores. O Mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos (INAAT) é segmentado Por Tecnologia (Amplificação Dependente de Helicase (HDA), Reação de Amplificação por Enzima de Corte (NEAR), Amplificação Isotérmica Mediada por Loop (LAMP), Amplificação por Deslocamento de Fita (SDA), Amplificação Baseada em Sequência de Ácidos Nucleicos (NASBA), Amplificação Mediada por Transcrição (TMA), Amplificação Isotérmica de Primer Único (SPIA), Outras Tecnologias), Por Produto (Instrumentos e Reagente), Por Usuário Final (Hospital, Laboratórios de pesquisa, Outros Usuários Finais), e Geografia (América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África, e América do Sul). O relatório de mercado também cobre os tamanhos de mercado estimados e tendências para 17 países diferentes nas principais regiões, globalmente. O relatório oferece o valor (em milhões de USD) para os segmentos acima.
| Amplificação Dependente de Helicase (HDA) |
| Reação de Amplificação por Enzima de Corte (NEAR) |
| Amplificação Isotérmica Mediada por Loop (LAMP) |
| Amplificação por Deslocamento de Fita (SDA) |
| Amplificação Baseada em Sequência de Ácidos Nucleicos (NASBA) |
| Amplificação Mediada por Transcrição (TMA) |
| Amplificação Isotérmica de Primer Único (SPIA) |
| Outras Tecnologias |
| Instrumentos |
| Reagentes e Consumíveis |
| Diagnósticos de Doenças Infecciosas |
| Oncologia e Biópsia Líquida |
| Triagem Sanguínea e Segurança Transfusional |
| Testes de Segurança Alimentar e Hídrica |
| Diagnósticos Veterinários e Agrícolas |
| Hospitais e Laboratórios de Referência |
| Ponto de Atendimento / Clínicas Descentralizadas |
| Institutos Acadêmicos e de Pesquisa |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Resto da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Resto do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Tecnologia | Amplificação Dependente de Helicase (HDA) | |
| Reação de Amplificação por Enzima de Corte (NEAR) | ||
| Amplificação Isotérmica Mediada por Loop (LAMP) | ||
| Amplificação por Deslocamento de Fita (SDA) | ||
| Amplificação Baseada em Sequência de Ácidos Nucleicos (NASBA) | ||
| Amplificação Mediada por Transcrição (TMA) | ||
| Amplificação Isotérmica de Primer Único (SPIA) | ||
| Outras Tecnologias | ||
| Por Produto | Instrumentos | |
| Reagentes e Consumíveis | ||
| Por Aplicação | Diagnósticos de Doenças Infecciosas | |
| Oncologia e Biópsia Líquida | ||
| Triagem Sanguínea e Segurança Transfusional | ||
| Testes de Segurança Alimentar e Hídrica | ||
| Diagnósticos Veterinários e Agrícolas | ||
| Por Usuário Final | Hospitais e Laboratórios de Referência | |
| Ponto de Atendimento / Clínicas Descentralizadas | ||
| Institutos Acadêmicos e de Pesquisa | ||
| Por Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Resto do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Principais Perguntas Respondidas no Relatório
O que está impulsionando o crescimento recente no mercado de Tecnologia de Amplificação Isotérmica de Ácidos Nucleicos?
Rápida adoção no ponto de atendimento, menores custos de instrumentos e suporte regulamentário contínuo na América do Norte e Ásia-Pacífico estão impulsionando uma TCAC de 8,87% até 2030.
Qual segmento de tecnologia lidera o mercado?
A Amplificação Isotérmica Mediada por Loop detém 44,34% da receita e também é o segmento de crescimento mais rápido a 13,36% TCAC.
Quais regiões estão se expandindo mais rapidamente?
A Ásia-Pacífico está prevista para crescer a 15,64% TCAC devido a aprovações simplificadas e investimento em infraestrutura.
Quais aplicações oferecem o maior crescimento futuro?
Testes de oncologia e biópsia líquida devem expandir a 16,11% TCAC à medida que a triagem não invasiva de câncer ganha aceitação médica e do pagador.
Quais são as principais barreiras para adoção mais ampla do INAAT?
Infraestrutura PCR incumbente, lacunas de reembolso e volatilidade do suprimento de enzimas permanecem as principais restrições afetando a adoção nos próximos dois a quatro anos.
Página atualizada pela última vez em:



