Tamanho e Participação do Mercado de Dispositivos Médicos Vestíveis da Europa
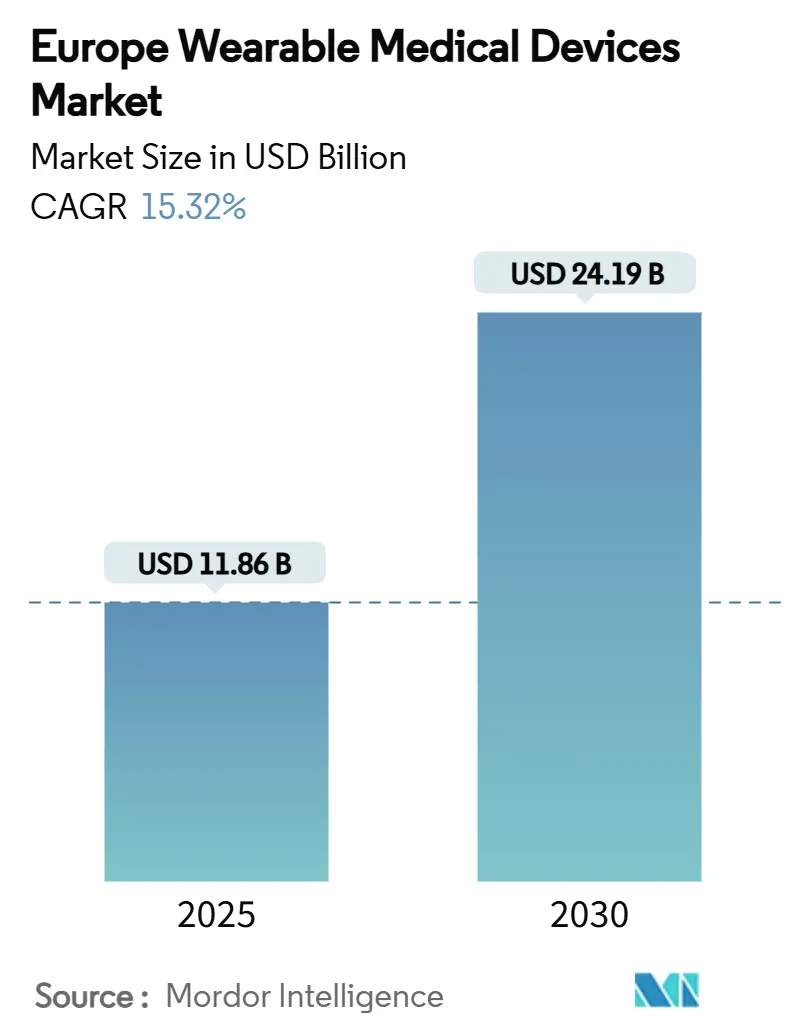
Análise do Mercado de Dispositivos Médicos Vestíveis da Europa pela Mordor Intelligence
O tamanho do mercado de dispositivos médicos vestíveis da Europa posiciona-se em USD 11,86 mil milhões em 2025 e projeta-se que atinja USD 24,19 mil milhões até 2030, refletindo uma TCCA de 15,32% durante o período de previsão. A harmonização regulamentar em curso sob o Regulamento de Dispositivos Médicos (RDM), a prevalência de doenças crónicas e a escassez de recursos humanos estão a impulsionar a adoção de monitorização contínua em contextos clínicos e de consumo. Os enquadramentos nacionais de reembolso-mais notavelmente a Lei de Cuidados Digitais da Alemanha-estão a reposicionar os vestíveis clinicamente validados como terapias prescritíveis em vez de acessórios de bem-estar, enquanto EUR 403 milhões em novo financiamento de inovação da UE está a acelerar os pipelines de produtos para dispositivos de próxima geração. A diversificação da cadeia de abastecimento, avanços na colheita de energia e stacks de sensores multimodais estão a reduzir as barreiras do fator de forma e a permitir maior duração dos dispositivos. Ao mesmo tempo, as regras fragmentadas de partilha de dados pós-RGPD e as preocupações de precisão dos médicos moderam o momentum de curto prazo, mantendo a validação clínica central nas estratégias de expansão do mercado.
Principais Conclusões do Relatório
- Por tipo de dispositivo, os vestíveis de diagnóstico e monitorização comandaram 62,55% da participação do mercado de dispositivos médicos vestíveis da Europa em 2024; os vestíveis terapêuticos estão previstos expandir a uma TCCA de 15,73% até 2030.
- Por grupo etário, o segmento abaixo dos 18 foi o coorte de crescimento mais rápido a uma TCCA de 16,29% entre 2025 e 2030; o grupo 18-60 reteve 60,22% do tamanho do mercado de dispositivos médicos vestíveis da Europa em 2024.
- Por canal de distribuição, os vendedores offline representaram 53,39% da receita em 2024, embora os canais online estejam a expandir a uma TCCA de 15,50% durante o horizonte de previsão.
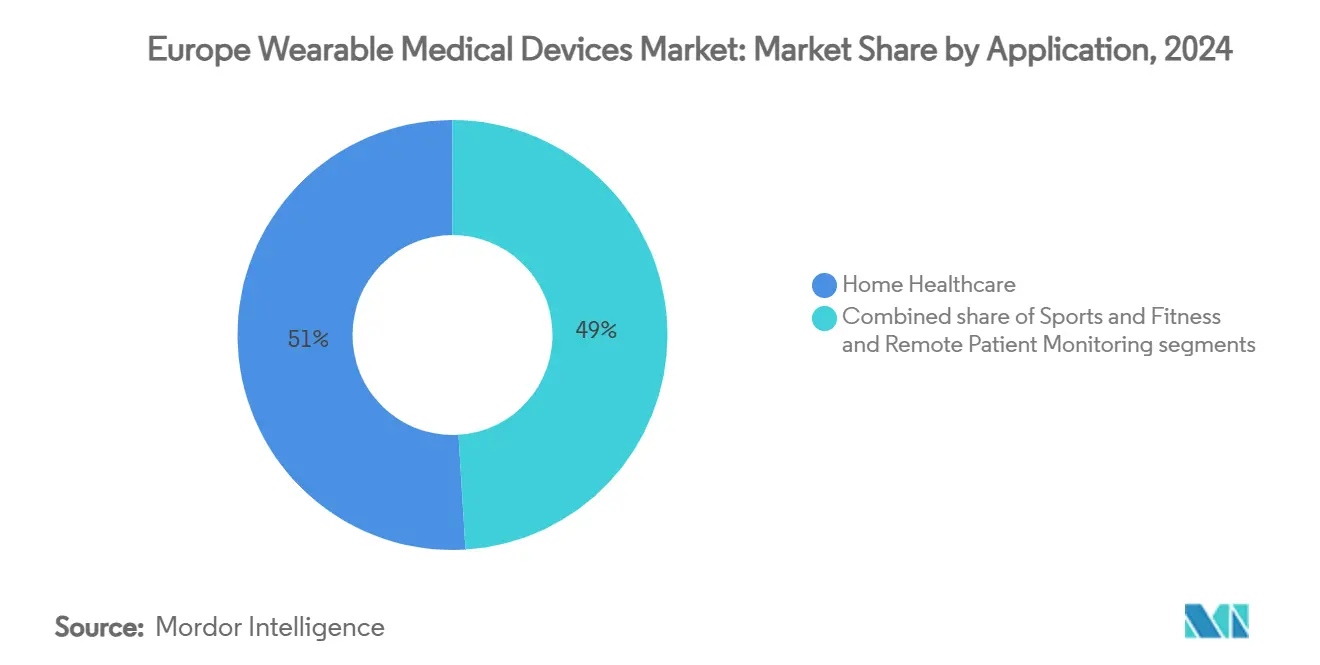
- Por aplicação, os cuidados de saúde domiciliários representaram 50,96% da participação do mercado de dispositivos médicos vestíveis da Europa em 2024, enquanto as aplicações de desporto e fitness estão a avançar a uma TCCA de 15,84% até 2030.
- Por utilizador final, os consumidores detiveram 63,07% da participação do mercado de dispositivos médicos vestíveis da Europa em 2024 e estão previstos crescer a uma TCCA de 15,61% até 2030; hospitais e clínicas permanecem os segundos maiores compradores.
- Por geografia, a Alemanha liderou com 28,37% de participação na receita em 2024, enquanto o Reino Unido deverá registar a mais alta TCCA de 15,94% até 2030.
Tendências e Insights do Mercado de Dispositivos Médicos Vestíveis da Europa
Análise do Impacto dos Impulsionadores
| Impulsionador | (~) % Impacto na Previsão TCCA | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Impulso regulamentar para vestíveis médicos aprovados pelo RDM | +2.8% | Toda a UE (mais forte na Alemanha, França) | Médio prazo (2-4 anos) |
| Miniaturização rápida de sensores e chips multimodais | +2.1% | Global, centros de fabrico da UE | Longo prazo (≥ 4 anos) |
| Programas de bem-estar corporativo financiados por empregadores | +1.9% | Alemanha, Reino Unido, Países Baixos | Curto prazo (≤ 2 anos) |
| Mudança dos pagadores de saúde para modelos baseados em resultados | +1.6% | Países nórdicos, Alemanha, Reino Unido | Médio prazo (2-4 anos) |
| Micro-colheita de energia para remover fricção de carregamento | +1.2% | Global, liderança I&D da UE | Longo prazo (≥ 4 anos) |
| Pilotos de reembolso de terapêuticas digitais da UE | +0.9% | Alemanha, França, Países Baixos | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Impulso Regulamentar para Vestíveis Médicos Aprovados pelo RDM
A aplicação do RDM desde 2021 obrigou os participantes do mercado de dispositivos médicos vestíveis da Europa a provar o desempenho clínico, transformando os vestíveis de gadgets de estilo de vida em ferramentas médicas regulamentadas. Os requisitos elevados de acompanhamento clínico pós-comercialização[1]Grupo de Coordenação de Dispositivos Médicos, "MDCG 2023-7 Aplicação prática do Artigo 61," HEALTH.EC.EUROPA.EUImpulsionadores criam ciclos de dados contínuos que melhoram a precisão algorítmica, mas cronogramas de certificação mais longos favorecem incumbentes ricos em capital. As cláusulas de segurança de materiais estão a incitar mudanças para polímeros biocompatíveis, estimulando inovações de design sustentável. Coletivamente, estes fatores aumentam a confiança dos médicos e elevam as barreiras de entrada para pequenas startups não especializadas.
Miniaturização Rápida de Sensores e Chips Multimodais
A micro-fabricação permitiu que chips únicos monitorizem múltiplos sinais vitais, reduzindo o volume dos dispositivos e alargando os casos de uso. O CGM+ da Trinity Biotech integra glicose contínua, temperatura e sensores de hidratação numa patch do tamanho de uma moeda, ilustrando esta mudança. O consumo de energia caiu para níveis de microwatt, estendendo a vida da bateria e abrindo caminho para módulos de colheita de energia. A liberdade de design encoraja diversos fatores de forma-desde patches adesivas a implantáveis-expandindo a adoção do mercado de dispositivos médicos vestíveis da Europa entre coortes pediátricas e geriátricas.
Mudança dos Pagadores de Saúde para Modelos Baseados em Resultados
Os pagadores nacionais estão a ligar os reembolsos a endpoints clínicos, incentivando os fabricantes de dispositivos a fornecer dados de resultados em vez de métricas brutas. O caminho DiGA da Alemanha[2]Lasse Cirkel, "Adoção e perceção de aplicações de saúde digital prescritíveis (DiGA) e a digitalização avançada entre médicos de medicina interna alemães: um estudo de inquérito transversal," Lasse Cirke, bmchealthservres.biomedcentral.com , por exemplo, reembolsa apps e dispositivos apenas após benefício comprovado ao paciente, fomentando desenvolvimento algorítmico mais forte e envolvimento de longo prazo do paciente. Ao monetizar a prevenção de eventos-como admissões de emergência reduzidas-o modelo assegura uso sustentado do dispositivo e sustenta a trajetória de dois dígitos do mercado de dispositivos médicos vestíveis da Europa.
Pilotos de Reembolso de Terapêuticas Digitais da UE
As aprovações "Fast-Track" DiGA da Alemanha[3]Robby Bräuniger, "O Mercado de Saúde Digital na Alemanha," Germany Trade & Invest, gtai.de desencadearam pilotos imitadores em França e nos Países Baixos, criando modelos progressivos de reembolso. Mais de 50 apps e vestíveis agora qualificam-se para cobertura estatutária, sinalizando futura harmonização do financiamento de terapia digital. Integrar dados contínuos de sensores com intervenções comportamentais eleva os vestíveis de ferramentas de monitorização para terapias de primeira linha, alargando o alcance do mercado de dispositivos médicos vestíveis da Europa.
Análise do Impacto das Restrições
| Restrição | (~) % Impacto na Previsão TCCA | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Regras fragmentadas de partilha de dados da UE pós-RGPD | -1.8% | Toda a UE (mais complexo na Alemanha) | Curto prazo (≤ 2 anos) |
| Risco da cadeia de abastecimento de fornecedores de baterias centrados na China | -1.3% | Global, vulnerabilidade da UE | Médio prazo (2-4 anos) |
| Ciclos de substituição de adotantes precoces em estagnação | -0.9% | Alemanha, Reino Unido, Países Baixos | Curto prazo (≤ 2 anos) |
| Ceticismo sobre precisão de grau clínico entre médicos | -0.7% | Sistemas de saúde conservadores da UE | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Regras Fragmentadas de Partilha de Dados da UE Pós-RGPD
As diferenças nacionais nas interpretações do RGPD obrigam os fabricantes a redesenhar fluxos de consentimento para cada mercado, atrasando lançamentos pan-UE. Os fornecedores permanecem cautelosos em integrar dados contínuos em registos eletrónicos devido à exposição de responsabilidade e risco de litígio de privacidade. Estes silos impedem modelos de análise preditiva que dependem de conjuntos de dados transnacionais, restringindo a escalabilidade do mercado de dispositivos médicos vestíveis da Europa até que surjam orientações harmonizadas.
Ceticismo sobre Precisão de Grau Clínico Entre Médicos
Uma revisão sistemática de 2024[4]Melanie Rabe, "Uso de Dados de Saúde Gerados pelo Paciente a partir de Dispositivos de Grau de Consumidor por Profissionais de Saúde," Journal of Medical Internet Research, jmir.org encontrou dependência médica limitada em sinais vitais derivados do consumidor devido a precisão inconsistente, especialmente em ambientes não controlados. As lacunas de formação e medos de responsabilidade restringem caminhos de cuidados baseados em dados, sublinhando a necessidade de estudos de validação robustos e métricas de precisão padronizadas antes da integração clínica em larga escala.
Análise de Segmentos
Por Tipo de Dispositivo: Diagnósticos Impulsionam Integração Clínica
Os vestíveis de diagnóstico e monitorização entregaram 62,55% da participação do mercado de dispositivos médicos vestíveis da Europa em 2024, confirmando as prioridades hospitalares e dos pagadores para vigilância contínua sobre terapia no dispositivo. O subsegmento está definido para crescer a 15,73% até 2030, impulsionado pela prevalência de doenças crónicas e mandatos de monitorização pós-alta. Os monitores contínuos de glicose lideram o crescimento, beneficiando de enzimas catalíticas melhoradas e calibração sem fios. As patches de sinais vitais agora agrupam sensores de ECG, SpO₂ e frequência respiratória, reduzindo orçamentos de equipamento para programas de tele-UCI. Os vestíveis terapêuticos permanecem nicho mas mostram pontos brilhantes na neuromodulação e entrega de insulina em ciclo fechado. Estimuladores autónomos em energia e bombas patch estão a reduzir o fardo do paciente, encorajando adoção mais ampla da endocrinologia. Estas tendências cimentam o mercado de dispositivos médicos vestíveis da Europa como pedra angular dos cuidados preditivos e centrados no ambulatório.
Os dispositivos terapêuticos possuem o restante da participação do segmento e estão a pivotar para algoritmos específicos de condições que titulam terapia em tempo real. As plataformas de gestão da dor combinam estimulação elétrica com feedback biométrico, abordando mandatos de redução de opióides. Os vestíveis respiratórios equipados com classificadores AI de tosse encontraram utilidade pós-COVID-19, enquanto exo-mangas de reabilitação transmitem telemetria de amplitude de movimento para fisioterapeutas. A diferenciação de segmentos agora gira em torno de evidência clínica, transparência algorítmica e conformidade RDM-fatores que definem posições vencedoras dentro do mercado de dispositivos médicos vestíveis da Europa.
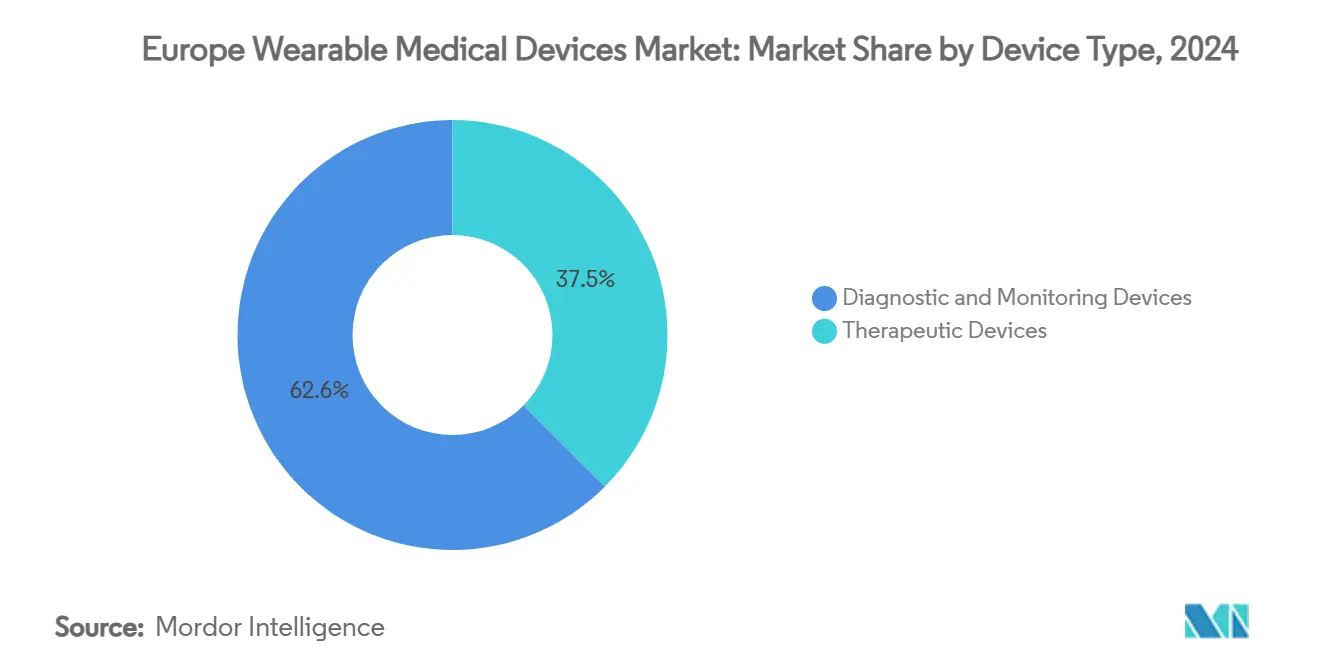
Nota: Participações de segmento de todos os segmentos individuais disponíveis na compra do relatório
Por Grupo Etário: Adoção Jovem Acelera
Os utilizadores com idades entre 18-60 adquiriram 60,22% do tamanho do mercado de dispositivos médicos vestíveis da Europa em 2024, apoiados por subsídios de bem-estar de empregadores e produtos de seguros digitais-first. No entanto, a adoção abaixo dos 18 está a expandir a uma TCCA de 16,29%, auxiliada pela procura parental por sensores de diabetes pediátrica e programas de bem-estar baseados em escolas. Designs com dashboards gamificados e bandas de desgaste tamanho infantil melhoram o envolvimento, reduzindo taxas de abandono. Para idosos, simplicidade de interface e colheita de energia são primordiais. Pingentes de deteção de quedas noturnas e berços de carregamento de baixa destreza visam pontos de dor geriátrica comuns. À medida que a demografia da UE se inclina mais velha, a adoção de longo prazo depende da integração de cuidadores e monitorização remota apoiada por reembolso-ambos pivotais para o mercado de dispositivos médicos vestíveis da Europa.
Os clínicos relatam maior aderência entre menores nativos digitais comparado a idosos, criando conjuntos de dados longitudinais que reforçam algoritmos de cuidados preventivos. Os decisores políticos veem a monitorização da vida precoce como uma alavanca de poupança de custos vitalícios, reforçando o financiamento governamental para ensaios pediátricos. Em todos os grupos, o coaching personalizado enraizado na ciência comportamental está a elevar o envolvimento sustentado do dispositivo, um KPI crítico para modelos de negócio de receita recorrente na indústria de dispositivos médicos vestíveis da Europa.
Por Canal de Distribuição: Validação Clínica Impulsiona Preferência Offline
Os canais offline detiveram 53,39% da participação do mercado de dispositivos médicos vestíveis da Europa em 2024, pois prescritores, farmácias e retalhistas especializados fornecem ajuste, calibração e documentação requerida pelo RDM-todos essenciais para aceitação clínica. Os hospitais frequentemente agrupam dispositivos em kits de alta, impulsionando vendas offline enquanto reduzem penalidades de readmissão. Entretanto, os canais online estão a avançar a 15,50% TCCA, apoiados pela expansão da telesaúde e integrações de e-prescrição. Os portais direto-ao-consumidor apresentam verificadores de sintomas, onboarding virtual e suporte de chat AI, fornecendo educação escalável. O e-commerce transfronteiriço enfrenta fricções regulamentares, contudo processos de IVA simplificados e equivalência de marca CE com UKCA podem alargar o alcance, sustentando ganhos online dentro do mercado de dispositivos médicos vestíveis da Europa.
À medida que chatbots AI lidam com suporte de primeira linha, as plataformas online estão a cortar custos operacionais, permitindo aos fabricantes igualar preços com outlets físicos. No entanto, a falta de ajuste físico pode prejudicar a precisão do sensor, estimulando modelos híbridos onde os utilizadores recolhem dispositivos em farmácias após compra online. Espera-se que a mistura de canais convirja para equilibrium, otimizando conveniência e credenciamento clínico para compradores do mercado de dispositivos médicos vestíveis da Europa.
Por Aplicação: Dominância dos Cuidados de Saúde Domiciliários Reflete Evolução do Modelo de Cuidados
Os cuidados de saúde domiciliários capturaram 50,96% do tamanho do mercado de dispositivos médicos vestíveis da Europa em 2024, pois os sistemas de saúde mudam cuidados para configurações de menor custo. Os pilotos hospital-em-casa emparelham patches de sinais vitais com dashboards de enfermagem, reduzindo drasticamente custos de internamento e libertando capacidade de cama. Os pacotes de cuidados crónicos para insuficiência cardíaca e DPOC incluem protocolos de triagem de escalada, demonstrando poupanças do pagador que reforçam a penetração do mercado de dispositivos médicos vestíveis da Europa. O segmento de desporto e fitness, embora menor, está a crescer mais rapidamente a 15,84% TCCA, pois sensores de grau clínico migram para vestíveis de bem-estar. Parcerias entre marcas de vestuário desportivo e OEMs de sensores estão a pioneirizar análises de performance baseadas em evidência, borrando fronteiras consumidor-médicas.
A monitorização remota de pacientes (MRP) abrange os domínios médico e bem-estar, atuando como campo de teste para modelos de reembolso ligados à redução de eventos. Os fabricantes de dispositivos devem navegar faixas de conformidade dupla-diretivas de dispositivos médicos e regulamentos de dados do consumidor-enquanto entregam insights acionáveis. A capacidade de se conectar a ecossistemas de tele-reabilitação e cuidados virtuais determinará a relevância de longo prazo de cada cluster de aplicação dentro do mercado de dispositivos médicos vestíveis da Europa.
Por Utilizador Final: Empoderamento do Consumidor Impulsiona Crescimento do Mercado
Os consumidores representaram 63,07% da receita de 2024, pois dispositivos aprovados pelo RDM tornaram-se prontos para prateleira para autocuidado. As apps companheiras traduzem sinais vitais clínicos em dashboards amigáveis ao utilizador, alimentando envolvimento diário formador de hábitos. Análises de subscrição e serviços de cloud estão a expandir a receita média por utilizador, sustentando a rentabilidade em todo o mercado de dispositivos médicos vestíveis da Europa. Hospitais e clínicas, a segunda maior coorte, implementam vestíveis para vigilância pós-operatória, permitindo alta mais precoce e prevenção de custos. Instalações de cuidados de longo prazo aproveitam o rastreamento contínuo de sinais vitais para mitigar escassez de pessoal, enquanto centros cirúrgicos ambulatórios adotam patches de sensores de uso único para supervisão de recuperação do mesmo dia.
Plataformas de grau empresarial oferecendo vistas multi-paciente, ganchos EMR e trilhos de auditoria atendem necessidades de governança institucional. Os OEMs de consumo que entram no domínio clínico devem elevar cibersegurança e rastreabilidade para níveis RDM. Inversamente, jogadores tradicionais de med-tech estão a melhorar disfarces de experiência do utilizador emprestados de eletrónica de consumo, sinalizando convergência que moldará a intensidade competitiva dentro do mercado de dispositivos médicos vestíveis da Europa.
Análise Geográfica
A Alemanha deteve 28,37% da receita de 2024, ancorada pelo motor de reembolso da Lei de Cuidados Digitais que posiciona vestíveis digitalmente prescritos como ferramentas terapêuticas mainstream. Mais de EUR 4 mil milhões em subvenções de digitalização hospitalar estabeleceram a infraestrutura para conectividade sensor-para-EMR sem costura, fomentando adoção sistemática. Interpretações RGPD regionais rigorosas, no entanto, impõem processos de consentimento de múltiplas camadas, complicando implementações multinacionais. A população envelhecida da Alemanha e altos gastos de saúde per capita continuam a criar terreno fértil para soluções de monitorização remota, sustentando sua liderança no mercado de dispositivos médicos vestíveis da Europa.
O Reino Unido, livre dos cronogramas RDM, está a moldar um regime regulamentar ágil através da MHRA que promete ciclos de aprovação de 12 meses, ficando abaixo das médias da UE. O financiamento do Plano de Longo Prazo do NHS e alvos de enfermarias virtuais estão a impulsionar aquisição de patches de sinais vitais e detetores AI de arritmia, impulsionando uma TCCA de 15,94% até 2030. Arquiteturas de dados nativas da cloud e frameworks de aquisição centralizados aceleram escala, compensando fricção da cadeia de abastecimento relacionada com Brexit.
França, Itália e Espanha exibem progresso cauteloso, equilibrando demandas rigorosas de evidência HTA com cargas crescentes de cuidados crónicos. O dossier de reembolso de França agora inclui biomarcadores digitais, sugerindo cobertura mais ampla para vestíveis uma vez que a custo-efetividade seja provada. A pegada madura de registos eletrónicos de saúde de Itália auxilia pilotos regionais, embora com disparidades de financiamento entre províncias. Espanha prioriza programas de envelhecimento-no-local; no entanto, orçamentos de saúde restringidos retardam escala nacional. Os estados nórdicos, embora menores, servem como laboratórios vivos para modelos de monitorização AI-first, enquanto a Europa Oriental oferece oportunidades greenfield onde estratégias mobile-first podem saltar infraestruturas legadas.
Panorama Competitivo
A competição é moderada e inclina-se para incumbentes com portfolios clínicos robustos e conhecimento regulamentar. Medtronic, Abbott e Philips detêm franquias cardiometabólicas fortes, aproveitando anos de dados pós-comercialização para refinar algoritmos. Gigantes de consumo Apple e Samsung estão a ganhar progressivamente marcas CE para funções ECG e oxigénio no sangue, erodindo participação tradicional de med-tech. Alianças estratégicas tipificam manobras de mercado: o investimento de USD 75 milhões da Dexcom na ŌURA funde telemetria contínua de glicose com análises de estilo de vida para aprofundar insights do paciente.
O investimento está a fluir para camadas de diagnóstico AI que transformam biosinais brutos em previsões acionáveis. Start-ups especializadas em baterias de estado sólido e colheita de energia estão a tornar-se alvos de aquisição para principais de dispositivos que procuram eliminar o carregamento como ponto de fricção. A repatriação da cadeia de abastecimento para a Europa está a emergir como diferenciador, pois empresas respondem a riscos de sourcing de bateria e escrutínio de pegada de carbono. Nos próximos cinco anos, a captura de valor dependerá de precisão de grau clínico, reembolso ligado a evidência e ecossistemas de dados interoperáveis-elementos que definem liderança no mercado de dispositivos médicos vestíveis da Europa.
Líderes da Indústria de Dispositivos Médicos Vestíveis da Europa
-
Abbott Laboratories
-
Apple Inc.
-
Koninklijke Philips N.V.
-
Medtronic plc
-
Samsung Electronics Co., Ltd.
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica


Desenvolvimentos Recentes da Indústria
- Julho 2025: A UE atribuiu EUR 403 milhões a inovadores de dispositivos médicos, acelerando ensaios clínicos e registos regulamentares para vestíveis de próxima geração.
- Junho 2025: PharmaSens e SiBionics fizeram parceria para desenvolver uma bomba patch vestível de insulina visando gestão de diabetes em ciclo fechado.
- Novembro 2024: Dexcom investiu USD 75 milhões na ŌURA para fundir monitorização contínua de glicose com anéis holísticos de rastreamento de saúde.
- Junho 2024: B-Secur e Galen Data colaboraram em análises ECG ligadas à cloud visando reduzir alertas falsos de arritmia em monitores cardíacos vestíveis.
Âmbito do Relatório do Mercado de Dispositivos Médicos Vestíveis da Europa
Conforme o âmbito do relatório, dispositivos médicos vestíveis são dispositivos autónomos capazes de diagnosticar ou monitorizar condições médicas, combinados com informação de saúde digital, tipicamente usados sobre o corpo. Estes dispositivos possuem características, tais como sensores fisiológicos não invasivos, módulos de processamento de dados, feedback médico e capacidades de transmissão de dados sem fios. O Mercado de Dispositivos Médicos Vestíveis da Europa está segmentado por Tipo de Dispositivo (Dispositivos de Monitorização e Dispositivos Terapêuticos), Aplicação (Desporto e Fitness, Monitorização Remota de Pacientes e Cuidados de Saúde Domiciliários), Tipo de Produto (Relógio, Pulseira, Dispositivo Auricular e Outros Tipos de Produto), e Geografia. O relatório oferece o valor (em milhões USD) para os segmentos acima.
| Dispositivos de Diagnóstico e Monitorização | Dispositivos de Monitorização de Sinais Vitais |
| Dispositivos de Monitorização do Sono | |
| Monitores Contínuos de Glicose | |
| Monitores de Pressão Arterial | |
| Outros Dispositivos de Diagnóstico e Monitorização | |
| Dispositivos Terapêuticos | Dispositivos de Gestão da Dor |
| Dispositivos de Reabilitação | |
| Dispositivos de Terapia Respiratória | |
| Dispositivos de Administração de Insulina | |
| Outros Dispositivos Terapêuticos |
| Abaixo dos 18 |
| 18 - 60 |
| Acima dos 60 |
| Online |
| Offline |
| Desporto e Fitness |
| Monitorização Remota de Pacientes |
| Cuidados de Saúde Domiciliários |
| Consumidores |
| Hospitais e Clínicas |
| Centros de Cuidados de Longo Prazo |
| Centros Cirúrgicos Ambulatórios |
| Outros |
| Alemanha |
| Reino Unido |
| França |
| Itália |
| Espanha |
| Resto da Europa |
| Por Tipo de Dispositivo | Dispositivos de Diagnóstico e Monitorização | Dispositivos de Monitorização de Sinais Vitais |
| Dispositivos de Monitorização do Sono | ||
| Monitores Contínuos de Glicose | ||
| Monitores de Pressão Arterial | ||
| Outros Dispositivos de Diagnóstico e Monitorização | ||
| Dispositivos Terapêuticos | Dispositivos de Gestão da Dor | |
| Dispositivos de Reabilitação | ||
| Dispositivos de Terapia Respiratória | ||
| Dispositivos de Administração de Insulina | ||
| Outros Dispositivos Terapêuticos | ||
| Por Grupo Etário | Abaixo dos 18 | |
| 18 - 60 | ||
| Acima dos 60 | ||
| Por Canal de Distribuição | Online | |
| Offline | ||
| Por Aplicação | Desporto e Fitness | |
| Monitorização Remota de Pacientes | ||
| Cuidados de Saúde Domiciliários | ||
| Por Utilizador Final | Consumidores | |
| Hospitais e Clínicas | ||
| Centros de Cuidados de Longo Prazo | ||
| Centros Cirúrgicos Ambulatórios | ||
| Outros | ||
| Por Geografia | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||


Questões Principais Respondidas no Relatório
Que fator regulamentar mais fortemente impulsiona a adoção de dispositivos médicos vestíveis em toda a Europa?
A aplicação completa do Regulamento de Dispositivos Médicos (RDM) posiciona os vestíveis como ferramentas clinicamente validadas, dando confiança aos médicos para prescrever dispositivos que atendem requisitos de segurança e performance de grau hospitalar.
Como é que os empregadores europeus estão a influenciar a adoção de vestíveis de grau médico?
Os programas de bem-estar corporativo agora subsidiam dispositivos capazes de glicose contínua ou monitorização cardíaca, ligando o uso a absentismo reduzido e custos de seguro menores
Que avanço tecnológico é esperado estender o uso do dispositivo sem intervenção do utilizador?
Módulos de colheita de energia a bordo-tais como componentes cinéticos, térmicos e fotovoltaicos-estão a eliminar a necessidade de carregamento rotineiro, uma característica especialmente valiosa para pacientes idosos e de cuidados crónicos.
Por que é que os clínicos permanecem cautelosos sobre integrar vestíveis de grau de consumidor em vias de cuidados?
Persistem preocupações sobre precisão de medição variável e exposição de responsabilidade; os médicos preferem dispositivos apoiados por estudos de validação revistos por pares e métricas de precisão padronizadas.
Como é que as plataformas de vendas online estão a mudar modelos de suporte para vestíveis médicos?
Os canais de e-commerce incluem cada vez mais onboarding virtual e suporte ao cliente impulsionado por AI, permitindo aos utilizadores receber orientação de ajuste remoto e resolução de problemas sem visitas presenciais.
Que risco da cadeia de abastecimento se tornou um ponto focal para fabricantes europeus?
A dependência pesada de fornecedores de baterias de lítio-íon chineses coloca ameaças de disrupção, incitando iniciativas de repatriação e exploração de químicas de células alternativas dentro da UE.
Página atualizada pela última vez em:









