Taille et part du marché des cellules souches en Amérique du Nord
Analyse du marché des cellules souches en Amérique du Nord par Mordor Intelligence
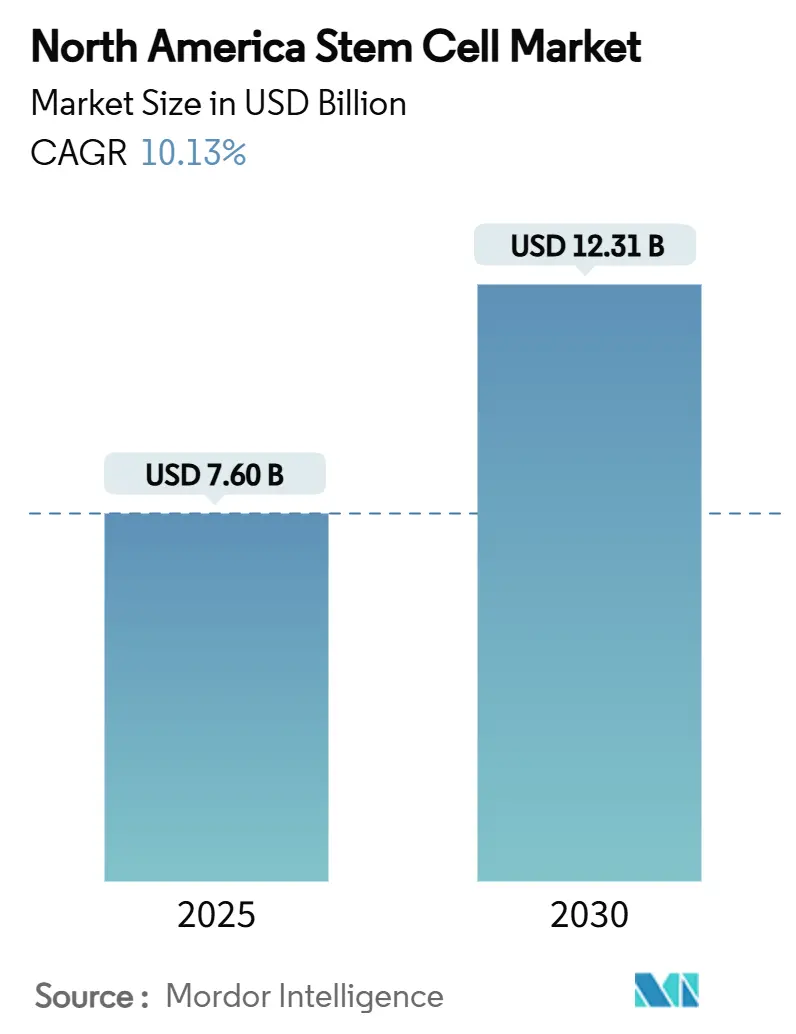
La taille du marché des cellules souches en Amérique du Nord est estimée à 7,60 milliards USD en 2025, et devrait atteindre 12,31 milliards USD d'ici 2030, à un TCAC de 10,13 % au cours de la période de prévision (2025-2030). Un mélange décisif de voies accélérées de la FDA, de liquidités profondes de capital-investissement et de centres de fabrication basés dans les hôpitaux propulse le marché des cellules souches en Amérique du Nord vers une expansion soutenue à deux chiffres. Les désignations Fast-track et Regenerative Medicine Advanced Therapy (RMAT) raccourcissent les délais de développement, tandis que les subventions du Pentagone et des Affaires des anciens combattants transfèrent les innovations de champ de bataille vers les environnements de soins civils, élargissant davantage le bassin de patients adressable. En parallèle, les objectifs de décarbonation des entreprises orientent les capitaux vers le ' biotraitement vert ', donnant aux précurseurs un avantage en termes de coûts et d'image de marque. Collectivement, ces forces du côté de la demande et de l'offre renforcent la position de la région comme banc d'essai mondial pour les thérapies régénératives de nouvelle génération.
Points clés du rapport
- Par type de produit, les cellules souches adultes ont détenu 51,86 % de la part du marché des cellules souches en Amérique du Nord en 2024 ; les cellules souches pluripotentes induites (iPSC) devraient se développer à un TCAC de 9,86 % jusqu'en 2030.
- Par application, les traitements orthopédiques ont capturé 25,12 % de la part des revenus en 2024, tandis que les troubles neurologiques devraient accélérer à un TCAC de 11,56 % jusqu'en 2030.
- Par type de traitement, la thérapie allogénique a commandé 60,16 % de la part de la taille du marché des cellules souches en Amérique du Nord en 2024 ; la thérapie autologue progresse à un TCAC de 11,96 % sur 2025-2030.
- Par utilisateur final, les instituts académiques et de recherche ont représenté 36,34 % de la part en 2024, tandis que les entreprises biopharmaceutiques et biotechnologiques devraient croître à un TCAC de 12,23 % jusqu'en 2030.
- Par géographie, les États-Unis ont mené avec 88,16 % de la part des revenus en 2024 ; le Canada devrait afficher le TCAC le plus rapide de 12,08 % sur la période de perspectives.
Tendances et perspectives du marché des cellules souches en Amérique du Nord
Analyse d'impact des moteurs
| Moteur | (~) % d'impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Désignations accélérées FDA Fast-Track et RMAT | +1.8% | États-Unis, avec retombées au Canada | Court terme (≤ 2 ans) |
| Montée du financement par capital-investissement pour les plateformes MSC prêtes à l'emploi | +1.5% | Amérique du Nord, concentré dans les pôles biotechnologiques | Moyen terme (2-4 ans) |
| Expansion des centres de cellules souches affiliés aux hôpitaux à travers les États-Unis | +1.2% | États-Unis, réseaux hospitaliers régionaux | Moyen terme (2-4 ans) |
| Intégration de CRISPR avec les pipelines iPSC | +1.4% | Amérique du Nord, avec concentration R&D dans les grandes villes | Long terme (≥ 4 ans) |
| Subventions du Pentagone et VA pour les programmes régénératifs de blessures de guerre | +0.9% | États-Unis, centres médicaux militaires | Court terme (≤ 2 ans) |
| Politiques de décarbonation des entreprises stimulant la demande de ' biotraitement vert ' | +0.7% | Amérique du Nord, régions intensives en fabrication | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Désignations accélérées FDA Fast-Track et RMAT
Un mandat RMAT plus large a reconfiguré le marché des cellules souches en Amérique du Nord en réduisant de moitié les délais de développement historiques. L'approbation du remestemcel-L pour la maladie du greffon contre l'hôte pédiatrique a validé l'efficacité des cellules souches mésenchymateuses et encouragé les sponsors à déposer des demandes similaires en neurologie et cardiologie.[1]Source: American Association of Blood Banks, "FDA Approves First Cell Therapy for Rare Eye Disease," aabb.org Encelto, la première thérapie génique allogénique encapsulée pour maladie oculaire rare, montre davantage la tolérance des régulateurs pour les plateformes de livraison innovantes. Alors que les tests de puissance gagnent en consensus, les analystes industriels s'attendent à ce que les approbations RMAT couvrent au moins 25 indications distinctes d'ici 2028, cimentant le marché des cellules souches en Amérique du Nord comme le baromètre réglementaire mondial.
Montée du financement par capital-investissement pour les plateformes MSC prêtes à l'emploi
Les tours de série A et série B dépassant 20 millions USD ciblent désormais couramment les lignes de fabrication allogéniques automatisées. La levée de 22 millions USD de Kincell Bio, réservée uniquement à l'expansion de la production de cellules stromales mésenchymateuses (MSC) polyvalentes, souligne l'inclinaison des investisseurs vers les plateformes avec un potentiel d'économies d'échelle. Avec des coûts par dose projetés pour chuter de 500 000 USD à 50 000 USD une fois l'automatisation mature, le marché des cellules souches en Amérique du Nord assiste à une course pilotée par le capital-risque pour construire les premières ' usines de cellules ' verticalement intégrées de la région.
Expansion des centres de cellules souches affiliés aux hôpitaux à travers les États-Unis
Les systèmes hospitaliers à but non lucratif internalisent les flux de travail régénératifs. L'installation de Durham de Cryo-Cell International illustre la tendance-combinant l'admission des patients, le traitement des cellules et les essais cliniques sous un même toit. Chaque satellite réduit les fuites de référencement et raccourcit les délais veine-à-veine, donnant aux hôpitaux des avantages de maîtrise des coûts tout en élargissant l'accès aux populations communautaires. Les institutions médicales diplômantes adoptent des centres similaires, intégrant la recherche translationnelle directement dans les parcours des patients.
Intégration de CRISPR avec les pipelines iPSC
La lignée iPSC éditée par CRISPR de Century Therapeutics, conçue pour échapper à la surveillance immunitaire de l'hôte, est entrée en essais de Phase I après avoir démontré des efficacités de knock-in constantes supérieures à 80 %. Les efforts parallèles à la Northeastern University appliquent des algorithmes d'apprentissage automatique pour prédire le succès d'édition et les ajustements de milieux de culture, réduisant les taux d'échec de lots d'environ 35 %. Ces avancées déplacent le marché des cellules souches en Amérique du Nord des protocoles manuels vers une production contrôlée numériquement, alignant l'ingénierie de précision avec la reproductibilité réglementaire.
Analyse d'impact des contraintes
| Contrainte | (~) % d'impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| COGS élevés de la fabrication allogénique à échelle GMP | -2.1% | Amérique du Nord, régions intensives en fabrication | Moyen terme (2-4 ans) |
| Règles de remboursement disparates au niveau des États | -1.6% | États-Unis, variation État par État | Court terme (≤ 2 ans) |
| Risque de pénurie de donneurs dans les chaînes d'approvisionnement autologues | -1.3% | Amérique du Nord, régions dépendantes du registre de donneurs | Long terme (≥ 4 ans) |
| Préoccupations de tumorogénicité ralentissant les approbations pluripotentes | -1.8% | Amérique du Nord, régions de surveillance réglementaire | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
COGS élevés de la fabrication allogénique à échelle GMP
Les thérapies allogéniques de grade GMP coûtent encore 3-4 fois plus cher que les biologiques traditionnels en raison des contrôles qualité intensifs et des exigences de main-d'œuvre qualifiée.[2]Source: BioProcess International Staff, "Automation of Cell Therapy Biomanufacturing," bioprocessintl.com Les plateformes d'automatisation d'Ori Biotech promettent 70 % d'économies de main-d'œuvre, mais les dépenses en capital restent prohibitives pour les entreprises émergentes. Les organisations de développement et fabrication sous contrat (CDMO) connaissent une surcapacité dans certains segments tout en faisant face à des pénuries dans les capacités spécialisées, créant une volatilité des prix qui impacte l'économie globale du marché.
Règles de remboursement disparates au niveau des États
Le statut de la Floride de 2025 permettant les traitements non approuvés par la FDA sous supervision médicale illustre l'environnement de remboursement fragmenté. Les critères de payeurs divergents à travers Anthem, Cigna et Medicare compliquent le codage et les réclamations, forçant les fournisseurs à maintenir des protocoles de facturation multicouches. La couverture inégale prolonge le délai jusqu'aux revenus et obscurcit la visibilité de la taille du marché, particulièrement pour les petites cliniques qui ancrent la demande rurale. Le manque de critères de remboursement standardisés limite également la capacité des systèmes de santé à développer des protocoles de traitement cohérents, impactant potentiellement les résultats cliniques et les analyses coût-efficacité.
Analyse des segments
Par type de produit : Les cellules souches adultes détiennent le leadership des revenus tandis que l'élan iPSC se construit
Les cellules souches adultes ont contrôlé 51,86 % du marché des cellules souches en Amérique du Nord en 2024, soutenues par des décennies de données de sécurité et un précédent réglementaire rationalisé. Leur utilisation clinique établie dans les troubles orthopédiques, hématologiques et auto-immuns sécurise une demande récurrente, mais les limites de scalabilité demeurent pour les indications à gros volume. Les homologues pluripotents induits, bien que plus petits aujourd'hui, grimpent à un TCAC de 9,86 % alors que l'intégration CRISPR et les bioréacteurs en système fermé révisent l'économie de production.
L'optimisation de culture guidée par IA devrait réduire les échecs de lots iPSC et compresser les coûts, positionnant les lignées éditées génétiquement pour un déploiement allogénique large au cours de la prochaine décennie. Les contraintes éthiques continuent de confiner les cellules embryonnaires humaines aux programmes de recherche de niche, assurant que les lignées adultes et iPSC façonneront le cœur commercial du paysage industriel des cellules souches en Amérique du Nord. La dynamique concurrentielle entre ces types de produits est de plus en plus pilotée par l'économie de fabrication plutôt que par des considérations purement scientifiques, avec des entreprises recherchant l'équilibre optimal entre sécurité, efficacité et viabilité commerciale.
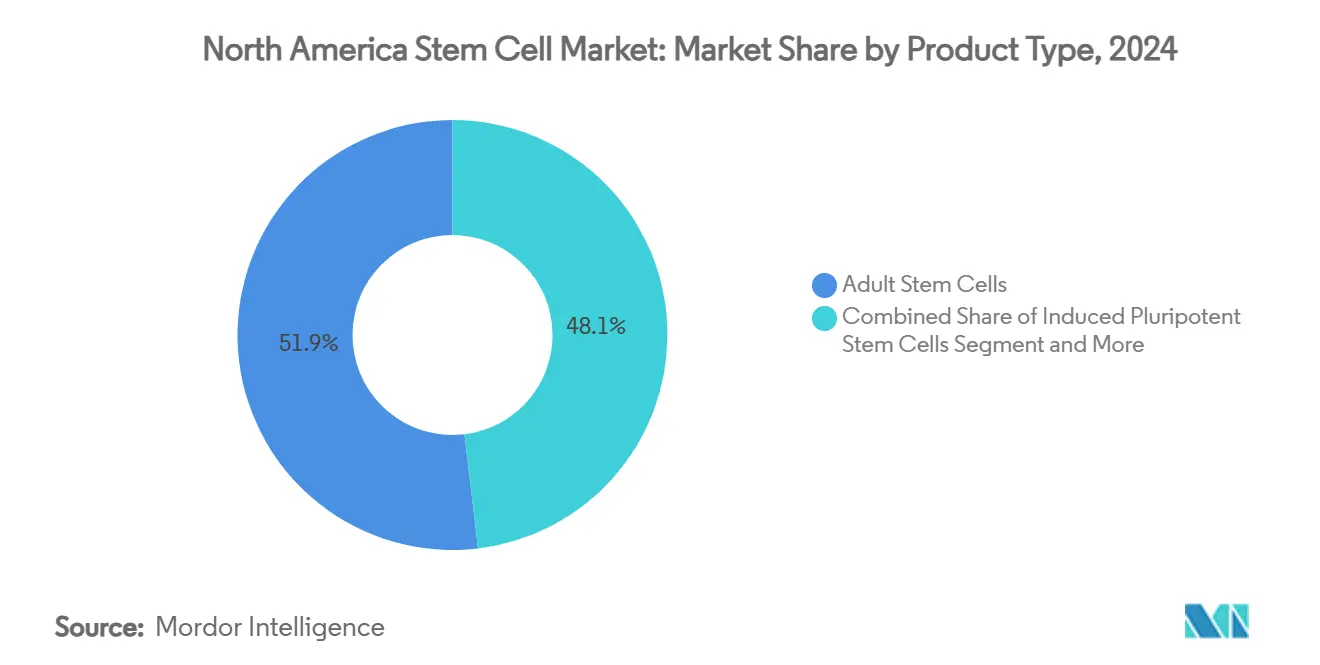
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par application : La dominance orthopédique fait face à la montée neurologique
Les procédures orthopédiques ont représenté 25,12 % des revenus de 2024, tirant parti d'applications intra-articulaires et spinales bien établies qui s'alignent avec la familiarité des chirurgiens et les voies de remboursement.[3]Source: International Journal of Spine Surgery Researchers, "Regenerative Options for Degenerative Disc Disease," ijssurgery.com Cependant, les indications neurologiques devraient afficher un TCAC de 11,56 % alors que les essais première-chez-l'humain pour la maladie de Parkinson, les blessures de la moelle épinière et la sclérose en plaques valident des améliorations fonctionnelles durables.
Le financement robuste du Département de la Défense pour les blessures cérébrales et nerveuses traumatiques accélère les pipelines translationnels, renforçant la confiance parmi les payeurs civils. L'oncologie, les segments cardiovasculaires et de soins des plaies fournissent un avantage auxiliaire mais nécessiteront des gains de rendement de processus continus pour tempérer les préoccupations de coût des marchandises à travers le marché des cellules souches en Amérique du Nord. Le paysage d'application est de plus en plus piloté par le besoin médical non satisfait plutôt que par la faisabilité technique, avec des entreprises se concentrant sur les conditions où les cellules souches peuvent fournir des avantages thérapeutiques uniques non disponibles par les produits pharmaceutiques traditionnels.
Par type de traitement : L'échelle allogénique rencontre la personnalisation autologue
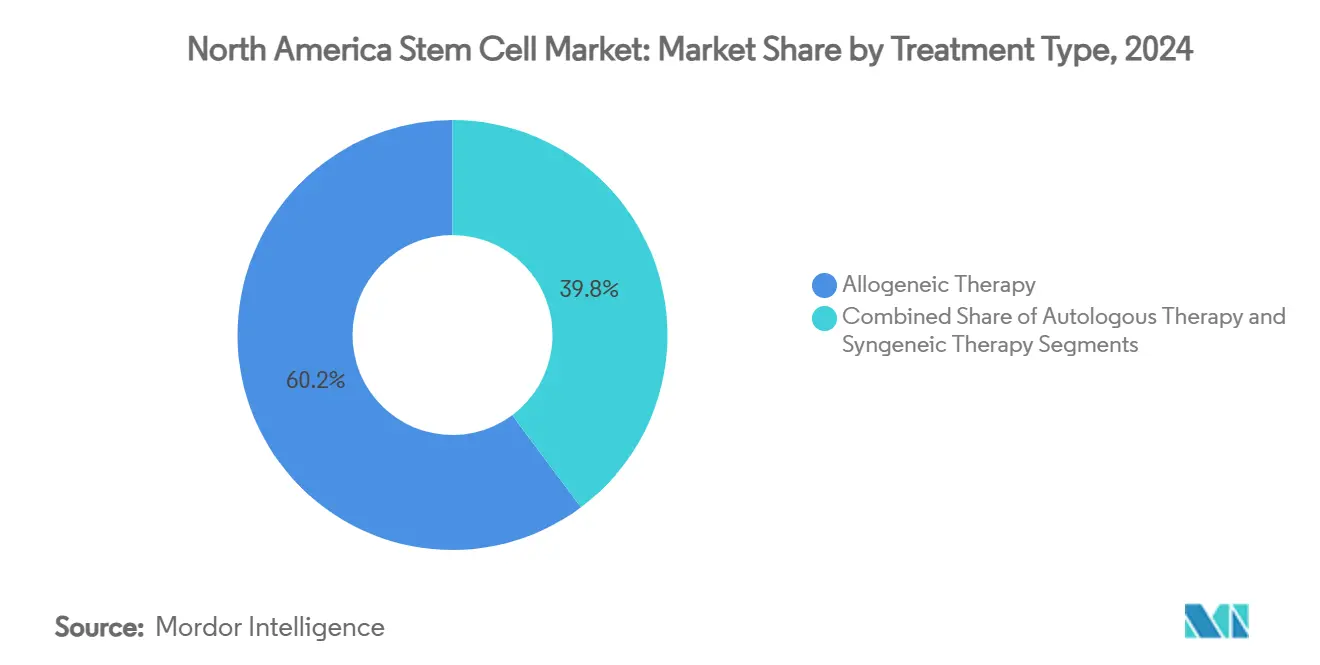
Les thérapies allogéniques ont livré 60,16 % de la part de la taille du marché des cellules souches en Amérique du Nord en 2024 parce qu'un lot de donneur peut traiter des centaines de patients, optimisant l'utilisation des installations. Pourtant, le TCAC de 11,96 % de la thérapie autologue souligne comment les avancées de mobilisation des donneurs et les systèmes point-of-care rendent les interventions le jour même faisables, réduisant les frais généraux logistiques.
Les concepts hybrides ' personnalisés prêts à l'emploi '-cellules de donneurs universels conçues pour échapper à l'immunité de l'hôte-sont en cours d'évaluation, promettant de mélanger l'échelle allogénique avec la sécurité autologue. Si validés, ils pourraient rediriger la part au sein du marché des cellules souches en Amérique du Nord d'ici 2030. Les entreprises poursuivent des approches hybrides qui combinent les avantages de scalabilité de la fabrication allogénique avec les avantages de sécurité du traitement autologue, créant potentiellement de nouveaux segments de marché qui font le pont entre les catégories de traitement traditionnelles.
Par utilisateur final : L'académie mène, la biopharmacie accélère
Les instituts académiques et de recherche ont capturé 36,34 % de la part en 2024, tirant parti du financement de subventions et de l'infrastructure IRB pour initier les études première-chez-l'humain. Les hôpitaux accélèrent les centres internes pour retenir les patients, tandis que les banques de sang de cordon se positionnent comme fournisseurs en amont de lignées cellulaires validées.
Les entreprises biopharmaceutiques et biotechnologiques, se développant à un TCAC de 12,23 %, passent de la dépendance aux licences à la commercialisation interne. Leurs ambitions de mise à l'échelle-alimentées par les injections de capital-investissement-se traduisent par une demande accrue pour les consommables automatisés et les logiciels d'analyse, approfondissant la résilience de la chaîne d'approvisionnement pour l'industrie plus large des cellules souches en Amérique du Nord. Le paysage des utilisateurs finaux est de plus en plus caractérisé par la collaboration plutôt que la concurrence, avec des institutions académiques partenaires d'entreprises biopharmaceutiques pour tirer parti des forces complémentaires en recherche et commercialisation.
Analyse géographique
Les États-Unis ont représenté 88,16 % des revenus de 2024 et restent le noyau réglementaire et de fabrication du marché des cellules souches en Amérique du Nord. Les désignations RMAT, plus un effet de clustering à Boston et dans la Bay Area, ancrent les afflux de capitaux et de talents. La législation permissive de la Floride de 2025 catalyse une nouvelle cohorte de cliniques détenues par des médecins, bien qu'avec une acceptation mitigée des payeurs.
Le Canada, projeté pour enregistrer un TCAC de 12,08 %, bénéficie d'une infusion fédérale de 30 millions CAD pour élargir l'usine de Vancouver de STEMCELL Technologies, renforçant la capacité GMP domestique et attirant les collaborations d'essais cliniques américains. La couverture de santé à payeur unique nationale peut rationaliser le remboursement une fois que les seuils d'efficacité clinique sont atteints, positionnant le Canada comme un adjuvant à forte croissance au sein du marché des cellules souches en Amérique du Nord.
La part du Mexique est modeste mais en hausse sur le tourisme médical ; cependant, l'opacité réglementaire et l'accréditation inégale des installations tempèrent l'expansion à court terme. L'échange de connaissances transfrontalier et les partenariats de fabrication suggèrent une harmonisation progressive au cours des cinq prochaines années, renforçant la sécurité d'approvisionnement continental pour le marché des cellules souches en Amérique du Nord.
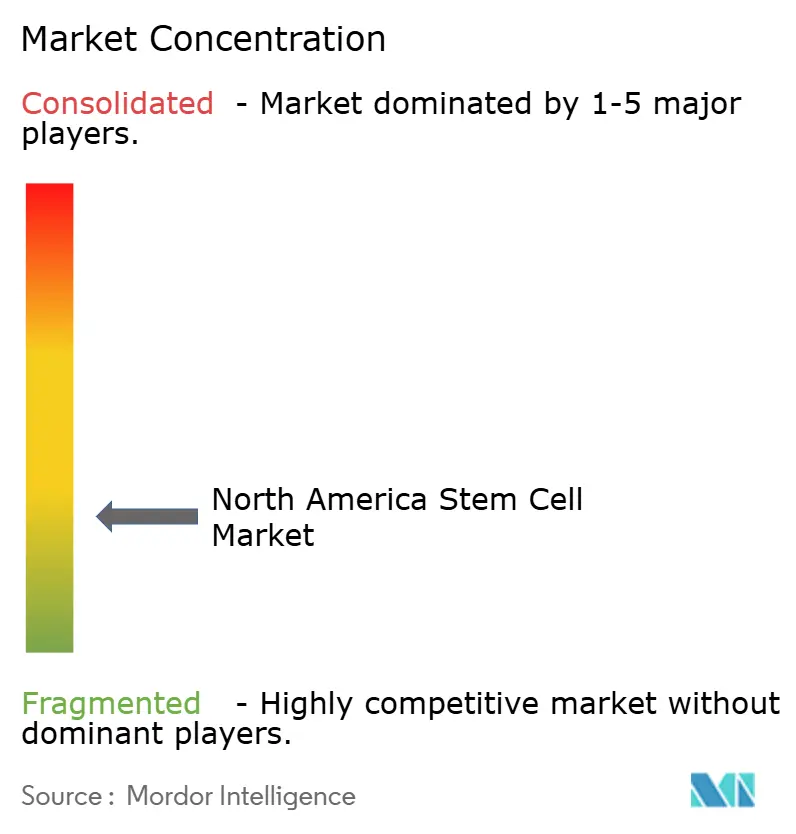
Paysage concurrentiel
Thermo Fisher Scientific, et Merck KGaA dominent les niches d'équipements, réactifs et fabrication sous contrat, fournissant des plateformes standardisées qui soutiennent la conformité GMP. Pendant ce temps, les entreprises axées sur la thérapie telles que Mesoblast, Fate Therapeutics et Lineage Cell Therapeutics font progresser les pipelines de phase tardive à travers l'orthopédie, l'oncologie et la neurologie. L'achat de 425 millions USD d'EsoBiotec par AstraZeneca illustre l'appétit des grandes pharmas pour le savoir-faire en thérapie cellulaire par acquisition.
Les spécialistes de l'automatisation comme Cellares et Ori Biotech misent leur valeur sur les suites de fabrication clés en main capables de 70 % d'économies de main-d'œuvre, établissant de nouvelles bases de coûts et intensifiant la concurrence par les prix sur le marché des cellules souches en Amérique du Nord. Les partenariats ' biotraitement vert ' pilotés par l'ESG entre Cytiva et Cellular Origins fournissent des avantages de précurseur parmi les acheteurs visant à réduire les empreintes carbone de 25 %.
Les perturbateurs intégrant l'édition CRISPR avec les lignées allogéniques iPSC, tels que Century Therapeutics, peuvent redessiner les frontières concurrentielles en fusionnant la scalabilité avec l'évasion immunitaire. Si les constructions de donneurs universels atteignent le succès d'essai pivot, les plateformes autologues incumbantes peuvent confronter une obsolescence accélérée, élevant l'impulsion stratégique pour les joint-ventures et le licensing technologique au sein du marché des cellules souches en Amérique du Nord.
Leaders de l'industrie des cellules souches en Amérique du Nord
-
Becton, Dickinson and Company
-
Thermo Fisher Scientific
-
Lineage Cell Therapeutics, Inc.,
-
Merck KGaA (Sigma Aldrich)
-
Bristol-Myers Squibb Company
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Avril 2025 : Le Maryland Stem Cell Research Fund a attribué 18 millions USD à des projets régénératifs en phase précoce.
- Mars 2025 : RegeneCyte a reçu l'approbation FDA pour sa thérapie de cellules souches de sang de cordon, marquant un jalon pour les applications de cellules souches périnatales.
- Juillet 2024 : Le Gouvernement du Canada a investi 22,5 millions USD pour élargir l'installation de biofabrication de STEMCELL Technologies en Colombie-Britannique, attendue pour créer plus de 1 000 emplois.
Portée du rapport sur le marché des cellules souches en Amérique du Nord
Selon la portée du rapport, les cellules souches sont des cellules biologiques qui peuvent se différencier en d'autres types de cellules. De plus, divers types de cellules souches sont utilisés à des fins thérapeutiques. Avec de multiples applications au stade clinique pour diverses maladies, celles-ci sont explorées de manière extensive par un grand nombre d'entreprises biopharmaceutiques ces derniers temps. Le marché des cellules souches en Amérique du Nord est segmenté par type de produit (cellule souche adulte, cellule embryonnaire humaine, cellule souche pluripotente, et autres types de produits), application (troubles neurologiques, traitements orthopédiques, troubles oncologiques, blessures et plaies, troubles cardiovasculaires, et autres applications), type de traitement (thérapie de cellules souches allogéniques, thérapie de cellules souches autologues, et thérapie de cellules souches syngéniques) et géographie. Le rapport offre la valeur (en millions USD) pour les segments ci-dessus.
| Cellules souches adultes |
| Cellules souches pluripotentes induites |
| Cellules souches embryonnaires humaines |
| Autres types de produits |
| Troubles neurologiques |
| Traitements orthopédiques |
| Troubles oncologiques |
| Troubles cardiovasculaires |
| Blessures et plaies |
| Autres applications |
| Thérapie allogénique |
| Thérapie autologue |
| Thérapie syngénique |
| Hôpitaux et cliniques spécialisées |
| Instituts académiques et de recherche |
| Entreprises biopharmaceutiques et biotechnologiques |
| Banques de cellules souches |
| Autres utilisateurs finaux |
| États-Unis |
| Canada |
| Mexique |
| Par type de produit | Cellules souches adultes |
| Cellules souches pluripotentes induites | |
| Cellules souches embryonnaires humaines | |
| Autres types de produits | |
| Par application | Troubles neurologiques |
| Traitements orthopédiques | |
| Troubles oncologiques | |
| Troubles cardiovasculaires | |
| Blessures et plaies | |
| Autres applications | |
| Par type de traitement | Thérapie allogénique |
| Thérapie autologue | |
| Thérapie syngénique | |
| Par utilisateur final | Hôpitaux et cliniques spécialisées |
| Instituts académiques et de recherche | |
| Entreprises biopharmaceutiques et biotechnologiques | |
| Banques de cellules souches | |
| Autres utilisateurs finaux | |
| Par géographie | États-Unis |
| Canada | |
| Mexique |
Questions clés répondues dans le rapport
Quelle est la taille actuelle du marché des cellules souches en Amérique du Nord ?
La taille du marché des cellules souches en Amérique du Nord est de 7,60 milliards USD en 2025.
Quel TCAC est attendu pour le marché jusqu'en 2030 ?
Le marché devrait croître à un TCAC de 10,13 % entre 2025 et 2030.
Quel type de produit domine les revenus ?
Les cellules souches adultes mènent avec 51,86 % de part de marché, grâce à leur long historique de sécurité.
Pourquoi les applications neurologiques gagnent-elles en traction ?
Les essais révolutionnaires dans la maladie de Parkinson et les blessures de la moelle épinière pilotent un TCAC de 11,56 % dans les segments neurologiques.
Comment les plateformes d'automatisation influencent-elles les coûts de fabrication ?
Les solutions d'entreprises comme Cellares pourraient réduire les dépenses de main-d'œuvre jusqu'à 70 %, abaissant les prix par dose et accélérant la mise à l'échelle.
Quelle géographie montre la croissance la plus rapide ?
Le Canada devrait enregistrer un TCAC de 12,08 %, soutenu par l'investissement fédéral dans l'infrastructure de biofabrication.
Dernière mise à jour de la page le:



