细胞培养市场规模和份额
魔多智能细胞培养市场分析
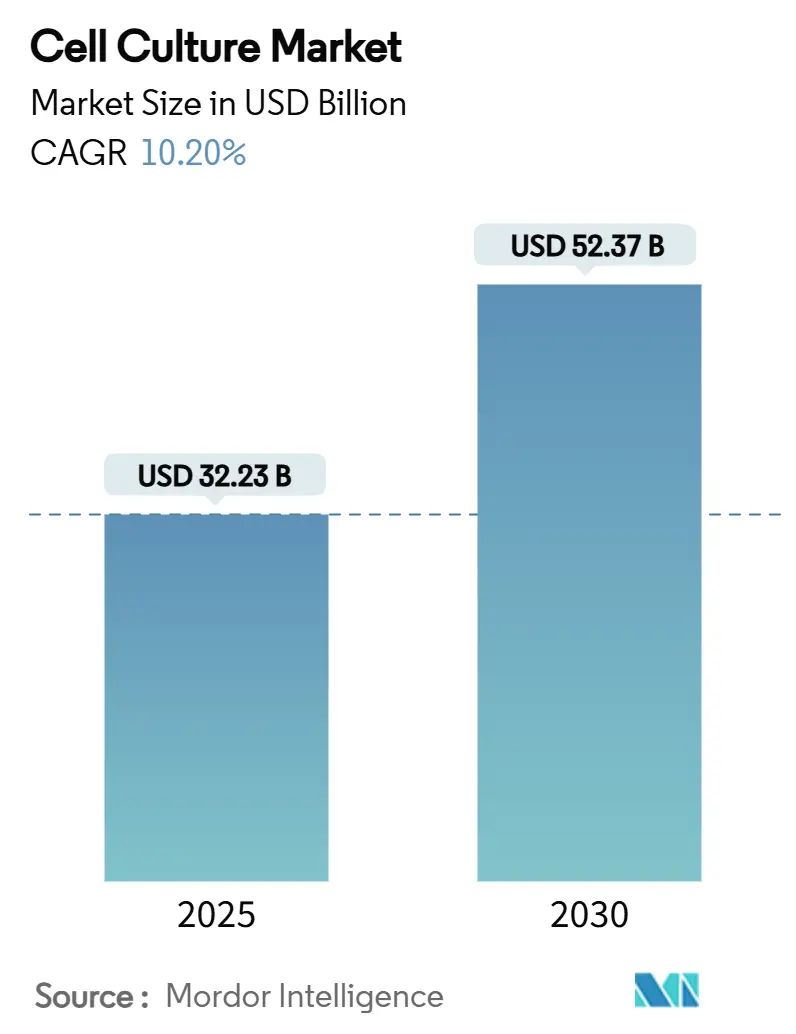
全球细胞培养市场规模在2025年为322.3亿美元,预计到2030年将达到523.7亿美元,在预测期内以10.2%的复合年增长率增长。强劲的生物制造需求、干细胞临床试验激增以及再生医学监管时限收紧,正在重塑细胞培养市场的资本配置。自动化单次使用生物反应器、无血清培养基创新和人工智能辅助工艺分析正在降低每批次成本,同时提高重现性,使开发人员能够扩展曾经在小批量研究环境中停滞不前的疗法。主要生命科学供应商现在寻求垂直整合--结合设备、耗材和合同服务--以加强供应链韧性并缩短技术转移周期。与此同时,日本、中国和美国的区域产业政策加速了设施建设,将生产推向更接近患者的地方,降低跨境物流风险。胎牛血清的供应限制,加上可持续发展要求,继续加速向化学成分明确、无动物成分系统的转型,这些系统简化了监管申报并消除了伦理瓶颈。
关键报告要点
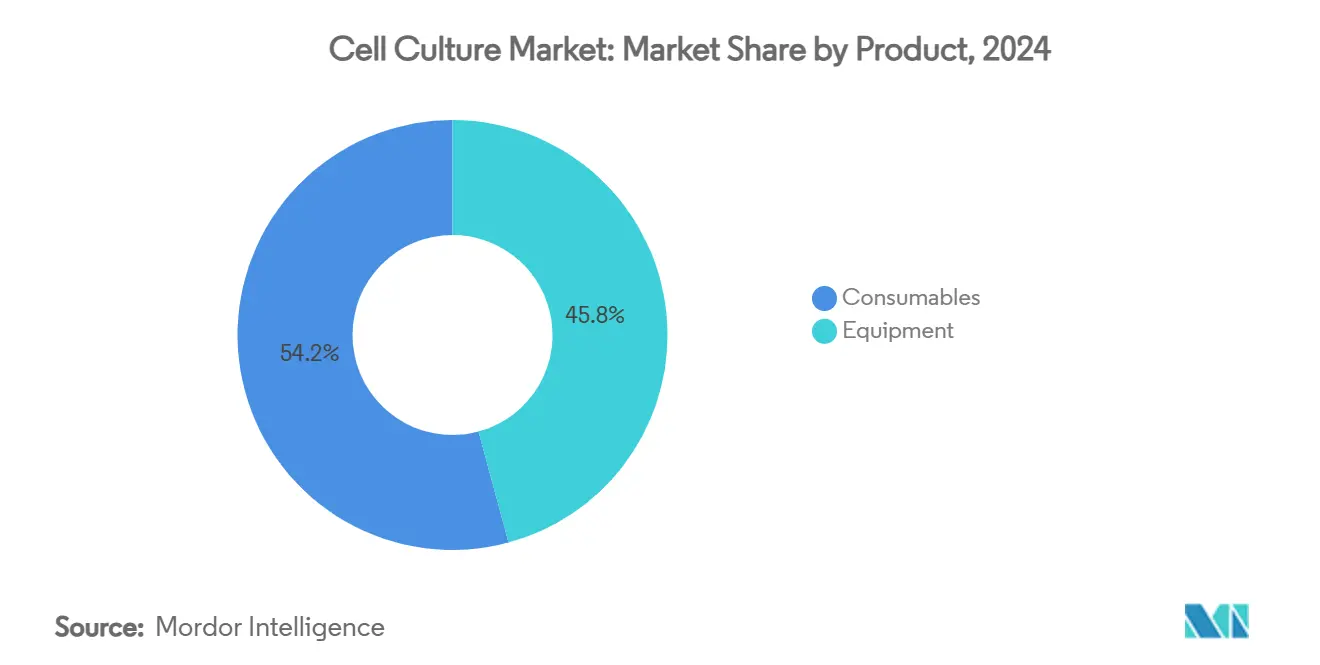
- 按产品类别,耗材在2024年以54.25%的收入份额领先;设备预计以13.65%的复合年增长率增长至2030年。
- 按细胞类型,哺乳动物细胞在2024年占据细胞培养市场份额的62.32%,而干细胞预计在2030年前以11.85%的复合年增长率增长。
- 按技术,2D系统在2024年以75.24%的份额占主导地位;3D培养以13.7%的复合年增长率增长至2030年。
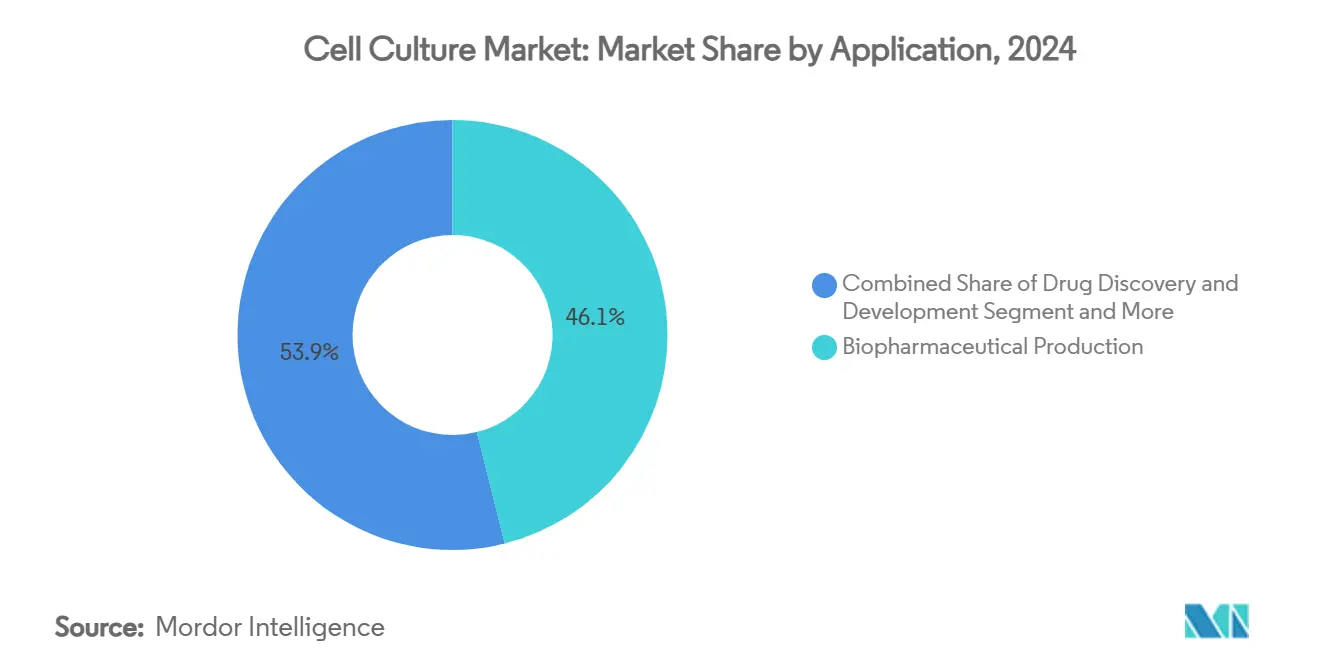
- 按应用,生物制药生产在2024年占细胞培养市场规模的46.12%,基因和细胞治疗制造以15.4%的复合年增长率增长至2030年。
- 按终端用户,制药和生物技术公司在2024年占据48.32%的份额;合同研究和制造组织以12.9%的复合年增长率增长至2030年。
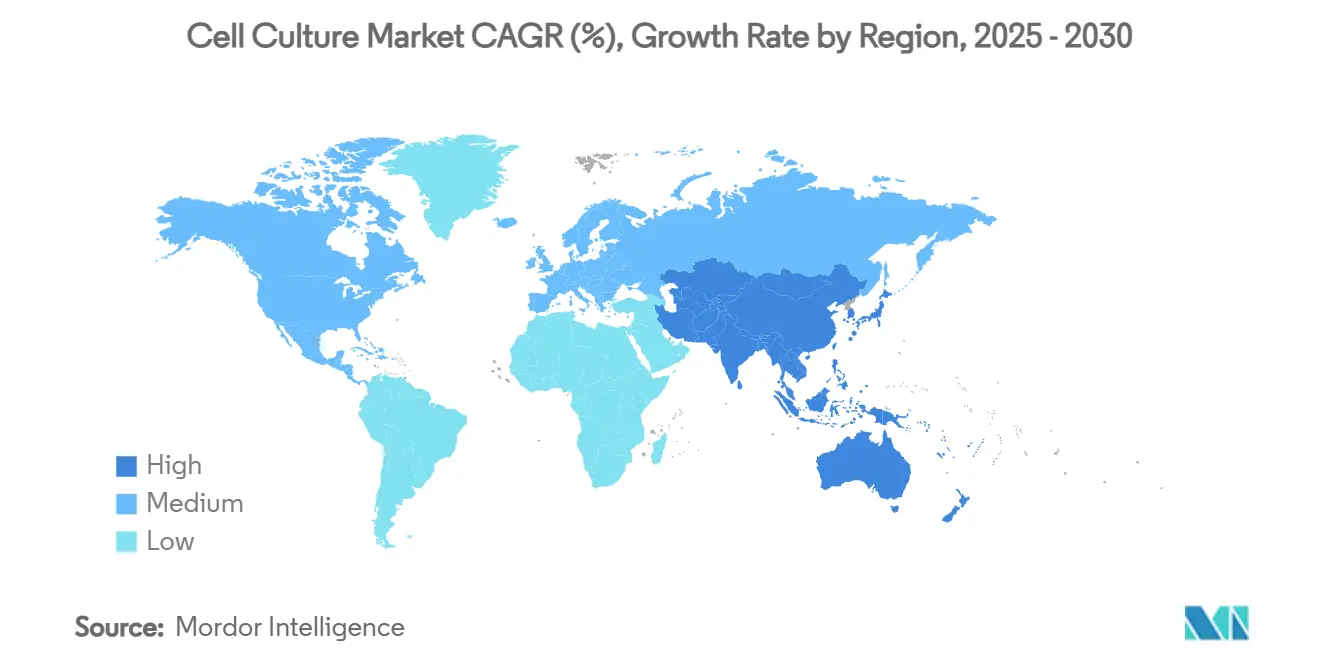
- 按地理位置,北美在2024年占细胞培养市场份额的38.52%;亚太地区预计在2025年至2030年间以12.8%的复合年增长率实现最快增长。
全球细胞培养市场趋势与洞察
驱动因素影响分析
| 驱动因素 | 对复合年增长率预测的影响(约%) | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 慢性病负担增加生物制品需求 | +2.8% | 北美、欧洲、全球溢出 | 中期(2-4年) |
| 自动化高通量系统 | +2.1% | 北美、亚太 | 短期(≤2年) |
| 公私合作资金动力 | +1.9% | 日本、中国、美国 | 长期(≥4年) |
| 基因和细胞治疗试验扩大 | +2.4% | 美国、日本、德国 | 中期(2-4年) |
| 药物发现中的细胞基分析 | +1.2% | 北美、欧盟 | 短期(≤2年) |
| 可持续、无动物生物加工 | +1.6% | 欧盟、北美、全球 | 长期(≥4年) |
| 来源: Mordor Intelligence | |||
慢性病全球负担上升推动生物制品需求
非传染性疾病继续充实生物制品管线,迫使制造商扩展支撑单克隆抗体、疫苗和GLP-1治疗药物的培养产能。赛诺菲承诺投资13亿欧元建设垂直整合的胰岛素设施,突显了大批量慢性病适应症如何直接转化为细胞培养市场扩张。肿瘤学加剧了这一压力;全球有超过60项诱导多能干细胞试验正在进行,其中近三分之一在日本,该国的快速审批缩短了从实验室到临床的路径[1]编辑团队,《日本对干细胞疗法的押注》,nature.com。算式很清楚:随着慢性病患病率规模扩大,细胞培养市场必须提供维持人口生产力的治疗支柱。
自动化和高通量细胞培养系统技术进步
封闭式单次使用生物反应器和AI编排工艺控制的快速采用,降低了污染风险和技术员工时,同时使批次产量翻倍。哥本哈根的一项扩建项目增加了8个2000升单次使用容器,每年可增加150个批次,证明自动化可以在不需要传统砖瓦规模化的情况下实现阶跃式产能提升。液滴微流体进一步压缩细胞株开发时间线,用数分钟的数字选择精度替代数周的手工克隆挑选。这些收益直接流入细胞培养市场损益表,让赞助商能够经济地追求更小的患者亚群。
政府和私人对细胞基础研究资金扩大
日本的7.6亿美元再生医学计划、德国78%的年度资金增幅以及风险投资支持的轮次(如bit bio的3000万美元融资)加强了一个持久的资本周期,降低了科学风险并吸引了私人共同投资[2]德国生物技术协会,《德国融资跳增78%》,biodeutschland.org。这些资金流入为试点工厂、GMP套件和人才发展付费,扩大了未来可触及的细胞培养市场。
全球细胞和基因治疗临床试验管线增长
美国FDA预计从2025年开始每年批准20种新的细胞和基因治疗产品。随着试验量上升,缺乏内部GMP套件的创新者涌向合同制造商,这些制造商已经处理了67.13%的外包先进疗法生产。结果是生物反应器、培养基和分析的持续订单量--细胞培养市场供应商的燃料。
限制因素影响分析
| 限制因素 | 对复合年增长率预测的影响(约%) | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 高资本和运营成本 | -2.3% | 新兴市场、全球 | 长期(≥4年) |
| 多样化监管合规负担 | -1.8% | 北美、欧盟、亚太 | 中期(2-4年) |
| 污染风险和批次失败 | -1.1% | 全球、低基础设施地区 | 短期(≤2年) |
| 关键投入品供应链脆弱性 | -1.4% | 进口依赖地区 | 中期(2-4年) |
| 来源: Mordor Intelligence | |||
大规模cGMP细胞培养设施高资本和运营成本
建造合规生物制品工厂的成本可能达到每平方英尺500-1400美元,这一障碍推动初创公司转向外包模式,并减缓现金有限地区的设施部署。即使是富士胶片和龙沙等资金雄厚的在位者也接受九位数的扩建价格标签,凸显了拖累细胞培养市场准入的财务重力。
各地区严格的监管和质量合规要求
FDA指导方针、不断发展的欧洲附件1规则以及各国对GMP义务的特定解释,需要独立提交、本地化审计,通常还需要冗余验证研究。较小公司必须聘请专业监管团队或面临批准延迟的风险--这一支出压缩了利润率并可能阻止跨境规模化[3]FDA传播办公室,《先进疗法预测》,fda.gov。
细分分析
按产品:耗材推动创新,设备变革运营
耗材在2024年保持了细胞培养市场的最大份额,占54.25%,该细分预计在2030年前以13.65%的复合增长,因为开发人员转向化学成分明确、无动物的培养基配方。这一演进保护运营商免受即将到来的FBS紧缺影响,并与偏好临床档案中可追溯成分的监管机构保持一致。在设备方面,单次使用生物反应器、灌流平台和在线传感器正在重写设施蓝图,减少停机时间和资本密集度。赛默飞世尔41亿美元的过滤收购凸显了纯化硬件如何成为稳健连续加工的战略要素。随着自动化的普及,归因于设备的细胞培养市场规模将比以前的周期上升更快--即使耗材保持更大的收入基础。
研发实验室同样在更新显微镜和成像系统;横河的CQ3000捕获实时3D图像,为下游AI分析提供数据,缩短分析开发时间。一次性管道、过滤器和取样端口完成单次使用生态系统,在每次新生物反应器安装时锁定可预测的耗材需求。这些变化共同巩固了一个反馈循环,设备创新释放新的耗材SKU,反之亦然,丰富了细胞培养市场价值链。
按细胞类型:哺乳动物主导地位面临干细胞创新浪潮
哺乳动物平台在2024年产生了细胞培养市场份额的62.32%,很大程度上因为CHO细胞株仍是单克隆抗体的主力。然而干细胞呈现最快上升,随着全球试验在2024年底达到115项而跟踪11.85%的复合年增长率。日本的监管加速器和公共资金已将诱导多能干细胞疗法拉至商业批准的边缘,标志着对GMP级干细胞培养基、基质和封闭收获系统需求的拐点。
在哺乳动物细胞株内,原代细胞赢得研究相关性,而永生化细胞株提供可靠的生产标题。微生物和昆虫细胞系统解决哺乳动物细胞株无法有效表达的利基蛋白靶点和疫苗抗原,在更广泛的细胞培养市场内保持多样化需求模式。
按技术:2D培养稳定性对比3D创新加速
尽管3D类器官和球体成为会议议程头条,2D平台仍在2024年控制了75.24%的收入,因为cGMP验证的抗体工艺继续在平板或搅拌罐单层上运行。将遗留产品转向3D增加了监管负担,而没有保证的产量收益,缓解了大规模迁移的步伐。然而,3D将以13.7%的复合年增长率获得增量预算,特别是在生理相关性超过纯生产力的发现工作流程中。
患者来源肿瘤类器官支持绕过动物试验的精准肿瘤学筛选,无支架球体试剂盒降低了高通量实验室的设置复杂性。生物打印与3D培养合并组装组织构建体,将细胞培养市场扩展至寻求结构复杂植入物的再生医学参与者。
按应用:生物制药生产锚定增长,基因治疗加速
生物制药制造在2024年保持了细胞培养市场规模的46.12%,这是大量商业抗体体积和季节性疫苗运行的函数。增量收入现在来自将遗留抗体放入强化灌流培养系统,从固定罐区域挤出更多克/升。与此同时,基因和细胞治疗制造以15.4%的复合年增长率加速,因为病毒载体和自体细胞批次计数与临床试验开始同步激增。
药物发现实验室采用3D分析来降低候选物选择风险,疫苗专家建造处理重组蛋白以及mRNA平台的双模式工厂,创造设备标准化顺风。组织工程和诊断学完善了利基需求口袋,使细胞培养市场多样化,超越治疗蛋白巨头。
备注: 购买报告后可获得所有单个细分的细分份额
按终端用户:制药主导面临CDMO加速
制药和生物技术公司吸收了2024年48.32%的营业额,但许多公司缩减内部GMP足迹,转而外包。净效应是合同研究和制造组织在2030年前12.9%的复合年增长率,迫使CDMO确保耗材供应和增值分析,以降低客户技术转移风险。医院和诊断实验室为无菌检测驱动较小但持续的体积,而学术中心维持上游发现管线,为未来商业需求提供营养。总的来说,这个多利益相关者生态系统在整体细胞培养市场内维持对高体积工业耗材和专业研究试剂的订单。
地理分析
北美在2024年占全球收入的38.52%,受到默克10亿美元Gardasil成分设施和阿斯利康在马里兰州3亿美元细胞治疗工厂等里程碑式扩建的支持。美国监管环境预测从2025年开始每年20项先进疗法批准,保证了新增GMP套件的利用率。加拿大通过吸引CDMO的税收抵免支撑该地区,墨西哥提供支持大陆供应链的灌装完成和组件成型能力。联邦到2040年用可持续生物制造满足30%美国化学需求的雄心为细胞培养市场提供了持久的政策顺风。
欧洲呈现强劲的追赶势头。德国生物技术融资在2024年飙升至19亿欧元,英国公布了4.5亿英镑疫苗中心以对冲疫情风险。欧盟协调GMP附件更新的努力简化了跨境产品发布并有利于泛欧服务网络。此外,拜耳在柏林的基因和细胞治疗中心等合作将工业合作伙伴拉入公共科学生态系统。
亚太地区记录最快攀升,时钟12.8%的复合年增长率。日本的7.6亿美元再生医学计划催生了超过60项iPSC试验,并为明确培养基、封闭生物反应器和下游纯化撬装的国内需求提供底色。中国既扩大上游抗体工厂又新兴mRNA生产线,而印度通过成本优势获得合同配方和分析。韩国和澳大利亚分别通过先进干细胞制造和支持性报销制度完善地区马赛克。总的来说,亚太地区的人口特征--老龄化人口和慢性病发病率增长--巩固了细胞培养市场延伸至预测期之外的需求跑道。
竞争格局
行业结构融合了集中的设备领导地位和专业创新者的长尾。赛默飞世尔的过滤收购,加上宣布的400-500亿美元并购战争基金,凸显了对端到端能力堆栈的争夺。丹纳赫、萨托流思和默克同样将耗材嵌入分析套件,创建锁定生态系统,提高客户转换成本。同时,风险投资支持的颠覆者将AI驱动的克隆性平台、高通量类器官库和无血清利基培养基商业化,蚕食传统在位者。
战略合作,而非价格战,推动份额转移:许可协议占2023年交易流的19%,让各方在没有完整收购溢价的情况下利用互补知识产权。最激烈争夺的白地围绕可持续原材料、硅片工艺控制和为主权生物技术议程量身定制的区域CDMO足迹。因此,细胞培养市场保持动态,奖励将资本规模与敏捷创新路线图相结合的参与者。
细胞培养行业领导者
赛默飞世尔科技
丹纳赫公司
萨托流思股份公司
默克集团
贝克顿迪金森公司
- *免责声明:主要玩家排序不分先后
近期行业发展
- 2025年3月:默克确认在其北卡罗来纳州达勒姆工厂投资10亿美元扩建,为Gardasil疫苗生产活性成分,增加225,000平方英尺的GMP空间。
- 2025年2月:赛默飞世尔完成41亿美元收购Solventum的纯化和过滤部门,以加强上游和下游细胞培养工作流程。
全球细胞培养市场报告范围
根据报告范围,细胞培养是在其自然环境外的特定受控条件下培养细胞的过程。一旦从活体组织中分离出感兴趣的细胞,就可以在精心控制的条件下维持它们。细胞培养市场按产品和耗材(产品(生物安全设备、离心机、低温储存设备、培养系统/生物反应器、培养箱、移液仪器和其他)和耗材(培养基、血清和试剂))、应用(生物制药、药物开发、基因治疗、组织培养和工程、疫苗生产和其他)和地理位置(北美、欧洲、亚太、中东和非洲以及南美)进行细分。市场报告还涵盖全球主要地区17个不同国家的估计市场规模和趋势。报告为上述细分提供价值(百万美元)。
| 设备 | 生物安全柜 |
| 离心机 | |
| 低温储存设备 | |
| 培养系统/生物反应器 | |
| 培养箱 | |
| 移液仪器 | |
| 显微镜和成像系统 | |
| 细胞计数器和分析仪 | |
| 过滤系统 | |
| 附件(管道、连接器、配件) | |
| 耗材 | 培养基 |
| 无血清培养基 | |
| 血清(FBS和替代品) | |
| 试剂 | |
| 缓冲液和盐类 | |
| 补充剂和生长因子 | |
| 冷冻保护剂 | |
| 塑料器皿(瓶、板、皿) |
| 哺乳动物细胞 | 原代细胞 |
| 连续细胞株 | |
| 干细胞 | 胚胎干细胞 |
| 成体干细胞 | |
| 诱导多能干细胞 | |
| 微生物细胞 | 细菌 |
| 酵母和真菌 | |
| 昆虫细胞 |
| 2D细胞培养 | |
| 3D细胞培养 | 基于支架 |
| 无支架 |
| 生物制药生产 |
| 药物发现与开发 |
| 基因和细胞治疗制造 |
| 疫苗生产 |
| 组织工程和再生医学 |
| 癌症研究 |
| 诊断和分析开发 |
| 毒性检测和安全评估 |
| 制药和生物技术公司 |
| 学术和研究机构 |
| CRO和CDMO |
| 医院和诊断实验室 |
| 细胞库和生物库 |
| 北美 | 美国 |
| 加拿大 | |
| 墨西哥 | |
| 欧洲 | 德国 |
| 英国 | |
| 法国 | |
| 意大利 | |
| 西班牙 | |
| 欧洲其他地区 | |
| 亚太地区 | 中国 |
| 日本 | |
| 印度 | |
| 韩国 | |
| 澳大利亚 | |
| 亚太其他地区 | |
| 中东和非洲 | 海湾合作委员会 |
| 南非 | |
| 中东和非洲其他地区 | |
| 南美 | 巴西 |
| 阿根廷 | |
| 南美其他地区 |
| 按产品 | 设备 | 生物安全柜 |
| 离心机 | ||
| 低温储存设备 | ||
| 培养系统/生物反应器 | ||
| 培养箱 | ||
| 移液仪器 | ||
| 显微镜和成像系统 | ||
| 细胞计数器和分析仪 | ||
| 过滤系统 | ||
| 附件(管道、连接器、配件) | ||
| 耗材 | 培养基 | |
| 无血清培养基 | ||
| 血清(FBS和替代品) | ||
| 试剂 | ||
| 缓冲液和盐类 | ||
| 补充剂和生长因子 | ||
| 冷冻保护剂 | ||
| 塑料器皿(瓶、板、皿) | ||
| 按细胞类型 | 哺乳动物细胞 | 原代细胞 |
| 连续细胞株 | ||
| 干细胞 | 胚胎干细胞 | |
| 成体干细胞 | ||
| 诱导多能干细胞 | ||
| 微生物细胞 | 细菌 | |
| 酵母和真菌 | ||
| 昆虫细胞 | ||
| 按技术 | 2D细胞培养 | |
| 3D细胞培养 | 基于支架 | |
| 无支架 | ||
| 按应用 | 生物制药生产 | |
| 药物发现与开发 | ||
| 基因和细胞治疗制造 | ||
| 疫苗生产 | ||
| 组织工程和再生医学 | ||
| 癌症研究 | ||
| 诊断和分析开发 | ||
| 毒性检测和安全评估 | ||
| 按终端用户 | 制药和生物技术公司 | |
| 学术和研究机构 | ||
| CRO和CDMO | ||
| 医院和诊断实验室 | ||
| 细胞库和生物库 | ||
| 地理位置 | 北美 | 美国 |
| 加拿大 | ||
| 墨西哥 | ||
| 欧洲 | 德国 | |
| 英国 | ||
| 法国 | ||
| 意大利 | ||
| 西班牙 | ||
| 欧洲其他地区 | ||
| 亚太地区 | 中国 | |
| 日本 | ||
| 印度 | ||
| 韩国 | ||
| 澳大利亚 | ||
| 亚太其他地区 | ||
| 中东和非洲 | 海湾合作委员会 | |
| 南非 | ||
| 中东和非洲其他地区 | ||
| 南美 | 巴西 | |
| 阿根廷 | ||
| 南美其他地区 | ||
报告中回答的关键问题
2025年细胞培养市场有多大?
细胞培养市场规模在2025年为322.3亿美元,预计到2030年增长至523.7亿美元。
哪个细分领导细胞培养耗材需求?
培养基和试剂主导耗材,由于血清短缺推动向化学成分明确、无动物配方的转换。
是什么推动干细胞培养的快速增长?
监管快速通道、超过115项活跃临床试验以及日本的资金推动使干细胞成为增长最快的细胞类型,复合年增长率为11.85%。
为什么CDMO获得细胞培养收入份额?
高设施资本支出和复杂GMP要求推动制药公司外包,推动CDMO以12.9%的复合年增长率增长。
哪个地区扩张最快?
亚太地区以12.8%的复合年增长率增长,由日本的大型公共投资以及中国和印度加速基础设施推动。
页面最后更新于:



