Tamanho e Participação do Mercado de Kits de Teste Diagnóstico para Parto Prematuro
Análise do Mercado de Kits de Teste Diagnóstico para Parto Prematuro por Mordor Intelligence
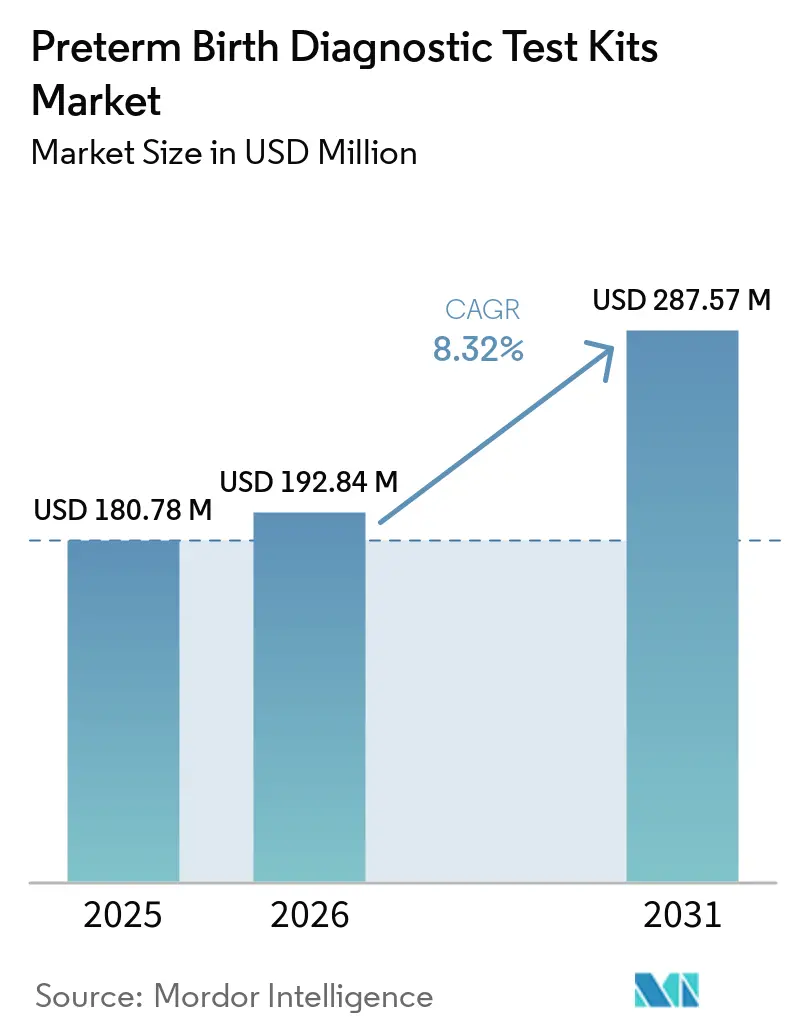
O tamanho do Mercado de Kits de Teste Diagnóstico para Parto Prematuro está projetado em USD 180,78 milhões em 2025, USD 192,84 milhões em 2026, e deve atingir USD 287,57 milhões até 2031, crescendo a um CAGR de 8,32% de 2026 a 2031.
O crescimento reflete uma mudança da triagem sintomática para uma estratificação de risco mais precoce, à medida que as equipes clínicas combinam testes de biomarcadores com ultrassonografia do comprimento cervical para reduzir internações e intervenções evitáveis. A descontinuação dos cassetes quantitativos de fibronectina fetal perturbou as rotinas hospitalares estabelecidas e redirecionou as aquisições para biomarcadores alternativos e plataformas binárias de exclusão diagnóstica. Os testes baseados em swab de PAMG-1 e IGFBP-1, juntamente com os diagnósticos de ruptura de membranas ovulares, continuam a fundamentar decisões rápidas nas unidades de trabalho de parto, onde os minutos são determinantes para a alta ou transferência. As evidências de 2026 reforçaram o valor do rastreamento proteômico baseado em sangue, com um grande estudo randomizado demonstrando melhores desfechos quando uma estratégia de prevenção baseada no PreTRM foi aplicada em gestações de baixo risco. A dinâmica regional favorece a escala e o engajamento dos pagadores, com a América do Norte mantendo a liderança em participação de mercado, enquanto a Ásia-Pacífico se expande mais rapidamente por meio da construção de laboratórios e projetos-piloto de reembolso.
Principais Conclusões do Relatório
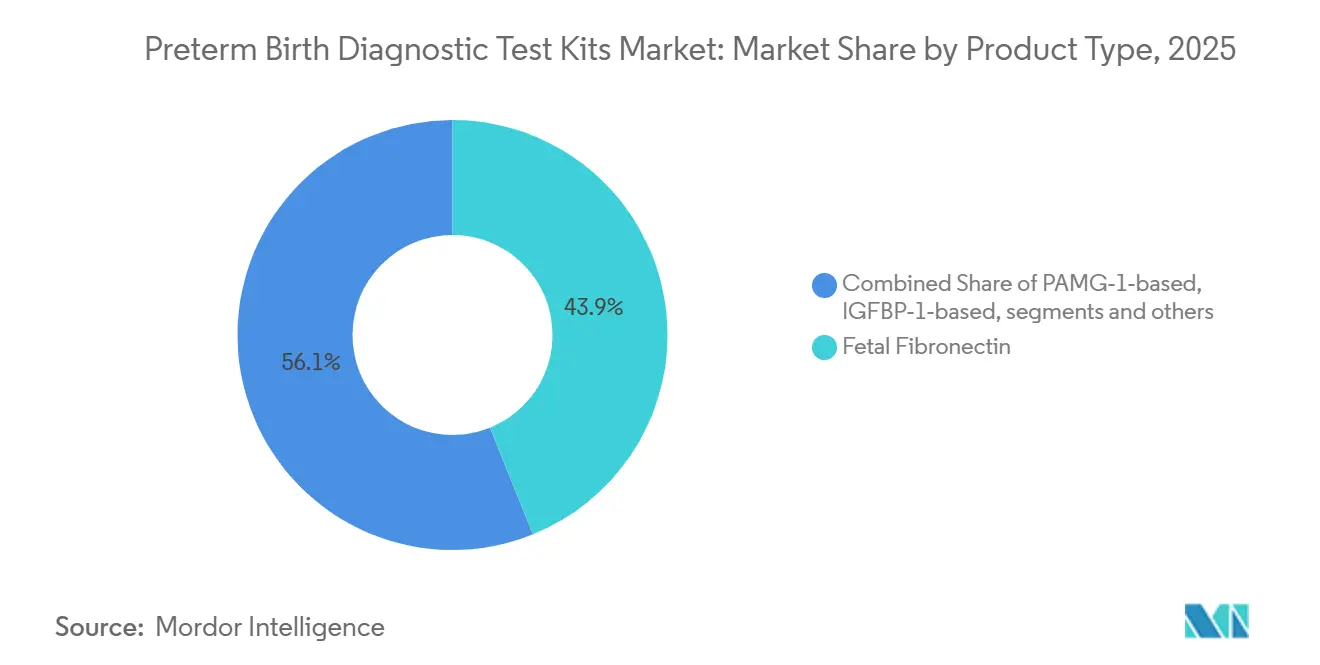
- Por tipo de produto, a fibronectina fetal liderou com 43,89% de participação na receita em 2025, enquanto as plataformas de PAMG-1 estão projetadas para registrar o crescimento mais rápido, com um CAGR de 9,67% até 2031.
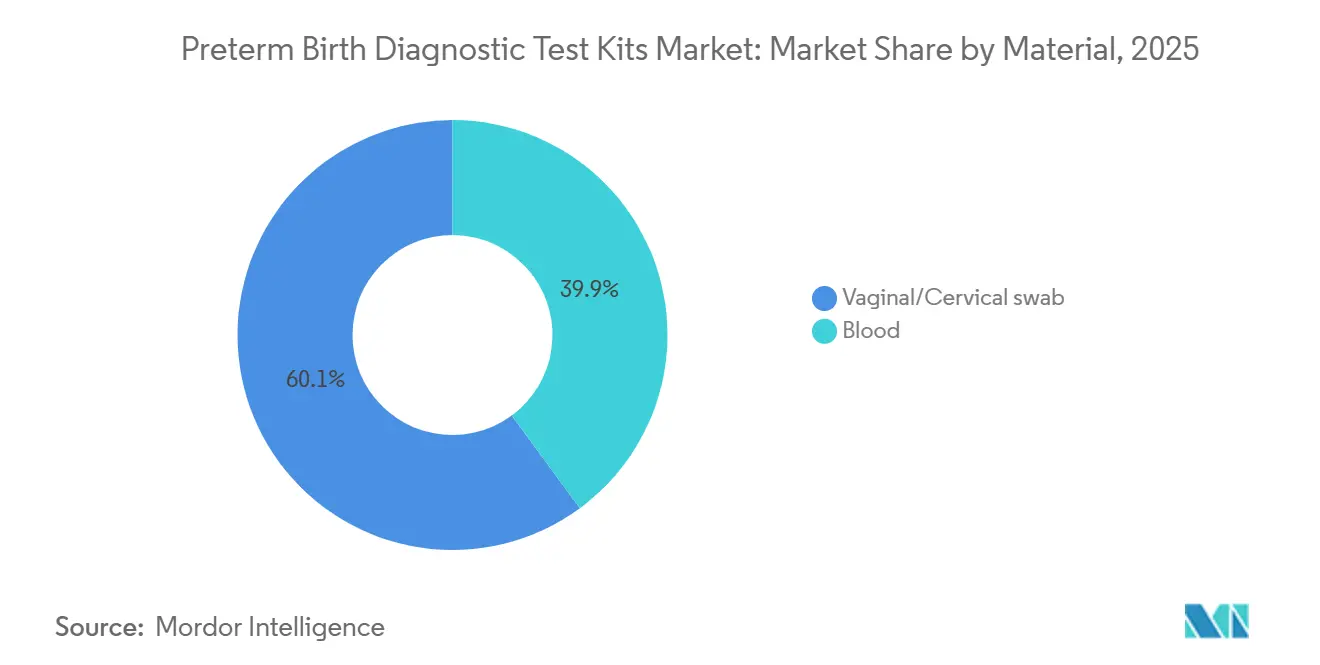
- Por material, os swabs vaginais-cervicais representaram 60,10% da receita de 2025 e os ensaios proteômicos baseados em sangue estão avançando a um CAGR de 9,01% até 2031.
- Por usuário final, hospitais e centros de maternidade detiveram 58,56% da demanda de 2025 e os laboratórios de diagnóstico registraram o maior crescimento projetado, com um CAGR de 10,34%.
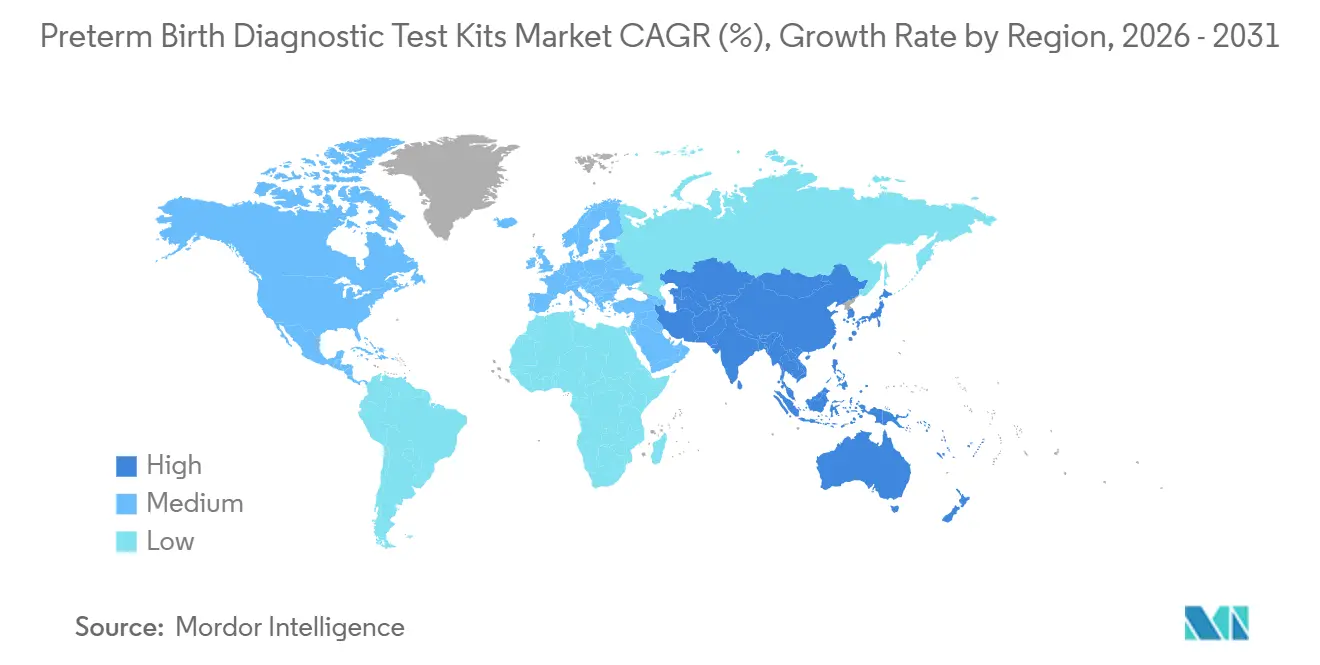
- Por região, a América do Norte contribuiu com 43,64% da receita de 2025 e a Ásia-Pacífico está projetada para crescer a um CAGR de 9,45% até 2031.
Nota: O tamanho do mercado e os números de previsão neste relatório são gerados usando a estrutura de estimativa proprietária da Mordor Intelligence, atualizada com os dados e percepções mais recentes disponíveis em janeiro de 2026.
Tendências e Perspectivas do Mercado Global de Kits de Teste Diagnóstico para Parto Prematuro
Análise de Impacto dos Impulsionadores
| Impulsionador | (~) % de Impacto na Previsão de CAGR | Relevância Geográfica | Horizonte Temporal de Impacto |
|---|---|---|---|
| Crescente incidência global e carga de partos prematuros | +2.3% | Global, com pressão aguda na África Subsaariana e no Sul da Ásia | Longo prazo (≥ 4 anos) |
| Integração da triagem baseada em biomarcadores nas vias clínicas (fFN, PAMG-1, IGFBP-1) | +2.8% | América do Norte e UE como núcleo, com expansão para centros urbanos da Ásia-Pacífico | Médio prazo (2-4 anos) |
| Kits de fluxo lateral de ponto de atendimento rápidos que permitem decisões rápidas de exclusão diagnóstica na triagem de maternidade | +1.6% | América do Norte, Europa Ocidental, Austrália | Curto prazo (≤ 2 anos) |
| Suporte de protocolo hospitalar e reembolso para testes direcionados em casos de alto risco/sintomáticos | +1.1% | Nacional, com ganhos iniciais nos planos comerciais e Medicaid dos EUA e nos sistemas públicos europeus | Médio prazo (2-4 anos) |
| Expansão de testes de risco proteômico baseados em sangue que informam vias de cuidado mais precoces | +0.9% | Foco nos EUA, programas-piloto em mercados europeus selecionados | Longo prazo (≥ 4 anos) |
| Ferramentas de decisão digital combinando biomarcadores quantitativos com comprimento cervical | +0.5% | Núcleo da Ásia-Pacífico (China, Índia, Coreia do Sul), emergindo na América Latina | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Crescente Incidência Global e Carga de Partos Prematuros
O parto prematuro continua sendo uma das principais causas de morbidade e mortalidade neonatal em todo o mundo, o que sustenta a demanda clínica por avaliação de risco mais precoce e precisa. Os hospitais buscam padronizar a triagem para limitar transferências desnecessárias e apoiar o uso oportuno de corticosteroides somente quando o risco é credível e próximo ao termo. A carga persistente em ambientes de baixos recursos expõe uma lacuna entre a necessidade e o acesso, o que sustenta o uso de testes mais simples e atrasa a adoção de ensaios avançados de biomarcadores. Os sistemas de saúde avaliam o valor operacional de testes que podem rapidamente excluir o parto iminente, prevenindo internações hospitalares evitáveis e reduzindo a pressão sobre as unidades terciárias. Essas dinâmicas mantêm o mercado de kits de teste diagnóstico para parto prematuro focado na velocidade e clareza do resultado para fortalecer as decisões na linha de frente.
Integração da Triagem Baseada em Biomarcadores nas Vias Clínicas (fFN, PAMG-1, IGFBP-1)
Muitas instituições na América do Norte e na Europa integraram a triagem baseada em biomarcadores em protocolos padronizados para pacientes com sintomas entre 24 e 34 semanas, reduzindo internações injustificadas quando um resultado negativo claro é obtido. A descontinuação dos cassetes quantitativos de fibronectina fetal levou as diretrizes nacionais em 2024 a fazer a transição para plataformas alternativas, o que reformulou as aquisições e incentivou uma avaliação mais ampla das opções de IGFBP-1 e PAMG-1[1]NHS England, "Descontinuação do teste de fibronectina fetal Hologic", NHS England, england.nhs.uk. O papel dos diagnósticos de ruptura de membranas ovulares persiste como parte da via de cuidado, uma vez que o estado das membranas influencia diretamente o risco de trabalho de parto próximo ao termo e as escolhas de vigilância clínica. A triagem orientada por protocolo limita a variação entre os clínicos e direciona os recursos para casos com risco mensurável, em vez de observação preventiva. As diretrizes profissionais e os comitês institucionais continuam a moldar a adoção, ancorando o mercado de kits de teste diagnóstico para parto prematuro a testes que fornecem clareza binária ou quase binária em minutos.
Kits de Fluxo Lateral de Ponto de Atendimento Rápidos que Permitem Decisões Rápidas de Exclusão Diagnóstica na Triagem de Maternidade
Os imunoensaios de ponto de atendimento fornecem resultados durante o mesmo atendimento, o que permite às equipes dar alta com confiança após um teste negativo ou escalar o cuidado quando um resultado positivo sinaliza risco próximo ao termo. O tempo até o resultado impulsiona o valor operacional, pois as unidades de emergência frequentemente precisam decidir sobre transferência ou momento de administração de esteroides em janelas de tempo curtas. Formatos estáveis em temperatura ambiente e fluxos de trabalho simples tornam os kits de fluxo lateral uma ferramenta prática para unidades de trabalho de parto movimentadas e para centros menores que buscam prática consistente. Onde o teste de ruptura de membranas ovulares é relevante, as opções de fluxo lateral apoiam a confirmação rápida do estado das membranas e reduzem a dependência de métodos legados menos precisos. As políticas dos pagadores e os formulários locais ainda influenciam quais kits são usados rotineiramente, razão pela qual os protocolos e os padrões de aquisição permanecem centrais para ampliar o acesso. O mercado de kits de teste diagnóstico para parto prematuro se beneficia quando os menus de testes se integram a fluxos de trabalho de ponto de atendimento que resolvem as decisões de triagem em minutos.
Suporte de Protocolo Hospitalar e Reembolso para Testes Direcionados em Casos de Alto Risco/Sintomáticos
A cobertura e os protocolos internos juntos determinam com que consistência os testes são usados nos cuidados obstétricos de primeira linha. Quando os comitês hospitalares codificam as escadas de testes para mulheres sintomáticas, a variação clínica diminui e os desfechos se tornam mais fáceis de gerenciar e medir. No Reino Unido, as diretrizes nacionais após a descontinuação do fFN ilustraram como os sistemas públicos podem orientar a seleção de produtos e estabilizar a prática em diferentes unidades. Nos Estados Unidos, os modelos de laboratório centralizado para testes proteômicos baseados em sangue operam sob a supervisão do CLIA e do CAP, o que permite qualidade consistente em escala à medida que os pagadores revisam os dados de desfechos para cobertura ampla. As empresas relataram engajamento com pagadores e discussões ativas sobre reembolso para estratégias de prevenção informadas por resultados de risco proteômico, o que reflete um impulso em direção a arranjos baseados em valor. Esses padrões reforçam o foco do mercado de kits de teste diagnóstico para parto prematuro em testes vinculados a ações clínicas claras e compensações de custos mensuráveis.
Análise de Impacto das Restrições
| Restrição | (~) % de Impacto na Previsão de CAGR | Relevância Geográfica | Horizonte Temporal de Impacto |
|---|---|---|---|
| Endossos de diretrizes mistos/condicionais para alguns biomarcadores e usos | -0.7% | Global, variabilidade mais alta no Oriente Médio e na América Latina | Médio prazo (2-4 anos) |
| VPP modesto/falsos positivos que necessitam de avaliação confirmatória | -0.4% | Global, carga operacional concentrada em ambientes de baixos recursos | Curto prazo (≤ 2 anos) |
| Restrições operacionais de coleta de amostras (tempo, co-interferência) limitam a implantação universal | -0.3% | África Subsaariana, Sul da Ásia rural, Austrália remota | Médio prazo (2-4 anos) |
| O IVDR da UE eleva as evidências clínicas, os custos e o tempo de entrada no mercado para dispositivos de diagnóstico in vitro | -0.8% | UE27, com expansão para países que reconhecem a marca CE | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Endossos de Diretrizes Mistos/Condicionais para Alguns Biomarcadores e Usos
A variabilidade das diretrizes entre as regiões retarda a adoção padronizada e sustenta um conjunto fragmentado de práticas de teste dentro e entre os países. Os documentos profissionais frequentemente fazem referência a classes de biomarcadores em vez de marcas específicas, o que deixa as equipes de aquisição a decidir com base em preço, disponibilidade e familiaridade local. O endosso inconsistente para casos de uso como o rastreamento assintomático contribui para uma adoção desigual fora dos centros terciários. Os clínicos também enfrentam regras divergentes dos pagadores sobre quais testes são reembolsados em cenários específicos, o que adiciona fricção ao pedido rotineiro. Esses fatores moderam o ritmo em que o mercado de kits de teste diagnóstico para parto prematuro pode passar do uso piloto para uma implantação estável e orientada por protocolo.
O IVDR da UE Eleva as Evidências Clínicas, os Custos e o Tempo de Entrada no Mercado para Dispositivos de Diagnóstico In Vitro
Os requisitos regulatórios europeus expandiram as obrigações de evidências e pós-comercialização, o que aumenta o custo e a complexidade de trazer diagnósticos obstétricos ao mercado. A capacidade dos organismos notificados e as exigências de documentação prolongam os prazos para atualizações e novas reivindicações, o que pode atrasar as transições do uso piloto para a ampla disponibilidade. As empresas com sistemas de qualidade maduros e submissões anteriores tendem a navegar nas revisões de forma mais previsível, enquanto os novos entrantes enfrentam necessidades de recursos mais elevadas. O resultado é um padrão mais alto para dados de desempenho e vigilância contínua que pode consolidar a participação com os incumbentes ao longo do tempo. Esse ambiente incentiva os fornecedores a priorizar reivindicações de testes que se alinhem estreitamente com a utilidade clínica e o valor para os pagadores, de modo que os investimentos em conformidade se traduzam em tração de adoção.
Análise de Segmentos
Por Tipo de Produto: A Proteômica Sanguínea Reduz a Lacuna na Triagem
A fibronectina fetal representou 43,89% de participação no tamanho do mercado de kits de teste diagnóstico para parto prematuro em 2025, refletindo o enraizamento histórico antes de uma mudança no fornecimento alterar o comportamento de pedidos. A descontinuação dos cassetes quantitativos de fFN em 2024 substituiu o padrão quantitativo por biomarcadores qualitativos e alternativos em muitas vias hospitalares. As plataformas de PAMG-1 estão projetadas para crescer a um CAGR de 9,67% até 2031, à medida que os hospitais adotam formatos binários de exclusão diagnóstica que simplificam as decisões de triagem para mulheres sintomáticas. Os diagnósticos de ruptura de membranas ovulares permanecem um pilar complementar na via, pois a confirmação do estado das membranas influencia substancialmente o gerenciamento de risco próximo ao termo. O mercado de kits de teste diagnóstico para parto prematuro também está redefinindo o momento, pois os testes proteômicos de sangue, liderados pelo PreTRM, focam no risco entre 18 e 20 semanas com uma estratégia de prevenção baseada em progesterona, aspirina e navegação de cuidados intensificada[2]Sera Prognostics, "A Ciência por Trás do Teste PreTRM", PreTRM, pretrm.com. As evidências randomizadas relatadas em 2026 mostraram uma redução nos partos prematuros muito precoces e menos complicações neonatais quando o rastreamento com PreTRM foi combinado com intervenções direcionadas. Essas mudanças deslocam o centro de gravidade para montante, da gestão de crises entre 24 e 34 semanas para uma estratificação de risco mais precoce que pode evitar episódios de alto custo. Os hospitais ainda valorizam o valor preditivo negativo acionável para evitar transferências, enquanto os laboratórios enfatizam fluxos de trabalho centralizados para ensaios complexos. Juntas, essas dinâmicas de produto sustentam um mercado em duas velocidades, no qual os kits de swab rápidos apoiam a triagem aguda e a proteômica sanguínea se expande para os cuidados preventivos.
O mix de produtos reflete compensações operacionais claras que moldam as preferências dos compradores. Os swabs de ponto de atendimento que retornam resultados em minutos se encaixam nas unidades de emergência e observação que precisam de clareza imediata para decisões de exclusão diagnóstica. As opções de PAMG-1 e IGFBP-1 competem em preço, disponibilidade e familiaridade com as diretrizes locais, à medida que as equipes de aquisição buscam fornecimento confiável após as interrupções do fFN. Os ensaios proteômicos baseados em sangue requerem processamento centralizado, mas abrem uma nova possibilidade de prevenção que visa os muitos partos prematuros espontâneos que carecem de fatores de risco tradicionais. O mercado de kits de teste diagnóstico para parto prematuro, portanto, alinha os produtos ao momento clínico, com a triagem sintomática ancorada por kits de fluxo lateral e o risco assintomático abordado por testes proteômicos que influenciam os planos de cuidado semanas antes do aparecimento dos sintomas. Esse posicionamento complementar ajuda os fornecedores a se defenderem da concorrência baseada apenas em preço, vinculando os testes a desfechos e impacto orçamentário.
Nota: As participações de segmento de todos os segmentos individuais estão disponíveis mediante a compra do relatório
Por Material: Swabs Vaginais Ancoram o Volume, Ensaios Sanguíneos Capturam Valor
Os testes de swab vaginal-cervical representaram 60,10% da participação do mercado de kits de teste diagnóstico para parto prematuro em 2025, refletindo os fluxos de trabalho hospitalares estabelecidos e a velocidade do resultado que esses formatos proporcionam. A coleta por swab se alinha a protocolos que priorizam o conforto do paciente e o suporte imediato à decisão para casos sintomáticos. As realidades operacionais, como o momento da coleta da amostra e a potencial interferência, ainda requerem disciplina, o que ressalta a importância de vias de triagem padronizadas. As plataformas baseadas em sangue estão projetadas para se expandir a um CAGR de 9,01% até 2031, à medida que os laboratórios centralizados usam processamento em lote e controles de qualidade para ampliar o acesso para janelas de rastreamento preventivo. A Sera Prognostics destacou a logística de sangue total em temperatura ambiente e as operações centralizadas do CLIA como principais habilitadores de testes proteômicos consistentes em escala nacional. Pesquisas independentes também relataram painéis promissores de proteínas plasmáticas do segundo trimestre para a predição do parto prematuro espontâneo, o que sinaliza maior potencial para a inovação em testes sanguíneos. Essas diferenças de material se mapeiam para momentos de cuidado distintos e criam um caminho equilibrado para o crescimento em ambientes agudos e preventivos.
A escolha do material também afeta o rendimento e o fluxo de dados para as equipes de cuidado. Os swabs de fluxo lateral fornecem resultados de ponto de atendimento e apoiam decisões de alta em tempo real nas salas de emergência e nas unidades de triagem de trabalho de parto. A proteômica sanguínea favorece as consultas pré-natais programadas e a interpretação centralizada que retorna o risco individualizado em dias, em vez de minutos. À medida que os sistemas de saúde combinam biomarcadores com ultrassonografia do comprimento cervical, ambos os materiais contribuem para algoritmos mais claros de inclusão e exclusão diagnóstica que otimizam o uso de recursos. O mercado de kits de teste diagnóstico para parto prematuro, portanto, acomoda um papel duradouro para os swabs, enquanto expande o valor dos testes sanguíneos para o planejamento de intervenção mais precoce.
Por Usuário Final: Laboratórios Superam Hospitais em Fluxos de Trabalho de Alta Complexidade
Hospitais e centros de maternidade representaram 58,56% da participação do mercado de kits de teste diagnóstico para parto prematuro em 2025, impulsionados pelo uso consistente de swabs de ponto de atendimento em ambientes de triagem onde a velocidade é central. Os resultados negativos apoiam a alta no mesmo dia e limitam as internações de observação que não são clinicamente necessárias. Os laboratórios de diagnóstico registraram um CAGR de 10,34% até 2031 ao absorver painéis de envio externo e proteômica sanguínea que requerem fluxos de trabalho centralizados e instrumentos especializados. A Sera Prognostics opera um único laboratório certificado pelo CLIA e credenciado pelo CAP para processar todas as amostras do PreTRM nacionalmente, o que permite uma supervisão rigorosa do desempenho em escala. Essa divisão de trabalho se alinha à forma como o cuidado é prestado, com os hospitais priorizando a imediatidade e os laboratórios avançando na prevenção e no gerenciamento de riscos.
O impulso está crescendo para modelos integrados que unificam as decisões de ponto de atendimento com a análise centralizada. Os hospitais mantêm um papel forte na triagem sintomática, enquanto os laboratórios expandem a pegada de rastreamento a montante com avaliações proteômicas que podem desencadear intervenções direcionadas. Os pagadores que avaliam dados de desfechos podem incentivar modelos que combinam testes de triagem imediata com estratégias preventivas que reduzem os dias de UTI neonatal e os custos. O mercado de kits de teste diagnóstico para parto prematuro, portanto, reflete os pontos fortes dos usuários finais tanto na imediatidade quanto nos benefícios de cuidado longitudinal.
Análise Geográfica
A América do Norte deteve 43,64% da receita de 2025 e ancora o mercado de kits de teste diagnóstico para parto prematuro com protocolos que incorporam o uso de biomarcadores nas unidades de trabalho de parto e parto. A descontinuação do fFN quantitativo em 2024 impulsionou transições aceleradas para biomarcadores alternativos e reforçou o peso das diretrizes nacionais na formação da prática. O Canadá e o México ficam atrás da adoção dos EUA, pois as regras de aquisição e cobertura variam entre as províncias e os mix de pagadores. O crescimento dos EUA agora inclui projetos-piloto de rastreamento assintomático sob planos comerciais e Medicaid, o que impulsiona a adoção além da triagem de crise em direção à prevenção. O mercado de kits de teste diagnóstico para parto prematuro na América do Norte continua a equilibrar o uso rápido de swabs com fluxos de trabalho proteômicos emergentes que podem demonstrar desfechos mensuráveis.
A Ásia-Pacífico está projetada para crescer a um CAGR de 9,45% até 2031, à medida que os laboratórios se expandem na China, Índia e Coreia do Sul e os projetos-piloto públicos examinam a cobertura para ensaios mais recentes. A fabricação doméstica e as licitações sensíveis ao preço influenciam a adoção de swabs nas redes públicas, enquanto as redes de hospitais privados se concentram em PAMG-1 e IGFBP-1 nos centros urbanos. A taxa de natalidade em declínio do Japão e uma força de trabalho obstétrica restrita moderam o crescimento da demanda, mas a adoção direcionada persiste nos centros terciários. Na Austrália, os grupos clínicos monitoraram as implicações das mudanças no fornecimento de fFN nas práticas de transferência rural e buscaram alternativas consistentes para preservar a confiança na triagem. Em todo o Sudeste Asiático, a cadeia de frio limitada e as vias regulatórias fragmentadas retardam a adoção de novos biomarcadores, o que mantém o mercado de kits de teste diagnóstico para parto prematuro ancorado em opções acessíveis e robustas.
A Europa manteve sua participação à medida que as instituições navegavam pelas expectativas regulatórias em evolução e pelos prazos de conformidade com os dispositivos de diagnóstico in vitro. A Alemanha, a França e o Reino Unido incorporam os testes de biomarcadores nas vias de maternidade, embora as avaliações orçamentárias possam retardar a inclusão nos cronogramas de reembolso nacionais. A mudança de 2024 no Reino Unido em direção a testes de triagem alternativos após a descontinuação do fFN destacou a sensibilidade ao custo do setor público e o papel central das diretrizes nacionais. O Sul e o Leste da Europa exibem adoção desigual devido à administração de saúde regionalizada e ao menor gasto per capita, o que sustenta a dependência do julgamento clínico e de testes mais antigos em alguns ambientes. O mercado de kits de teste diagnóstico para parto prematuro na Europa recompensa cada vez mais os fornecedores que conseguem atender às necessidades de documentação e pós-comercialização sem interromper o fornecimento.
O Oriente Médio e a África mostram crescimento incipiente, com hospitais privados no Golfo importando plataformas de biomarcadores ocidentais e centros terciários na África do Sul usando diagnósticos de forma seletiva. A África Subsaariana suporta uma alta carga de partos prematuros, mas enfrenta restrições de infraestrutura que limitam o uso de testes a centros urbanos. Os esforços programáticos continuam a visar complicações relacionadas, como a pré-eclâmpsia, onde novos testes rápidos em desenvolvimento buscam ampliar o acesso em ambientes de menores recursos. Os setores privados da América do Sul no Brasil e na Argentina apoiam a adoção em clínicas urbanas, enquanto os sistemas públicos enfrentam pressões orçamentárias que moderam a escala. Esses fatores regionais mantêm o crescimento do mercado de kits de teste diagnóstico para parto prematuro vinculado à sofisticação das aquisições, à capacidade laboratorial e à disposição dos pagadores de vincular os testes a desfechos mensuráveis.
Cenário Competitivo
O mercado de kits de teste diagnóstico para parto prematuro permanece fragmentado, e a descontinuação do fFN em 2024 redistribuiu oportunidades de participação para múltiplos fornecedores de biomarcadores. A QIAGEN aproveita um portfólio de ruptura de membranas ovulares e trabalho de parto prematuro para venda cruzada dentro de programas de saúde da mulher, o que permite contratos agrupados em redes hospitalares. A Sera Prognostics avança um modelo de laboratório centralizado focado em janelas de rastreamento preventivo e desfechos para pagadores, reforçado por evidências randomizadas de 2026 que apoiam reduções no parto prematuro muito precoce e nas complicações neonatais. Essas estratégias se diferenciam ao longo do tempo e do ambiente de cuidado, o que permite aos fornecedores defender o valor apesar da concorrência de preços nas categorias de swab de commodities.
Os movimentos estratégicos ressaltam a geração de evidências e a cobertura como principais diferenciadores. A Sera relatou engajamentos com pagadores e expansão de sua presença comercial em campo para acelerar a adoção entre redes de prestação integrada. Nos distúrbios hipertensivos da gravidez, a Roche obteve a autorização 510(k) da FDA dos EUA para um teste de razão que informa a intensidade da vigilância e o momento do parto, o que indiretamente expande o conjunto de problemas endereçáveis vinculados ao parto prematuro. Esses avanços regulatórios e dados clínicos ajudam as empresas a articular os benefícios dos desfechos além da precisão preditiva, o que importa para contratos baseados em valor e aquisições baseadas em orçamento.
As pressões de custo e conformidade moldam os incentivos de consolidação sem eliminar espaço para especialistas. As empresas com sistemas de qualidade robustos e experiência regulatória em múltiplas regiões estão melhor posicionadas para navegar pelas evidências em evolução e pelas obrigações pós-comercialização, o que estabiliza o fornecimento e apoia a disciplina de preços. Os novos entrantes que dependem de produtos únicos competem enfatizando acessibilidade, estabilidade em prateleira ou vantagens discretas de fluxo de trabalho que resolvem pontos de dor em ambientes com recursos limitados. O mercado de kits de teste diagnóstico para parto prematuro, portanto, centra-se na velocidade, na agilidade regulatória e no valor vinculado a desfechos que, juntos, impulsionam a adoção duradoura.
Líderes do Setor de Kits de Teste Diagnóstico para Parto Prematuro
-
BIOSYNEX S.A.
-
Laborie Medical Technologies (Clinical Innovations)
-
Medix Biochemica (Actim)
-
QIAGEN N.V.
-
Hologic, Inc.
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes do Setor
- Janeiro de 2026: A Sera Prognostics publicou o estudo PRIME na revista PREGNANCY, demonstrando que o rastreamento com o teste sanguíneo PreTRM combinado com progesterona vaginal diária, aspirina em baixa dose e gerenciamento de cuidados por enfermeiros reduziu os partos antes de 32 semanas em 56% e as internações em UTI neonatal em 20% em 5.018 mulheres inscritas em 19 centros nos EUA. O ensaio clínico randomizado e controlado atingiu ambos os desfechos primários e economizou um dia de UTI neonatal para cada 4,2 pacientes rastreadas, fornecendo evidências de que o rastreamento de biomarcadores a montante combinado com intervenções direcionadas melhora os desfechos neonatais e reduz os custos de saúde.
- Março de 2026: A Sera Prognostics divulgou os resultados financeiros do ano completo de 2025 e observou que comentários europeus no The Journal of Maternal-Fetal & Neonatal Medicine apoiaram a abordagem de teste e tratamento do PreTRM como escalável para sistemas de financiamento público. A empresa divulgou discussões ativas com pagadores de planos comerciais e Medicaid e expandiu sua organização comercial nos EUA para visar uma adoção mais ampla entre redes de prestação integrada.
- Fevereiro de 2025: A Roche Diagnostics recebeu a autorização 510(k) da FDA dos EUA para o teste de razão Elecsys sFlt-1/PlGF para estratificar mulheres grávidas hospitalizadas com distúrbios hipertensivos pelo risco de curto prazo de desenvolver pré-eclâmpsia grave, o que pode informar decisões de vigilância ou parto mais precoce que se intersectam com o risco de parto prematuro.
Escopo do Relatório do Mercado Global de Kits de Teste Diagnóstico para Parto Prematuro
De acordo com o escopo do relatório, os kits de teste diagnóstico para parto prematuro são ensaios rápidos, seja de ponto de atendimento ou baseados em laboratório, projetados para avaliar o risco de parto prematuro em mulheres grávidas. Esses kits funcionam detectando biomarcadores específicos no fluido cervicovaginal ou no sangue, permitindo que os profissionais de saúde determinem se uma mulher sintomática provavelmente dará à luz nos próximos 7 a 14 dias.
O mercado de kits de teste diagnóstico para parto prematuro é segmentado por tipo de produto, material, usuário final e geografia. Por tipo de produto, o mercado é segmentado em fibronectina fetal, baseado em PAMG-1, baseado em IGFBP-1, testes de ruptura de membranas ovulares de marcador duplo e testes de risco proteômico baseados em sangue. Por material, o mercado é segmentado em swab vaginal/cervical e sangue. Por usuário final, o mercado é segmentado em hospitais e centros de maternidade, laboratórios de diagnóstico, centros de parto/clínicas ambulatoriais de ginecologia e obstetrícia e outros. Por geografia, o mercado é segmentado em América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África e América do Sul. O relatório de mercado também abrange os tamanhos de mercado estimados e as tendências para 17 países nas principais regiões globalmente. O relatório oferece o valor (em USD) para os segmentos acima.
| Fibronectina Fetal |
| Baseado em PAMG-1 |
| Baseado em IGFBP-1 |
| Testes de Ruptura de Membranas Ovulares de Marcador Duplo |
| Testes de Risco Proteômico Baseados em Sangue |
| Swab Vaginal/Cervical |
| Sangue |
| Hospitais e Centros de Maternidade |
| Laboratórios de Diagnóstico |
| Centros de Parto / Clínicas Ambulatoriais de Ginecologia e Obstetrícia |
| Outros |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Restante da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Restante da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Restante do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Restante da América do Sul |
| Por Tipo de Produto | Fibronectina Fetal | |
| Baseado em PAMG-1 | ||
| Baseado em IGFBP-1 | ||
| Testes de Ruptura de Membranas Ovulares de Marcador Duplo | ||
| Testes de Risco Proteômico Baseados em Sangue | ||
| Por Material | Swab Vaginal/Cervical | |
| Sangue | ||
| Por Usuário Final | Hospitais e Centros de Maternidade | |
| Laboratórios de Diagnóstico | ||
| Centros de Parto / Clínicas Ambulatoriais de Ginecologia e Obstetrícia | ||
| Outros | ||
| Por Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Restante da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Restante da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Restante do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Restante da América do Sul | ||
Principais Perguntas Respondidas no Relatório
Qual é o tamanho atual e as perspectivas de crescimento do mercado de kits de teste diagnóstico para parto prematuro?
O tamanho do mercado de kits de teste diagnóstico para parto prematuro é de USD 180,78 milhões em 2025 e está projetado para atingir USD 287,57 milhões até 2031 a um CAGR de 8,32% no período de 2026 a 2031.
Qual segmento está crescendo mais rapidamente no mercado de kits de teste diagnóstico para parto prematuro?
As plataformas de PAMG-1 e os ensaios proteômicos baseados em sangue são os de crescimento mais rápido, com CAGRs projetados de 9,67% e 9,01% até 2031, respectivamente.
Como a descontinuação do fFN afetou o mercado de kits de teste diagnóstico para parto prematuro?
A descontinuação dos cassetes quantitativos de fFN em 2024 deslocou as aquisições para biomarcadores alternativos e reforçou o papel dos protocolos hospitalares e das diretrizes nacionais na seleção de produtos.
Quais evidências apoiam o rastreamento assintomático mais precoce neste espaço?
Em 2026, um grande estudo randomizado relatou menos partos prematuros muito precoces e menos complicações neonatais quando uma estratégia de prevenção baseada no PreTRM foi usada em gestações de baixo risco.
Quais regiões lideram e quais estão acelerando no mercado de kits de teste diagnóstico para parto prematuro?
A América do Norte lidera em participação de receita em 2025, enquanto a Ásia-Pacífico está projetada para se expandir mais rapidamente até 2031, à medida que os laboratórios se expandem e os projetos-piloto ampliam o acesso.
Como o mix de usuários finais influencia os padrões de adoção para testes de parto prematuro?
Os hospitais dominam a triagem urgente com swabs rápidos, enquanto os laboratórios de diagnóstico estão crescendo mais rapidamente ao ampliar os testes proteômicos centralizados e os painéis de envio externo que requerem fluxos de trabalho especializados.
Página atualizada pela última vez em: