Tamanho e Participação do Mercado de Sistema de Execução de Manufatura Farmacêutica
Análise do Mercado de Sistema de Execução de Manufatura Farmacêutica por Mordor Intelligence
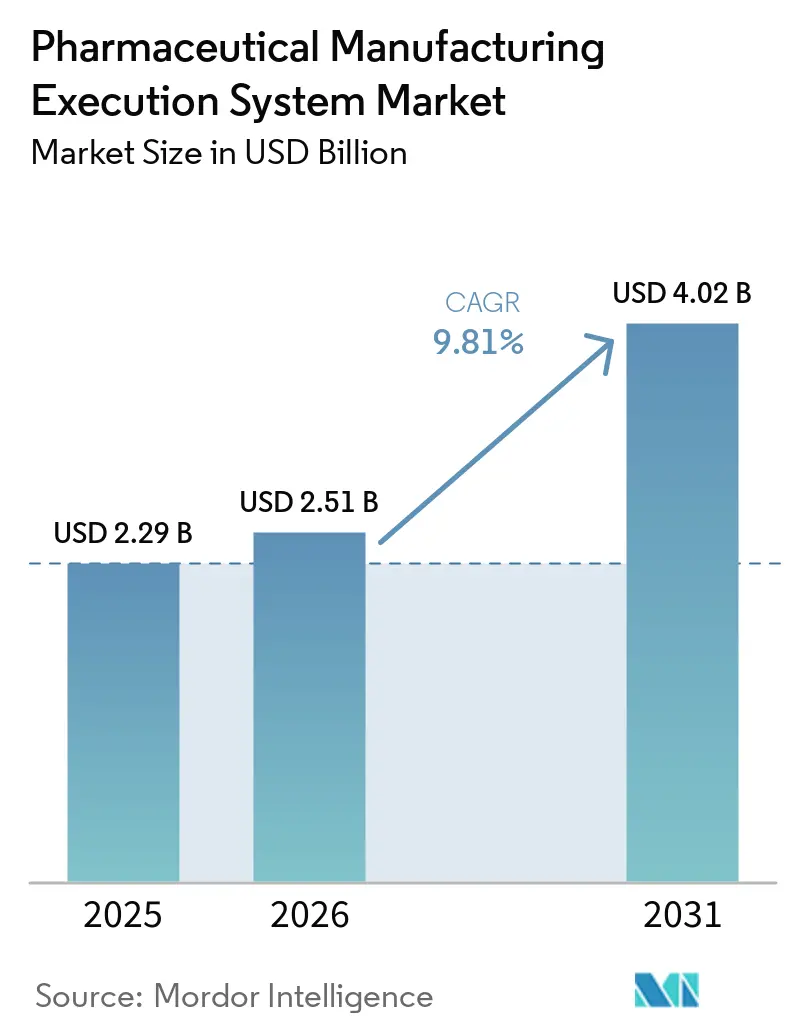
O tamanho do Mercado de Sistema de Execução de Manufatura Farmacêutica está projetado em USD 2,29 bilhões em 2025, USD 2,51 bilhões em 2026, e deve atingir USD 4,02 bilhões até 2031, crescendo a uma CAGR de 9,81% de 2026 a 2031.
A digitalização regulatória, as práticas de validação baseadas em risco e a pressão contínua sobre a integridade de dados e a serialização continuam a direcionar investimentos para plataformas de MES validadas, capazes de orquestrar operações em conformidade em múltiplos sites. O mercado de sistema de execução de manufatura farmacêutica também se beneficia de implantações nativas em nuvem que reduzem a carga de infraestrutura e aceleram implementações globais, mantendo o estado validado e a auditabilidade. Em paralelo, os requisitos de serialização e rastreabilidade interoperável sob regimes maduros estão incorporando conectividade de Nível 4 e mensagens EPCIS nos fluxos de trabalho centrais de MES para visibilidade de ponta a ponta. O rápido crescimento em biológicos e terapias celulares e gênicas está expandindo a demanda por capacidades de MES que gerenciam a cadeia de identidade e a cadeia de custódia com controle determinístico, listas de verificação padronizadas e integração estreita com agendamento, LIMS e cadeia de frio. O mercado de sistema de execução de manufatura farmacêutica está, portanto, migrando da digitalização discreta em nível de site para arquiteturas multinacionais habilitadas para nuvem que padronizam receitas mestre, reduzem ciclos de revisão e melhoram a resiliência da cadeia de suprimentos.
Principais Conclusões do Relatório
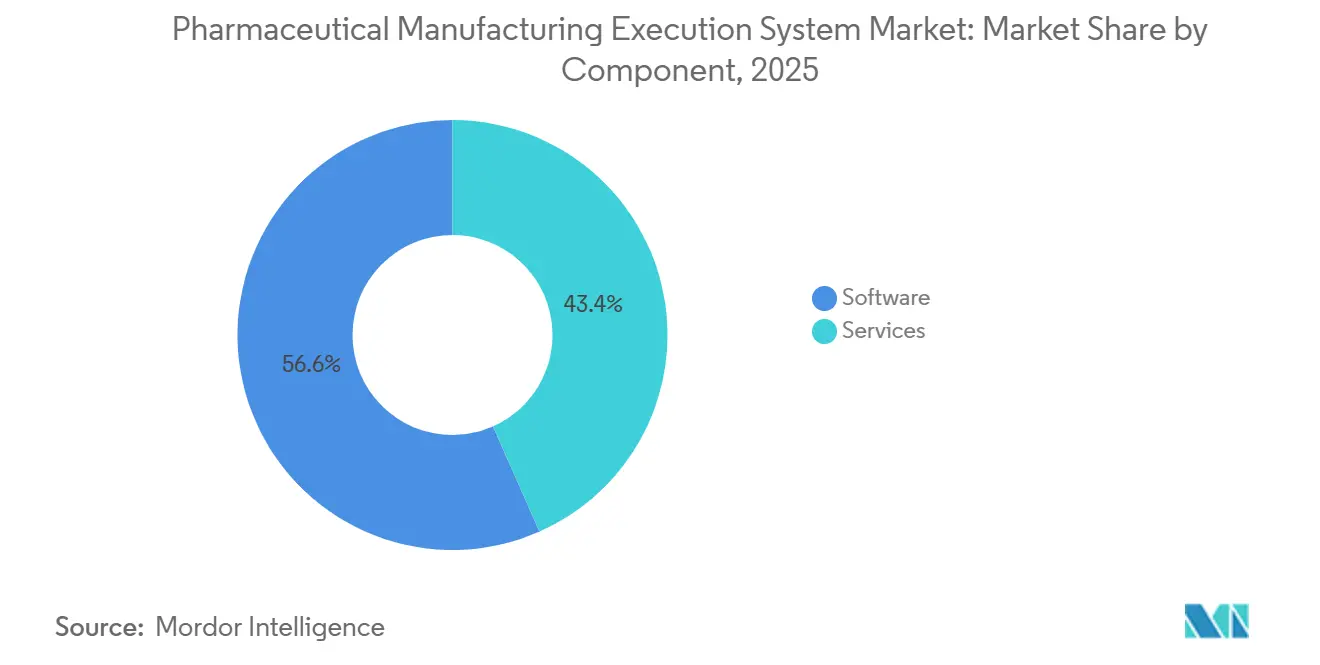
- Por componente, o software capturou 56,64% da participação de receita em 2025, enquanto os serviços devem registrar uma CAGR de 10,23% ao longo de 2026-2031 no mercado de sistema de execução de manufatura farmacêutica.
- Por implantação, a solução local deteve 55,81% em 2025, e a nuvem/SaaS deve expandir a uma CAGR de 13,65% até 2031.
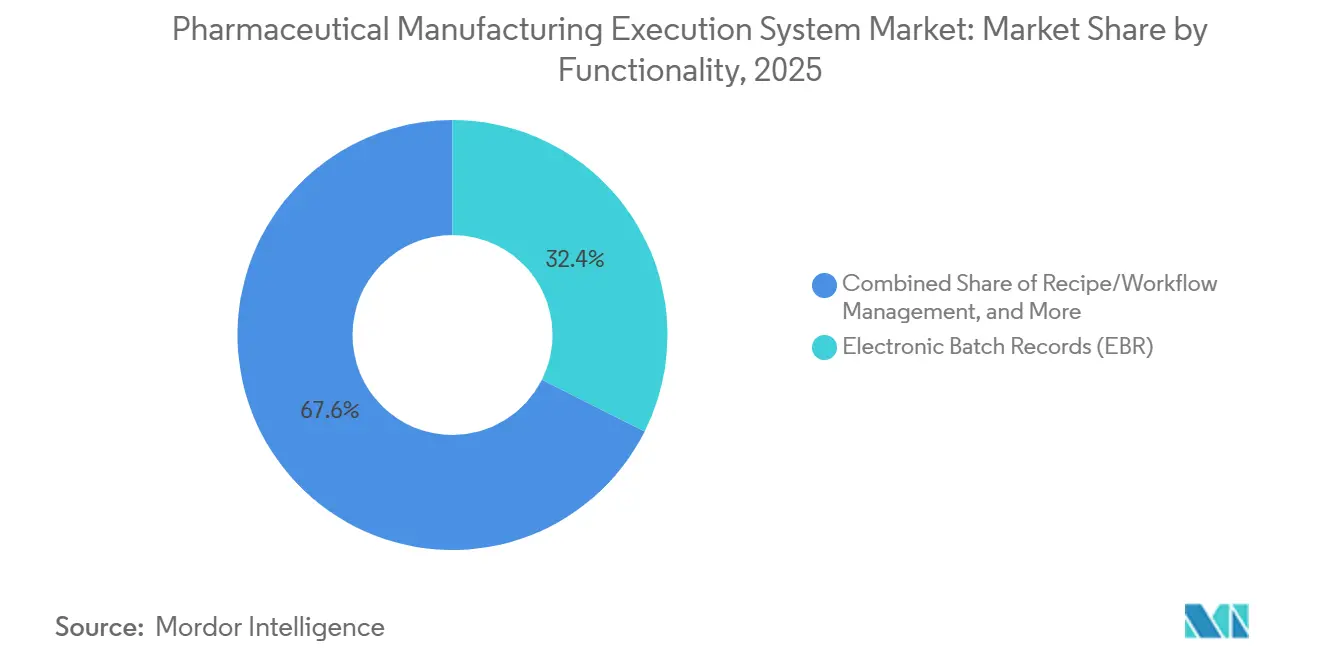
- Por funcionalidade, os registros eletrônicos de lote lideraram com 32,40% em 2025, e a integração de serialização avança a uma CAGR de 12,78% até 2031 no mercado de sistema de execução de manufatura farmacêutica.
- Por usuário final, os fabricantes farmacêuticos responderam por 42,54% em 2025, enquanto os fabricantes de terapias celulares e gênicas têm projeção de CAGR de 14,93% entre 2026 e 2031 no mercado de sistema de execução de manufatura farmacêutica.
- Por geografia, a América do Norte deteve 37,23% da participação do mercado de sistema de execução de manufatura farmacêutica em 2025, enquanto a Ásia-Pacífico registrou a maior CAGR projetada de 15,83% até 2031.
Nota: O tamanho do mercado e os números de previsão neste relatório são gerados usando a estrutura de estimativa proprietária da Mordor Intelligence, atualizada com os dados e percepções mais recentes disponíveis em janeiro de 2026.
Tendências e Perspectivas do Mercado Global de Sistema de Execução de Manufatura Farmacêutica
Análise de Impacto dos Impulsionadores
| Impulsionador | (~) % de Impacto na Previsão de CAGR | Relevância Geográfica | Prazo de Impacto |
|---|---|---|---|
| Conformidade Regulatória e Requisitos de Integridade de Dados | +3.2% | Global, com maior peso na América do Norte e na UE devido à escalada de fiscalização da FDA e da EMA | Curto prazo (≤ 2 anos) |
| Impulso de Digitalização da Pharma 4.0 (ISPE) | +2.1% | América do Norte como núcleo, Ásia-Pacífico como seguidores rápidos | Médio prazo (2-4 anos) |
| Necessidade de Visibilidade em Tempo Real e Rastreabilidade de Ponta a Ponta | +1.8% | Global, particularmente crítico em centros de biológicos (EUA, UE, Singapura) | Curto prazo (≤ 2 anos) |
| Crescimento em Biológicos, Terapias Celulares e Gênicas | +2.4% | Corredor de biotecnologia dos EUA, UE (Alemanha, Suíça), adotantes iniciais na China/Singapura | Longo prazo (≥ 4 anos) |
| Garantia de Software Computacional (CSA) Habilitando Validação Baseada em Risco | +1.3% | América do Norte, sites progressivos da UE | Médio prazo (2-4 anos) |
| Manufatura Contínua (ICH Q13) e Liberação em Tempo Real | +1.6% | Adotantes iniciais nos EUA, UE, projetos-piloto na Ásia-Pacífico | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Requisitos de Conformidade Regulatória e Integridade de Dados Aceleram o Investimento em MES
Os fabricantes regulamentados estão reforçando sistemas eletrônicos validados para se alinhar aos requisitos da 21 CFR Parte 11 para registros eletrônicos confiáveis, assinaturas eletrônicas e trilhas de auditoria que possam suportar investigações rigorosas. As plataformas de MES abordam isso com fluxos de trabalho controlados, ações com registro de data e hora e logs de auditoria imutáveis que reduzem o risco de erros e fortalecem a integridade dos dados.[1]Equipe Dot Compliance, "Conformidade com a FDA 21 CFR Parte 11: O Que Você Precisa Saber em 2026," Dot Compliance A serialização e a rastreabilidade interoperável estão impulsionando uma integração mais profunda entre MES e repositórios corporativos para garantir visibilidade em nível de unidade, lote e remessa ao longo de todo o ciclo de vida do produto. [2]SAP, "SAP Advanced Track and Trace for Pharmaceuticals," SAP À medida que os fabricantes substituem registros em papel e híbridos por execução de lotes digitalizada e revisão por exceção, eles comprimem os tempos de ciclo e aprimoram a prontidão para liberação com desvios acionáveis, assinaturas e completude probatória.[3]Honeywell, "Honeywell Apresenta Plataforma de Automação Assistida por IA para Transformar o Setor de Manufatura de Ciências da Vida," Essa mudança orientada pela conformidade é visível no escopo de projetos e nas avaliações de fornecedores que priorizam modelos validados, ciclos de vida de desenvolvimento seguros e prontidão de auditoria comprovada.[4]Rockwell Automation, "Rockwell Automation Lança PharmaSuite 12.00 para Acelerar Implantações Seguras e Escaláveis," O mercado de sistema de execução de manufatura farmacêutica está, portanto, se inclinando para plataformas que possam demonstrar integridade de dados totalmente alinhada à ALCOA e geração simplificada de evidências para auditorias e inspeções.
O Impulso de Digitalização da Pharma 4.0 Remodela os Modelos Operacionais
A digitalização nas operações está avançando em direção a arquiteturas prontas para nuvem, conteinerizadas e habilitadas para baixo código que trazem agilidade à validação e ao controle de mudanças, preservando o estado validado. As plataformas de MES que unificam a execução no chão de fábrica com qualidade e análises criam uma visão operacional comum para operadores, supervisores e controle de qualidade, o que apoia a tomada de decisões em tempo real e uma melhor disposição de lotes. Os programas de melhoria contínua também se apoiam em receitas mestre padronizadas e instruções de trabalho eletrônicas para eliminar a variabilidade e reduzir os tempos de espera, o que é consistente com as ambições de liberação em tempo real. À medida que as ferramentas de baixo código se tornam incorporadas nos ecossistemas de MES, os engenheiros de processo podem iterar fluxos de trabalho e formulários mais rapidamente sem código personalizado extenso, o que encurta os ciclos de design e validação sob abordagens baseadas em risco.[5]Tulip, "Sistema de Execução de Manufatura (MES) para Farmacêutica," O efeito líquido é que o mercado de sistema de execução de manufatura farmacêutica está se alinhando com os princípios da Pharma 4.0 ao convergir execução, qualidade, serialização e análises com opções de implantação flexíveis que escalam de uma única linha para redes multiplanta.
A Necessidade de Visibilidade em Tempo Real Impulsiona a Adoção da Revisão por Exceção
Os fabricantes estão migrando a revisão de lotes do pós-produção para a revisão concorrente por exceção, a fim de reduzir os ciclos de liberação e diminuir as verificações manuais. Na prática, o MES aplica regras de aceitação às ações e resultados registrados, identifica exceções para intervenção humana e encaminha os problemas para fluxos de trabalho de CAPA padronizados que aceleram o encerramento. A mesma espinha dorsal digital permite painéis de equipamentos em tempo real e genealogia de materiais, o que suporta reescalonamento mais rápido, recalls direcionados e respostas mais resilientes a paralisações não planejadas. À medida que as equipes ganham confiança na captura de dados contemporânea do MES e dos sistemas conectados, a dependência de registros em papel diminui e a prontidão para auditoria se fortalece. O mercado de sistema de execução de manufatura farmacêutica está, portanto, registrando demanda sustentada por módulos de EBR habilitadores de revisão por exceção e gerenciamento integrado de desvios, pois eles proporcionam economias de tempo mensuráveis e consistência de qualidade em escala.
O Crescimento em Biológicos, Terapias Celulares e Gênicas Exige Infraestrutura de Execução Especializada
Os programas de biológicos e terapias celulares e gênicas requerem orquestração precisa entre agendamento de pacientes, materiais, análises e logística, com uma cadeia de identidade e cadeia de custódia de ponta a ponta. Os fornecedores estão respondendo com camadas de orquestração especializadas, hardware de sistema fechado e fluxos de trabalho digitais validados para gerenciar execuções específicas de pacientes sem risco de contaminação cruzada. As implantações de MES hospedadas em nuvem estão ganhando tração em ambientes clínicos e comerciais iniciais de terapias celulares e gênicas para simplificar as operações globais, preservando a integridade dos dados e as trilhas de auditoria. À medida que os programas de terapias celulares e gênicas escalam, a integração entre MES, LIMS, serialização e ERP torna-se essencial para manter a identidade do lote, coordenar os cronogramas de aférese até infusão e garantir o rastreamento correto da dose. Esse perfil de necessidade especializada está elevando a demanda no mercado de sistema de execução de manufatura farmacêutica por capacidades que sejam nativamente centradas no paciente e interoperáveis ao longo do continuum clínico e comercial.
Análise de Impacto das Restrições
| Restrição | (~) % de Impacto na Previsão de CAGR | Relevância Geográfica | Prazo de Impacto |
|---|---|---|---|
| Alto Custo de Implementação e Complexidade do Programa | -1.4% | Empresas de médio porte globalmente, agudo em mercados da Ásia-Pacífico sensíveis a custos | Curto prazo (≤ 2 anos) |
| Integração com Sistemas Legados e Silos de Dados | -0.9% | Farmacêuticas maduras com sites brownfield (América do Norte, Europa Ocidental) | Médio prazo (2-4 anos) |
| Lacunas de Talentos em Validação e Gargalos na Transição CSV/CSA | -0.7% | Global, particularmente agudo em CDMOs da Ásia-Pacífico | Médio prazo (2-4 anos) |
| Deficiências na Prontidão de Padronização de Dados Mestre e Processos | -0.5% | Farmacêuticas multissite (América do Norte, UE), CDMOs de crescimento rápido na Ásia-Pacífico | Curto prazo (≤ 2 anos) |
| Fonte: Mordor Intelligence | |||
Alto Custo de Implementação e Complexidade do Programa Atrasam a Adoção no Mercado Intermediário
A complexidade do programa continua sendo uma barreira para organizações com equipes de TI e controle de qualidade enxutas, pois o MES é um programa de transformação e não uma simples instalação de software. Os modelos nativos em nuvem e de serviço gerenciado estão ganhando preferência porque reduzem a propriedade de infraestrutura, simplificam a qualificação e transferem mais documentação de validação para fornecedores que operam práticas seguras de desenvolvimento e liberação. Os kits de ferramentas de baixo código também estão emergindo para acelerar o valor, permitindo que as equipes de manufatura configurem fluxos de trabalho e formulários validados mais rapidamente com menos código personalizado. Alguns fornecedores agora empacotam conteúdo pré-validado, horas de consultoria e modelos do setor para reduzir o esforço de validação para equipes farmacêuticas e de biotecnologia emergentes. Mesmo com esses avanços, muitos compradores do mercado intermediário ritimam as implantações para se alinhar com a capacidade de controle de mudanças e a prontidão do site, o que pode prolongar os cronogramas gerais apesar dos ganhos tecnológicos. O mercado de sistema de execução de manufatura farmacêutica continua a abordar essa restrição com roteiros em fases, projetos-piloto hospedados em nuvem e conteúdo pré-construído que pode ser replicado entre plantas sem retrabalho.
A Integração com Sistemas Legados Fragmenta a Continuidade Digital
Os sites brownfield heterogêneos devem conectar CLPs, SCADA, historiadores, LIMS, ERP e repositórios de serialização em um tecido de dados coerente e governado, sem links ponto a ponto frágeis. Muitas empresas farmacêuticas identificam a integração de equipamentos legados como uma barreira primária para o sucesso do MES, o que impulsiona o interesse em middleware rico em conectores e interfaces padronizadas que reduzem a sobrecarga de validação e manutenção. Os silos de dados também aumentam os custos de relatórios e retardam as investigações, razão pela qual os projetos incluem cada vez mais uma camada de dados governada que unifica registros de lotes, qualidade e suprimentos sob uma única estrutura de conformidade. Os mandatos de serialização acrescentam a essa agenda de integração ao exigir uma associação estreita entre o contexto do lote no MES e os identificadores em nível de unidade nos repositórios corporativos para relatórios globais. Os fornecedores estão respondendo com gerenciadores de site modulares, mensagens EPCIS 1.2 e escalabilidade em nuvem que reduzem interfaces personalizadas enquanto mantêm as salvaguardas de integridade de dados. O mercado de sistema de execução de manufatura farmacêutica está, portanto, migrando para conectores agnósticos de fornecedor, pacotes de integração pré-construídos e serviços em nuvem gerenciados ao longo do ciclo de vida que simplificam a integração em parques industriais diversificados.
Análise de Segmentos
Por Componente: O Crescimento dos Serviços Reflete a Complexidade dos Ecossistemas de TI Farmacêutica
O software capturou 56,64% da participação do mercado de sistema de execução de manufatura farmacêutica em 2025, e os Serviços devem expandir a uma CAGR de 10,23% ao longo de 2026-2031, refletindo a crescente demanda por implantação liderada por especialistas, validação e suporte ao ciclo de vida. Os compradores continuam a priorizar fornecedores com EBR comprovado, gerenciamento de desvios e integração de serialização, juntamente com práticas de desenvolvimento seguro e trilhas de auditoria robustas. À medida que as organizações expandem as implantações multissite, elas também requerem serviços sustentados para gerenciar versões, testes de regressão e notas de versão em linha com os sistemas de qualidade. O mercado de sistema de execução de manufatura farmacêutica está, portanto, registrando taxas de adesão mais amplas para treinamento, validação gerenciada e suporte 24x7 para manter um estado validado durante as atualizações. No lado da força de trabalho, fornecedores e integradores estão ajudando a fechar lacunas de habilidades com currículos certificados para que operadores, controle de qualidade e administradores de TI possam sustentar operações em conformidade. Esse modelo centrado em serviços é reforçado pelo MES em nuvem, onde os provedores qualificam a infraestrutura e entregam conteúdo pré-validado que reduz a carga do cliente durante implantações e atualizações de rotina.
O crescimento dos serviços também reflete a complexidade de integrar o MES com sistemas de automação, qualidade e corporativos em ambientes brownfield. As equipes do setor favorecem cada vez mais parceiros que trazem conectores pré-construídos, modelos de validação e aceleradores de receitas para reduzir os cronogramas dos projetos sem sacrificar a conformidade. O setor de sistema de execução de manufatura farmacêutica está adotando ferramentas de baixo código para acelerar a configuração de formulários e fluxos de trabalho sob controle de mudanças, o que, por sua vez, eleva a demanda por serviços de governança e gerenciamento do ciclo de vida. Os fornecedores também estão agrupando horas de consultoria com novas licenças e ofertas como serviço para alinhar o escopo com atividades de garantia baseadas em risco e prontidão do site. Essa migração em direção à entrega de valor liderada por serviços posiciona o mercado de sistema de execução de manufatura farmacêutica para uma expansão sustentada de serviços à medida que a maturidade digital avança em grandes farmacêuticas, biotecnologias e CDMOs.
Por Implantação: Nuvem/SaaS Ganha Tração à Medida que a Carga de Validação Migra para os Fornecedores
As implantações locais detiveram 55,81% em 2025, enquanto a Nuvem/SaaS deve ser o caminho de crescimento mais rápido a uma CAGR de 13,65% ao longo de 2026-2031, à medida que os compradores equilibram a soberania de dados com agilidade e velocidade para obter valor. Os modelos de MES nativos em nuvem e como serviço estão reduzindo a propriedade de infraestrutura, permitindo implementações globais mais rápidas e padronizando atualizações com pacotes de testes automatizados gerenciados pelo fornecedor. As plataformas conteinerizadas adicionam flexibilidade ao permitir topologias híbridas que mantêm a execução da produção próxima à linha, enquanto movem análises e relatórios para computação em nuvem elástica. As capacidades de baixo código em suítes modernas ajudam as equipes de processo a configurar formulários e fluxos de trabalho sem código personalizado extenso, o que comprime os ciclos de design e reduz o backlog de TI. Os provedores também estão fortalecendo os controles de segurança cibernética com práticas de desenvolvimento seguro, orientações de proteção e pacotes de documentação que se alinham com as expectativas de qualidade do cliente para operações validadas.
Os modelos híbridos agora servem como uma ponte pragmática à medida que as equipes modernizam plantas brownfield, mantendo o tempo de atividade e o controle determinístico para etapas regulamentadas. À medida que os CDMOs escalam portfólios entre regiões, o SaaS multilocatário torna-se atraente para receitas mestre padronizadas, fluxos de trabalho de qualidade específicos do cliente e integração mais rápida com governança centralizada. A orquestração em nuvem da serialização suporta ainda mais redes de suprimentos distribuídas, vinculando eventos de embalagem, comissionamento e mensagens de remessa com contexto de lote para consultas posteriores. O mercado de sistema de execução de manufatura farmacêutica está, portanto, convergindo para a flexibilidade de implantação, onde opções locais, de nuvem privada e de nuvem pública podem ser combinadas para equilibrar controle, escalabilidade e conformidade. Os provedores que entregam conteúdo pré-validado, atualizações gerenciadas e pilhas seguras por design continuarão a se destacar à medida que os compradores buscam simplificar o custo total de propriedade sem comprometer a prontidão para auditoria.
Por Funcionalidade: A Integração de Serialização Emerge como o Módulo de Crescimento Mais Rápido
Os registros eletrônicos de lote permaneceram como a maior funcionalidade em 2025 com 32,40%, enquanto a Integração de Serialização deve ser a capacidade de crescimento mais rápido a uma CAGR de 12,78% ao longo de 2026-2031, à medida que a rastreabilidade interoperável se torna uma expectativa de base. A DSCSA e as diretivas globais relacionadas exigem intercâmbio de dados interoperável que vincule números de série, lotes e remessas ao contexto de execução de lotes, o que está impulsionando uma integração mais profunda entre MES e repositórios de Nível 4. Os módulos modernos de serialização atuam como gerenciadores de site e hubs de mensagens que unificam linhas de embalagem, MES, ERP e sistemas nacionais usando padrões como EPCIS com escalabilidade em nuvem para eventos de pico. Em investigações de qualidade, desvios e CAPA, os dados de serialização são agora rotineiramente referenciados para restringir o escopo de recalls e identificar lotes de fornecedores suspeitos mais rapidamente. O mercado de sistema de execução de manufatura farmacêutica está alinhando EBR, gerenciamento de desvios e serialização para suportar recalls direcionados e disposição mais rápida com forte integridade de dados.
À medida que os repositórios se expandem e as regras específicas de cada país evoluem, interfaces escaláveis e conectores gerenciados ao longo do ciclo de vida estão reduzindo o código personalizado e o retrabalho de validação. As plataformas de serialização nativas em nuvem que podem operar localmente, em nuvens de clientes ou como SaaS gerenciado ajudam a harmonizar as operações em portfólios multirregionais. A integração com o MES também traz trilhas de auditoria com registro de data e hora e assinaturas eletrônicas para cada evento de comissionamento, agregação e descomissionamento. Para os fabricantes, essa convergência suporta revisão por exceção, análises de lote dourado e melhorias contínuas ancoradas em dados consistentes e consultáveis. O tamanho do mercado de sistema de execução de manufatura farmacêutica para módulos focados em serialização está, portanto, posicionado para crescimento sustentado à medida que a conformidade e a resiliência da cadeia de suprimentos permanecem no topo das agendas executivas.
Nota: As participações de segmento de todos os segmentos individuais estão disponíveis mediante a compra do relatório
Por Usuário Final: Fabricantes de Terapias Celulares e Gênicas Impulsionam a Expansão Mais Rápida do Segmento
Os fabricantes farmacêuticos responderam por 42,54% em 2025, enquanto os Fabricantes de Terapias Celulares e Gênicas devem registrar uma CAGR de 14,93% em 2026-2031, à medida que as operações específicas de pacientes requerem orquestração digital profunda. A manufatura centrada no paciente requer uma cadeia de identidade e cadeia de custódia de ponta a ponta que sejam aplicadas eletronicamente em cada etapa, o que está criando demanda por orquestração integrada ao MES e pontos de controle de controle de qualidade. Os fornecedores estão lançando plataformas de orquestração especializadas e de sistema fechado que condensam as áreas de sala limpa e permitem que um único operador processe múltiplos lotes de pacientes, mantendo isolamento e rastreabilidade. O MES em nuvem também está entrando em ambientes clínicos e comerciais iniciais para acelerar a configuração global e manter a documentação de validação atualizada com atualizações frequentes sob uma construção de serviço gerenciado. O mercado de sistema de execução de manufatura farmacêutica está, portanto, expandindo a cobertura para verificações de cadeia de identidade, rastreamento de dose serializado e agendamento sensível ao tempo, garantindo trilhas de auditoria em conformidade.
Os fabricantes biofarmacêuticos continuam a padronizar EBR e gerenciamento de desvios para operações complexas de biológicos, onde altos volumes de dados e monitoramento contínuo exigem controles robustos de integridade. Os CDMOs dependem de SaaS multilocatário e bibliotecas de modelos para integrar clientes rapidamente e harmonizar processos de qualidade em portfólios de produtos diversificados. A interoperabilidade com LIMS e serialização garante que materiais, amostras e doses permaneçam estreitamente acoplados ao contexto do lote para liberação e relatórios de farmacovigilância. Como resultado, o setor de sistema de execução de manufatura farmacêutica está ampliando os conjuntos de recursos para suportar transições clínico-comerciais com receitas padronizadas, dados mestre de referência e controle de mudanças governado. O mercado de sistema de execução de manufatura farmacêutica continuará a priorizar módulos que lidam com produtos serializados, agendamento de pacientes e análises multissite que encurtam o tempo para escalar.
Análise Geográfica
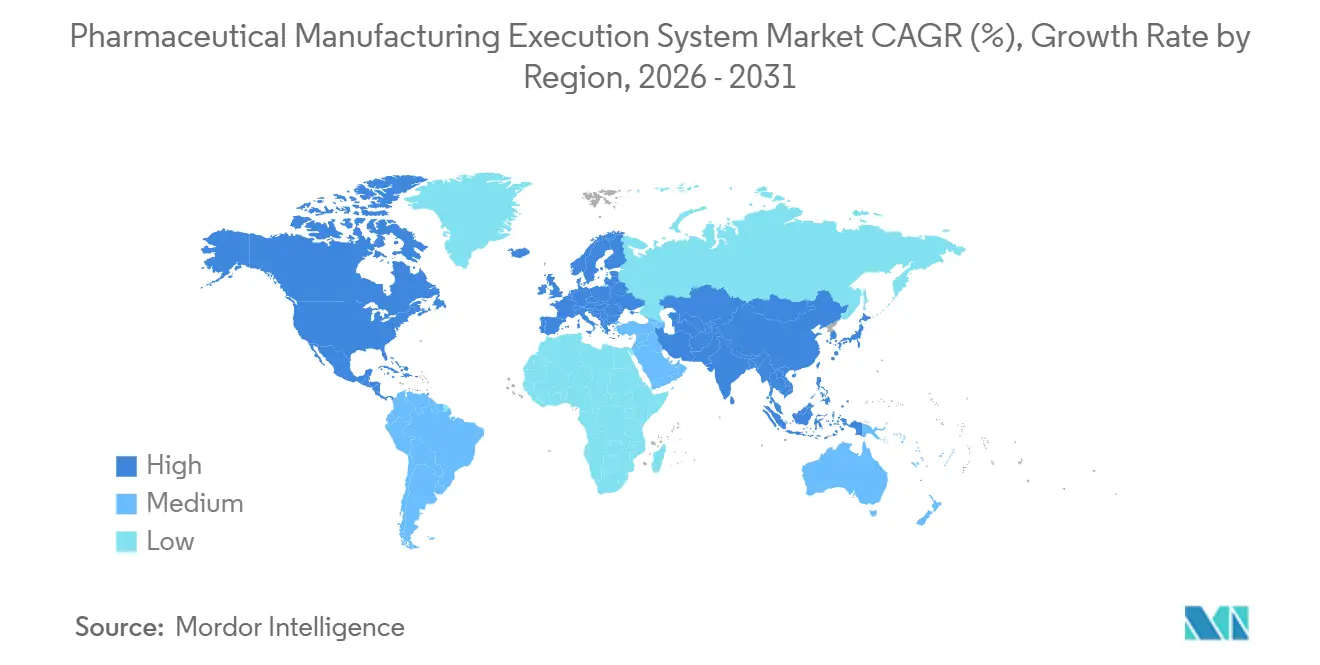
A América do Norte deteve 37,23% da participação do mercado de sistema de execução de manufatura farmacêutica em 2025, ancorada por estruturas regulatórias maduras e uma base profunda de inovadores em clusters de biotecnologia. As prioridades dos compradores em 2026 centram-se em implantações de MES habilitadas para nuvem que preservam o estado validado enquanto melhoram a velocidade de mudança em múltiplas plantas. As grandes farmacêuticas e os principais CDMOs continuam as reformas em sites legados para padronizar EBR, integrar serialização e habilitar a revisão por exceção em portfólios de produtos diversificados. A região também está investindo em plataformas de terapia celular de sistema fechado e ferramentas de orquestração que unificam agendamento, execução de lotes e evidências de controle de qualidade de forma compatível. Essa base suporta o crescimento contínuo no mercado de sistema de execução de manufatura farmacêutica à medida que as empresas expandem modelos multissite, fortalecem a integridade dos dados e constroem resiliência na cadeia de suprimentos.
A Ásia-Pacífico é a região de crescimento mais rápido com uma CAGR de 15,83% ao longo de 2026-2031 para o tamanho do mercado de sistema de execução de manufatura farmacêutica, impulsionada por expansões de capacidade em biológicos e pelo aumento de escala dos serviços de CDMO. À medida que os fabricantes adicionam novas linhas e instalações, a demanda está crescendo por EBR padronizado, opções de nuvem validadas e atualizações gerenciadas pelo fornecedor que reduzem o tempo de qualificação. Os CDMOs regionais adotam conteúdo de MES modular para integrar patrocinadores rapidamente e manter práticas de qualidade harmonizadas em portfólios multiclientes. Os fornecedores também estão trabalhando com clientes em estratégias de conectores para equipamentos mais antigos e sistemas pontuais para minimizar o código personalizado e simplificar a validação. Essas prioridades mantêm o mercado de sistema de execução de manufatura farmacêutica focado em interoperabilidade, escalabilidade em nuvem e operações seguras por design em toda a crescente pegada de manufatura da Ásia-Pacífico.
A Europa continua a avançar por meio de governança de dados padronizada, expectativas mais fortes de segurança cibernética e abordagens de qualidade por design que favorecem sistemas digitais validados. Em toda a UE, a harmonização de serialização, rastreamento e rastreabilidade e qualificação em nível de site está promovendo um acoplamento mais estreito entre MES, ERP e repositórios corporativos. O mercado de sistema de execução de manufatura farmacêutica na Europa também está enfatizando implantações em nuvem e híbridas que preservam o controle local enquanto centralizam análises e dados mestre. À medida que os fornecedores aprofundam as capacidades de baixo código e o conteúdo pré-validado, os fabricantes europeus estão acelerando as atualizações sem comprometer a disciplina de validação, especialmente em clusters de biológicos. Esses padrões reforçam a demanda constante no mercado de sistema de execução de manufatura farmacêutica à medida que as empresas modernizam as operações, expandem a cobertura de serialização e escalam modelos multissite.
Cenário Competitivo
O mercado de sistema de execução de manufatura farmacêutica permanece competitivo com grandes empresas globais de automação, provedores de software corporativo e desafiantes nativos em nuvem atendendo a necessidades de compradores sobrepostas, mas distintas. Os fornecedores estão se diferenciando com serviços em nuvem validados, conteúdo de EBR pré-construído e integração comprovada com repositórios de ERP e serialização para um tempo de valor mais rápido. As plataformas que combinam execução, qualidade e análises estão ganhando participação nas contas à medida que os clientes migram da digitalização pontual para operações integradas e revisão por exceção. Os compradores continuam a valorizar fluxos de trabalho configuráveis, desenvolvimento seguro e trilhas de auditoria de ponta a ponta, o que favorece provedores com modelos validados e gerenciamento rigoroso do ciclo de vida.
Os movimentos estratégicos ilustram para onde o mercado está se dirigindo. A Rockwell introduziu uma versão conteinerizada que suporta modelos de implantação híbrida e em nuvem com instaladores automatizados e segurança cibernética incorporada ao processo de desenvolvimento, o que ajuda a padronizar as implementações entre plantas. A Körber expandiu uma solução de serialização nativa em nuvem que integra linhas de embalagem, MES e ERP enquanto gerencia diversos requisitos de países sob uma plataforma gerenciada ao longo do ciclo de vida. A Honeywell lançou uma plataforma nativa em nuvem assistida por IA que vincula o controle crítico à qualidade digital para reduzir erros de métodos baseados em papel e acelerar a introdução digital de novos produtos. A Siemens incorporou desenvolvimento de baixo código que permite às equipes de processo configurar aplicativos nativamente, o que encurta os ciclos de design e validação e suporta as práticas da Pharma 4.0.
A entrega de valor liderada por serviços também é um tema definidor. Os fornecedores e integradores estão empacotando horas de consultoria, conteúdo pré-validado e testes automatizados que se alinham com abordagens de garantia baseadas em risco e reduzem a sobrecarga de documentação do cliente. As arquiteturas SaaS multilocatário visam CDMOs que precisam de modelos compartilhados e fluxos de trabalho específicos do cliente, enquanto as plataformas de sistema fechado para terapia celular reduzem as áreas de sala limpa e aumentam o rendimento por operador. Em todos esses movimentos, o mercado de sistema de execução de manufatura farmacêutica está tendendo para estratégias modulares, escaláveis em nuvem e com prioridade de interoperabilidade que aceleram as implantações sem diluir a integridade dos dados ou a prontidão para auditoria.
Líderes do Setor de Sistema de Execução de Manufatura Farmacêutica
ABB Ltd.
Emerson Electric Co.
Honeywell International Inc.
Körber AG
Rockwell Automation, Inc.
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes do Setor
- Março de 2026: A Sartorius lançou a Plataforma de Terapia Celular Eveo, um sistema modular integrado para produção de terapia celular autóloga, permitindo um aumento quádruplo na produção dentro dos espaços de sala limpa existentes. Um operador pode processar oito lotes de pacientes simultaneamente, produzindo mais de 350 doses anualmente em comparação com aproximadamente 100 doses anteriormente, potencialmente reduzindo os custos de manufatura de CAR-T em aproximadamente 90% por meio de design compacto e automação de fluxo de trabalho.
- Maio de 2025: A Rockwell Automation lançou o FactoryTalk PharmaSuite 12.00, introduzindo implantação baseada em nuvem via contêineres Kubernetes com compatibilidade com Linux, instalação automatizada por meio da ferramenta de configuração MICKA e segurança cibernética aprimorada desenvolvida sob práticas certificadas de desenvolvimento seguro.
- Abril de 2025: A Honeywell introduziu o TrackWise Manufacturing, uma plataforma nativa em nuvem assistida por IA entre as primeiras em ciências da vida a integrar ambientes de manufatura digital e físico. A plataforma conteinerizada aproveita o Controlador de Operações de Unidade da Honeywell para controle crítico e incorpora uma estrutura de qualidade para manufatura de qualidade por design, acelerando a introdução de medicamentos enquanto reduz erros e ineficiências de métodos baseados em papel.
Escopo do Relatório do Mercado Global de Sistema de Execução de Manufatura Farmacêutica
De acordo com o escopo do relatório, um sistema de execução de manufatura farmacêutica (MES) é um sistema baseado em software utilizado para monitorar, controlar e documentar os processos de fabricação de medicamentos em tempo real. Ele conecta as operações do chão de fábrica com os sistemas corporativos para garantir produção eficiente, integridade de dados e visibilidade do processo. Em ambientes farmacêuticos, o MES é fundamental para gerenciar registros eletrônicos de lote, garantir a conformidade regulatória e habilitar a rastreabilidade completa de materiais e processos.
O mercado de sistema de execução de manufatura farmacêutica é segmentado por componente, implantação, funcionalidade, usuário final e geografia. Por componente, o mercado é segmentado em software e serviços. Por implantação, o mercado é segmentado em local e nuvem / SaaS. Por funcionalidade, o mercado é segmentado em registros eletrônicos de lote (EBR), gerenciamento de receitas/fluxo de trabalho, gerenciamento de equipamentos, integração de desvios e CAPA, integração de serialização e outros. Por usuário final, o mercado é segmentado em fabricantes farmacêuticos, fabricantes biofarmacêuticos, fabricantes de terapias celulares e gênicas e CMOs / CDMOs. Por geografia, o mercado é segmentado em América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África e América do Sul. O relatório de mercado também cobre tamanhos de mercado estimados e tendências de mercado para 17 países nas principais regiões do mundo. O relatório oferece valor de mercado (em USD) para os segmentos acima.
| Software |
| Serviços |
| Local |
| Nuvem / SaaS |
| Registros Eletrônicos de Lote (EBR) |
| Gerenciamento de Receitas / Fluxo de Trabalho |
| Gerenciamento de Equipamentos |
| Integração de Desvios e CAPA |
| Integração de Serialização |
| Outros |
| Fabricantes Farmacêuticos |
| Fabricantes Biofarmacêuticos |
| Fabricantes de Terapias Celulares e Gênicas |
| CMOs / CDMOs |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Restante da Europa | |
| Ásia-Pacífico | China |
| Índia | |
| Japão | |
| Austrália | |
| Coreia do Sul | |
| Restante da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Restante do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Restante da América do Sul |
| Por Componente | Software | |
| Serviços | ||
| Por Implantação | Local | |
| Nuvem / SaaS | ||
| Por Funcionalidade | Registros Eletrônicos de Lote (EBR) | |
| Gerenciamento de Receitas / Fluxo de Trabalho | ||
| Gerenciamento de Equipamentos | ||
| Integração de Desvios e CAPA | ||
| Integração de Serialização | ||
| Outros | ||
| Por Usuário Final | Fabricantes Farmacêuticos | |
| Fabricantes Biofarmacêuticos | ||
| Fabricantes de Terapias Celulares e Gênicas | ||
| CMOs / CDMOs | ||
| Por Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Restante da Europa | ||
| Ásia-Pacífico | China | |
| Índia | ||
| Japão | ||
| Austrália | ||
| Coreia do Sul | ||
| Restante da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Restante do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Restante da América do Sul | ||
Principais Perguntas Respondidas no Relatório
Qual é o tamanho projetado e a CAGR para o mercado de sistema de execução de manufatura farmacêutica até 2031?
O tamanho do mercado de sistema de execução de manufatura farmacêutica está projetado para atingir USD 4,02 bilhões até 2031, registrando uma CAGR de 9,81% ao longo de 2026-2031.
Qual modelo de implantação está crescendo mais rapidamente no espaço de sistema de execução de manufatura farmacêutica?
A Nuvem/SaaS apresenta o crescimento mais rápido com uma CAGR projetada de 13,65% ao longo de 2026-2031, à medida que os compradores adotam serviços validados e gerenciados pelo fornecedor para velocidade e escalabilidade.
Quais áreas de funcionalidade estão registrando a adoção mais rápida?
A Integração de Serialização está avançando mais rapidamente à medida que a rastreabilidade interoperável se torna obrigatória e estreitamente acoplada aos fluxos de trabalho de MES para visibilidade de ponta a ponta e relatórios em conformidade.
O que está impulsionando a adoção da revisão por exceção na liberação de lotes?
O EBR digitalizado com verificações baseadas em regras, desvios integrados e revisão concorrente de controle de qualidade encurta os ciclos de liberação e aumenta a prontidão para auditoria em comparação com processos intensivos em papel.
Por que a demanda por MES está crescendo em terapias celulares e gênicas?
A produção específica de pacientes requer cadeia de identidade e custódia rigorosas, orquestração especializada e integração com LIMS e serialização, que o MES pode unificar com trilhas de auditoria em conformidade.
Como os fornecedores estão ajudando a reduzir a complexidade e o custo dos programas de MES?
Os fornecedores oferecem serviços em nuvem validados, modelos pré-construídos e horas de consultoria para acelerar as implantações, mantendo a integridade dos dados e a disciplina de validação.
Página atualizada pela última vez em:



