Tamanho e Participação do Mercado de TIC de Saúde e Dispositivos Médicos
Análise do Mercado de TIC de Saúde e Dispositivos Médicos por Mordor Intelligence
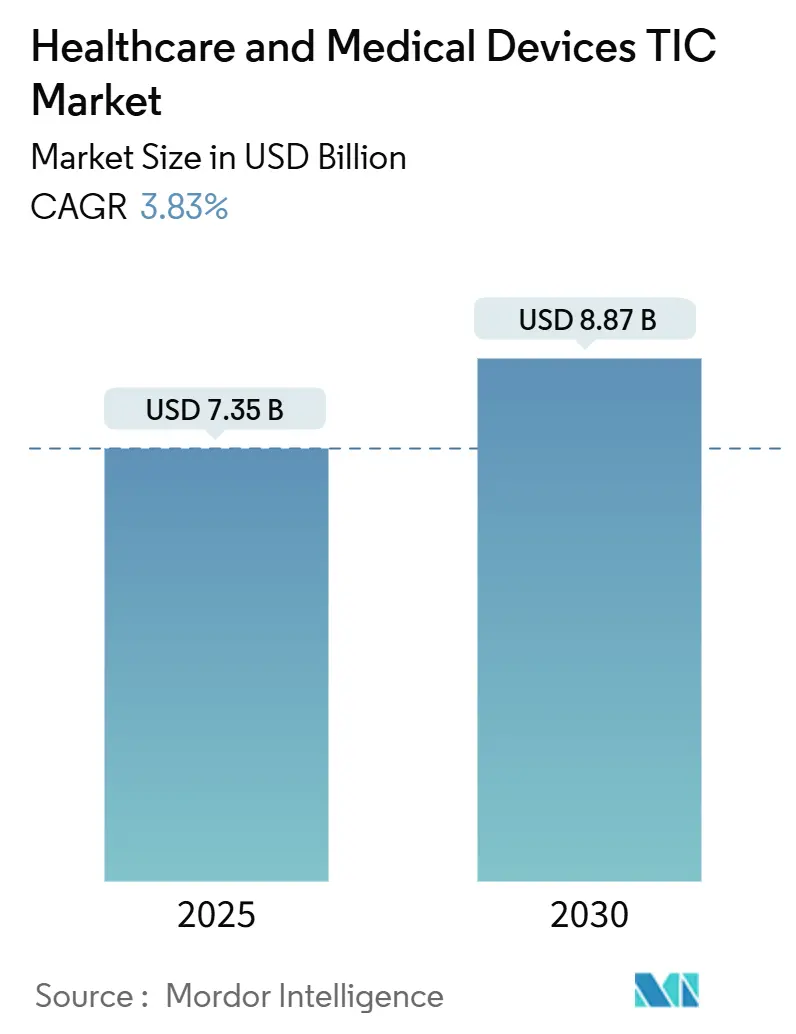
O mercado de teste, inspeção e certificação de saúde e dispositivos médicos está atualmente avaliado em USD 7,35 bilhões em 2025 e deve atingir USD 8,87 bilhões até 2030, refletindo um CAGR de 3,83% durante o período de previsão. Estruturas globais de conformidade obrigatória, crescente complexidade dos dispositivos e acelerada harmonização regulatória sustentam uma demanda estável mesmo com o aperto dos orçamentos de saúde. A concentração de manufatura na Ásia-Pacífico e a rápida evolução regulatória sustentam a dominância regional, enquanto recalls motivados por cibersegurança e diagnósticos habilitados por inteligência artificial ampliam o escopo de validação. Provedores consolidados de TIC aproveitam acreditações multijurisdicionais e automação laboratorial para manter poder de precificação frente a especialistas regionais fragmentados. A escassez acentuada de talentos, especialmente de auditores biomédicos, e os custos crescentes de modelos de biocompatibilidade moderam as perspectivas de crescimento, mas persistem oportunidades consideráveis de consolidação e especialização em nichos.
Principais Conclusões do Relatório
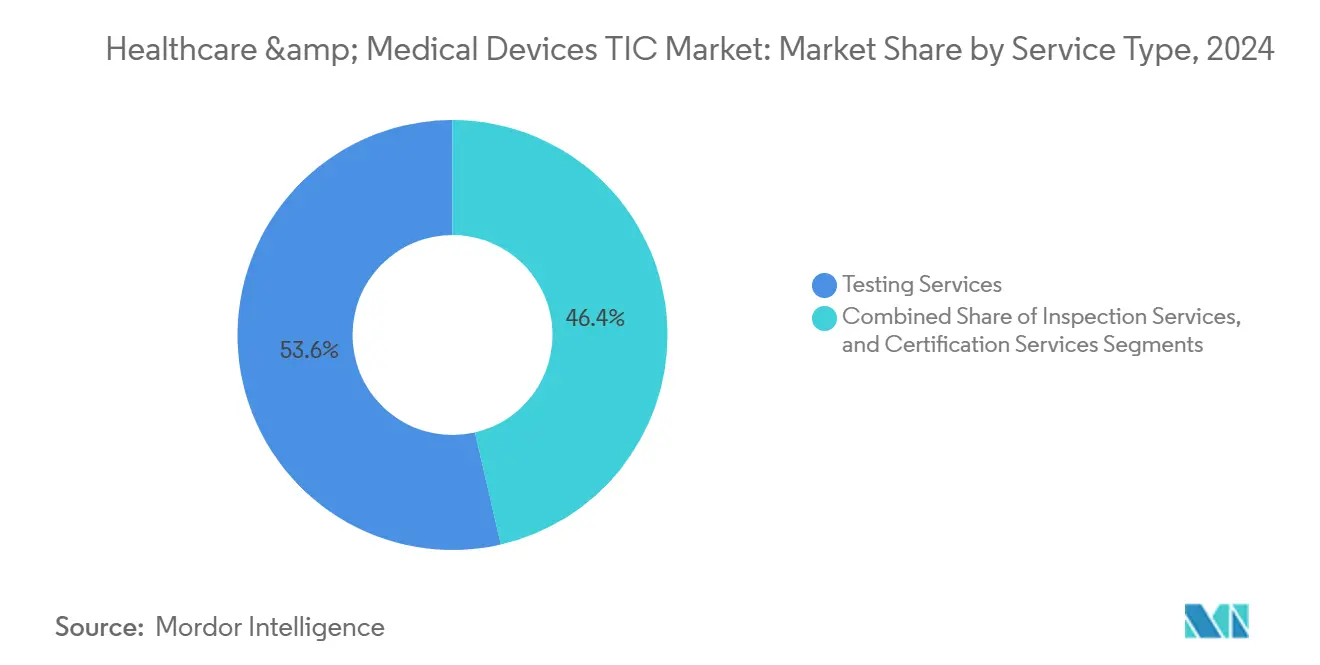
- Por tipo de serviço, os Serviços de Teste lideraram com 53,6% da participação do mercado de teste, inspeção e certificação de saúde e dispositivos médicos em 2024, enquanto os Serviços de Certificação avançam a um CAGR de 4,2% até 2030.
- Por tipo de fornecimento, os modelos Terceirizados responderam por 69,3% do tamanho do mercado de teste, inspeção e certificação de saúde e dispositivos médicos em 2024 e devem se expandir a um CAGR de 3,9% entre 2025-2030.
- Por geografia, a Ásia-Pacífico capturou 44,7% da participação de receita do mercado de teste, inspeção e certificação de saúde e dispositivos médicos em 2024; a região deve registrar o CAGR mais rápido de 4,5% até 2030.
Tendências e Perspectivas do Mercado Global de TIC de Saúde e Dispositivos Médicos
Análise de Impacto dos Impulsionadores
| Impulsionador | (~) % de Impacto na Previsão de CAGR | Relevância Geográfica | Prazo de Impacto |
|---|---|---|---|
| Aumento na complexidade e miniaturização dos dispositivos | +0.8% | Global, com concentração na América do Norte e na Ásia-Pacífico | Médio prazo (2-4 anos) |
| Expansão da harmonização regulatória global (MDSAP, IVDR) | +0.7% | Global, liderado pela América do Norte, pela UE e pela Ásia-Pacífico | Longo prazo (≥ 4 anos) |
| Crescimento de diagnósticos domiciliares e vestíveis | +0.6% | América do Norte e UE são primárias, Ásia-Pacífico está emergindo | Curto prazo (≤ 2 anos) |
| O aumento de recalls impulsiona os gastos com testes preventivos | +0.5% | Global, com maior impacto na América do Norte | Médio prazo (2-4 anos) |
| Protocolos de teste rápido habilitados por inteligência artificial | +0.4% | América do Norte e UE são de adoção antecipada, e a Ásia-Pacífico está seguindo. | Longo prazo (≥ 4 anos) |
| Demanda por testes de recondicionamento na economia circular | +0.3% | UE liderando, América do Norte com adoção seletiva | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Aumento na Complexidade e Miniaturização dos Dispositivos
Os dispositivos vestíveis agora combinam sensoriamento, conectividade e motores de inteligência artificial que exigem avaliação simultânea de precisão de sensores, eletromagnetismo, confiabilidade de software e segurança cutânea em diversas condições do mundo real. Os ciclos modernos de validação também devem verificar o aprendizado contínuo de algoritmos, levando os fabricantes a formar parcerias de teste recorrentes em vez de projetos episódicos.[1]FDA, "FDA Aprova Primeiro Dispositivo Médico Habilitado por Inteligência Artificial para Teste Domiciliar de Apneia do Sono," FDA.GOV Protocolos intensivos em talentos elevam os custos dos projetos, mas garantem receita previsível para os provedores de TIC que mantêm equipes multidisciplinares e ferramentas avançadas de simulação.
Expansão da Harmonização Regulatória Global (MDSAP, IVDR)
O framework MDSAP permite que uma única auditoria satisfaça cinco agências regulatórias, reduzindo os gastos de conformidade dos fabricantes em aproximadamente 30-40%, mas aumentando a demanda por empresas de TIC com reconhecimento simultâneo nos Estados Unidos, Canadá, Austrália, Japão e Brasil.[2]Health Canada, "Programa de Auditoria Única para Dispositivos Médicos," CANADA.CA A adoção do IVDR na Europa espelha essa tendência, ampliando as categorias de dispositivos sujeitos a testes rigorosos de desempenho diagnóstico e, assim, concentrando negócios com provedores globalmente acreditados.
Crescimento de Diagnósticos Domiciliares e Vestíveis
A FDA aprovou mais de 50 dispositivos de saúde digital para uso doméstico em 2024, incluindo monitores de apneia do sono e de glicose conectados a smartphones que exigem avaliações de cibersegurança, usabilidade e robustez em múltiplos ambientes, além dos testes clássicos de bancada. A economia do cuidado descentralizado incentiva os pagadores a reembolsar o monitoramento remoto, ampliando a receita para empresas de TIC que possuem laboratórios de simulação domiciliar e competências em testes de penetração de IoT.
Aumento de Recalls Impulsionando os Gastos com Testes Preventivos
Um salto de 400% nos recalls de dispositivos entre 2013-2018, impulsionado principalmente por vulnerabilidades de software e de rede, levou os fabricantes a aumentar os orçamentos de teste para 15-25% dos gastos de desenvolvimento, em comparação com os históricos 8-12%. A validação preventiva agora compensa os custos de recall, com média de USD 10-50 milhões, ancorando engajamentos mais robustos e em estágio inicial para especialistas em TIC.
Análise de Impacto das Restrições
| Restrição | (~) % de Impacto na Previsão de CAGR | Relevância Geográfica | Prazo de Impacto |
|---|---|---|---|
| Escassez de auditores de TIC biomédicos qualificados | -0.4% | Global, mais aguda na América do Norte e na UE | Curto prazo (≤ 2 anos) |
| Redução do financiamento de capital de risco em startups de tecnologia médica | -0.3% | Global, com maior impacto na América do Norte | Médio prazo (2-4 anos) |
| Riscos cibernéticos de integridade de dados em dispositivos conectados | -0.2% | Global, concentrado em mercados digitalmente avançados | Longo prazo (≥ 4 anos) |
| Custos crescentes para modelos animais de biocompatibilidade | -0.2% | Global, com a UE liderando a adoção de alternativas | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Escassez de Auditores de TIC Biomédicos Qualificados
O recrutamento de auditores especializados requer de 5 a 7 anos de treinamento multidisciplinar; as aposentadorias superam os novos talentos em aproximadamente dois para um, produzindo uma lacuna de pessoal de 25-30% e alimentando uma inflação salarial anual de 15-20%.[3]Departamento de Estatísticas do Trabalho, "Cientistas Médicos," BLS.GOV Os provedores estão automatizando a captura de dados e as avaliações remotas para mitigar gargalos, mas ainda não conseguem capitalizar a expansão de capacidade no curto prazo.
Redução do Financiamento de Capital de Risco em Startups de Tecnologia Médica
O investimento global em tecnologia médica caiu para USD 19,1 bilhões em 2024, ante o pico de USD 22,1 bilhões em 2021, reduzindo os pipelines de dispositivos em estágio inicial e adiando os contratos de TIC para marcos posteriores. As startups com restrições de caixa agora comprimem os escopos de validação, alterando o cronograma de receita para os fornecedores de TIC.
Análise de Segmentos
Por Tipo de Serviço: Serviços de Teste Mantêm a Primazia Enquanto as Certificações Aceleram
Os Serviços de Teste geraram a maior participação do mercado de teste, inspeção e certificação de saúde e dispositivos médicos, com 53,6% em 2024, impulsionados pelas avaliações de materiais da ISO 10993 e pelas verificações obrigatórias de compatibilidade eletromagnética. A amplitude do segmento abrange protocolos de biocompatibilidade, segurança elétrica e cibersegurança, cada um escalando com a conectividade dos dispositivos e a adoção de inteligência artificial. Embora o crescimento se modere à medida que alguns testes se consolidam sob frameworks harmonizados, a crescente complexidade do design sustenta o volume e a resiliência das margens.
Os Serviços de Certificação, embora representem uma parcela menor do tamanho do mercado de teste, inspeção e certificação de saúde e dispositivos médicos, registraram o CAGR mais rápido de 4,2%. Os fabricantes investem cada vez mais em certificações de fonte única que satisfazem o MDSAP e o IVDR simultaneamente, trocando taxas iniciais por lançamentos globais mais rápidos. Os Serviços de Inspeção, com aproximadamente um quarto da receita, se beneficiam dos mandatos de transparência da cadeia de suprimentos, mas se expandem mais lentamente à medida que as auditorias remotas ganham força.
Efeitos de segunda ordem reforçam a interação entre segmentos: certificações avançadas frequentemente agrupam testes pré-requisitos, e auditorias bem-sucedidas alimentam inspeções de vigilância recorrentes. Os provedores de TIC que integram as três ofertas em plataformas em nuvem monetizam ciclos de vida de conformidade de ponta a ponta, atraindo tanto multinacionais quanto inovadores com recursos limitados.


Por Tipo de Fornecimento: A Terceirização Continua a Superar os Modelos Internos
A terceirização comandou 69,3% da participação do mercado de teste, inspeção e certificação de saúde e dispositivos médicos em 2024 e está registrando um CAGR de 3,9% até 2030. Os crescentes desembolsos de capital para câmaras especializadas, salas limpas e laboratórios de cibersegurança — frequentemente de USD 10-50 milhões por instalação — tornam as parcerias externas economicamente vantajosas para startups e até mesmo para grandes fabricantes de equipamentos originais que buscam capacidade adicional.
As capacidades internas, embora estratégicas para as linhas de produtos principais, enfrentam restrições de talentos e rápida obsolescência à medida que os padrões evoluem. Algumas multinacionais agora operam modelos híbridos nos quais testes críticos de software ou de materiais proprietários permanecem internos, enquanto laboratórios terceirizados lidam com coexistência sem fio, viés de inteligência artificial e certificações internacionais de nicho. A dinâmica incentiva os fornecedores de TIC a se instalarem próximos aos principais clusters de manufatura, oferecendo infraestrutura compartilhada e portais de dados em tempo real que se integram aos ciclos de design dos fabricantes de equipamentos originais.
Análise Geográfica
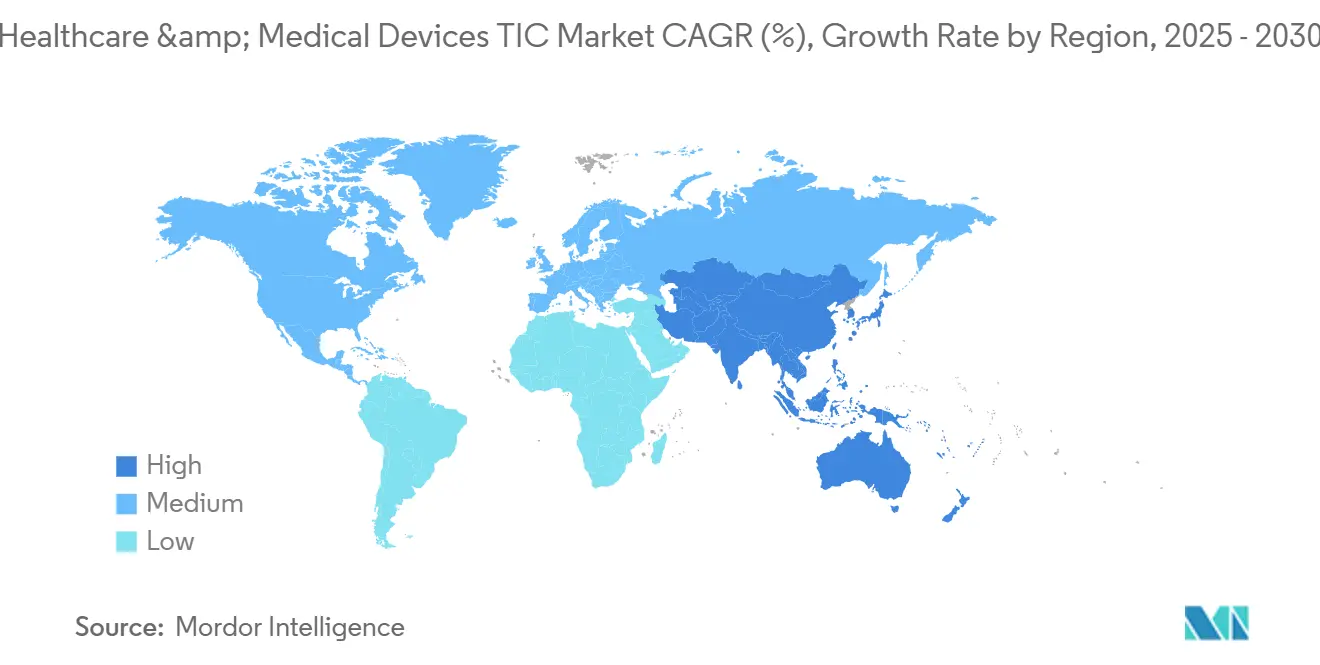
A Ásia-Pacífico capturou 44,7% da receita global em 2024 e deve registrar um CAGR de 4,5% até 2030, tornando a região o motor de crescimento do mercado de teste, inspeção e certificação de dispositivos médicos. As reformas da Administração Nacional de Produtos Médicos (NMPA) da China sincronizam as regras domésticas com os padrões ISO e IEC, ao mesmo tempo em que exigem relatórios de teste locais, consolidando a demanda por laboratórios internacionalmente acreditados.[4]Administração Nacional de Produtos Médicos, "Atualizações Regulatórias," NMPA.GOV.CN O Japão e a Coreia do Sul adicionam necessidades premium de validação de cibersegurança e inteligência artificial, enquanto o Sudeste Asiático ganha força para ensaios de rotina com boa relação custo-benefício sob a harmonização da ASEAN.
A América do Norte detinha 28% de participação de mercado em 2024 e deve se expandir moderadamente a um CAGR de 3,2%. Os Estados Unidos lideram com projetos de alta margem em avaliações de risco de dispositivos conectados, à medida que a FDA examina as divulgações de listas de materiais de software. A participação do Canadá no MDSAP sustenta sinergias de auditoria transfronteiriça, enquanto os laboratórios de menor custo do México atraem segmentos de teste de commodities para cadeias de suprimentos regionais.
A Europa respondeu por 22% da receita de 2024, à medida que o MDR e o IVDR transformaram as autocertificações legadas em engajamentos formais de TIC. A Alemanha e o Reino Unido dominam o volume, com certificações duplas UE-Reino Unido abrindo oportunidades incrementais no pós-Brexit. As regulamentações de economia circular catalisam nichos de teste de recondicionamento e ciclo de vida, e o GDPR impulsiona maior escrutínio sobre a integridade dos dados dos pacientes.


Cenário Competitivo
A liderança global permanece dispersa, posicionando o setor de teste, inspeção e certificação de dispositivos médicos em um nível moderadamente concentrado. SGS, Intertek, TÜV SÜD e Bureau Veritas aproveitam mais de 1.000 reconhecimentos governamentais e extensas redes de laboratórios para se diferenciar dos especialistas regionais. A recente aprovação da SGS em Xangai com zero observações do Formulário 483 da FDA exemplifica a profundidade de credenciais que garante prêmios de precificação.
A transformação digital sustenta as vantagens competitivas. A automação FlexLab X da Siemens Healthineers e os conjuntos de robótica da Merck ilustram a mudança em direção ao processamento impulsionado por inteligência artificial, mitigando a escassez de auditores e elevando a fidelidade dos dados. A validação de cibersegurança, as auditorias de viés de algoritmos e a validação de dispositivos recondicionados constituem espaços lucrativos onde especialistas menores podem escalar rapidamente ou se tornar alvos de aquisição, como demonstrado pela compra de USD 405 milhões pela Mérieux NutriSciences do negócio de testes de alimentos da Bureau Veritas para dobrar a presença na Ásia-Pacífico.
Espera-se que o impulso de fusões e aquisições continue, impulsionado pelo interesse de capital privado e por movimentos sinérgicos entre setores que combinam portfólios ambientais, farmacêuticos e de tecnologia médica para a conveniência do usuário final. A precificação permanece resiliente dada a escassez de acreditações e os altos custos de troca, mas a inflação salarial e os investimentos em tecnologia regulatória comprimem as margens para empresas sem escala ou roteiros de automação.
Líderes do Setor de TIC de Saúde e Dispositivos Médicos
SGS SA
Bureau Veritas SA
Intertek Group plc
TÜV SÜD AG
TÜV Rheinland AG
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica


Desenvolvimentos Recentes do Setor
- Março de 2025: A Merck lançou soluções de automação laboratorial e robótica para controle de qualidade farmacêutica, em parceria com empresas de engenharia para fornecer sistemas integrados de testes microbiológicos.
- Fevereiro de 2025: A GN Store Nord reportou gastos em P&D de DKK 1,9 bilhão, enfatizando frameworks centralizados de qualidade e segurança de produtos para dispositivos auditivos habilitados por inteligência artificial (USD 0,29 bilhão).
- Janeiro de 2025: A Eurofins Scientific adquiriu a SF Analytical Laboratories, expandindo o alcance de testes ambientais e de alimentos nos Estados Unidos.
- Outubro de 2024: A Mérieux NutriSciences concordou em adquirir a divisão de testes de alimentos da Bureau Veritas por EUR 360 milhões (USD 405 milhões).
Escopo do Relatório Global do Mercado de TIC de Saúde e Dispositivos Médicos
| Serviços de Teste |
| Serviços de Inspeção |
| Serviços de Certificação |
| Interno |
| Terceirizado |
| América do Norte | Estados Unidos | |
| Canadá | ||
| México | ||
| América do Sul | Brasil | |
| Argentina | ||
| Restante da América do Sul | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Rússia | ||
| Restante da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Coreia do Sul | ||
| Sudeste Asiático | ||
| Restante da Ásia-Pacífico | ||
| Oriente Médio e África | Oriente Médio | Arábia Saudita |
| Emirados Árabes Unidos | ||
| Turquia | ||
| Restante do Oriente Médio | ||
| África | África do Sul | |
| Nigéria | ||
| Restante da África | ||
| Por Tipo de Serviço | Serviços de Teste | ||
| Serviços de Inspeção | |||
| Serviços de Certificação | |||
| Por Tipo de Fornecimento | Interno | ||
| Terceirizado | |||
| Por Geografia | América do Norte | Estados Unidos | |
| Canadá | |||
| México | |||
| América do Sul | Brasil | ||
| Argentina | |||
| Restante da América do Sul | |||
| Europa | Alemanha | ||
| Reino Unido | |||
| França | |||
| Itália | |||
| Espanha | |||
| Rússia | |||
| Restante da Europa | |||
| Ásia-Pacífico | China | ||
| Japão | |||
| Índia | |||
| Coreia do Sul | |||
| Sudeste Asiático | |||
| Restante da Ásia-Pacífico | |||
| Oriente Médio e África | Oriente Médio | Arábia Saudita | |
| Emirados Árabes Unidos | |||
| Turquia | |||
| Restante do Oriente Médio | |||
| África | África do Sul | ||
| Nigéria | |||
| Restante da África | |||


Principais Questões Respondidas no Relatório
Qual é o tamanho atual do mercado global de teste, inspeção e certificação de saúde e dispositivos médicos?
O mercado está em USD 7,35 bilhões em 2025 e deve atingir USD 8,87 bilhões até 2030.
Qual região contribui com a maior receita para os serviços de conformidade de dispositivos médicos?
A Ásia-Pacífico lidera com 44,7% da receita global, impulsionada pela escala de manufatura e pela maturidade regulatória.
Por que os serviços de certificação estão crescendo mais rapidamente do que os serviços de teste?
Frameworks harmonizados como o MDSAP e o IVDR permitem que um único certificado abra múltiplos mercados, tornando a certificação por terceiros mais valiosa.
Qual é o principal desafio que limita o crescimento de capacidade no curto prazo para os provedores de TIC?
Uma escassez de 25-30% de auditores biomédicos qualificados está restringindo a expansão dos serviços apesar da crescente demanda.
Como a terceirização se compara aos testes internos?
A terceirização controla 69,3% do gasto total porque laboratórios especializados reduzem os desembolsos de capital e aceleram as aprovações em múltiplos países.
Quais nichos emergentes oferecem o maior potencial de crescimento para as empresas de TIC?
As áreas de alta margem incluem validação de cibersegurança para dispositivos conectados, auditorias de viés de algoritmos de inteligência artificial e testes de recondicionamento na economia circular.
Página atualizada pela última vez em:









