ヘルスケア・医療機器TIC市場規模とシェア
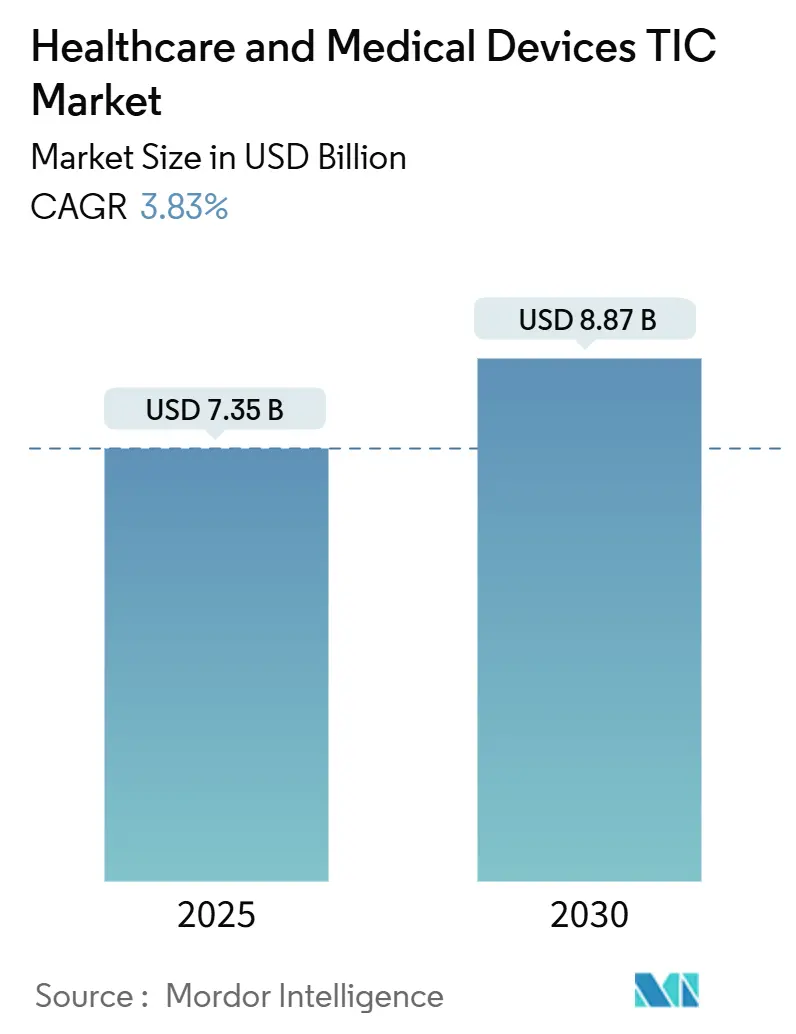
Mordor Intelligenceによるヘルスケア・医療機器TIC市場分析
ヘルスケア・医療機器の試験、検査、認証市場は2025年現在73億5,000万米ドルと評価されており、予測期間中に3.83%のCAGRを反映して2030年までに88億7,000万米ドルに達すると予測されています。世界的な強制コンプライアンスの枠組み、機器の複雑性の高まり、規制の調和加速が、ヘルスケア予算が逼迫する中でも安定した需要を支えています。アジア太平洋地域の製造集中と急速な規制の進化が地域的優位性を支え、サイバーセキュリティ主導のリコールとAI対応診断が検証範囲を拡大しています。確立されたTICプロバイダーは、複数法域の認定と実験室の自動化を活用して、分散した地域専門業者に対する価格決定力を維持しています。特に生物医学監査員の深刻な人材不足と生体適合性モデルコストの上昇が成長見通しを抑制していますが、大規模な統合とニッチ専門化の機会は依然として存在しています。
主要レポートのポイント
- サービスタイプ別では、試験サービスが2024年のヘルスケア・医療機器の試験、検査、認証市場シェアの53.6%をリードし、認証サービスは2030年にかけて4.2%のCAGRで拡大しています。
- 調達タイプ別では、外部委託モデルが2024年のヘルスケア・医療機器の試験、検査、認証市場規模の69.3%を占め、2025年~2030年にかけて3.9%のCAGRで拡大する見込みです。
- 地域別では、アジア太平洋地域が2024年のヘルスケア・医療機器の試験、検査、認証市場において44.7%の収益シェアを獲得しており、同地域は2030年にかけて最速の4.5%のCAGRを記録すると予測されています。
世界のヘルスケア・医療機器TIC市場のトレンドと洞察
促進要因の影響分析
| 促進要因 | (~)CAGR予測への影響(%) | 地理的関連性 | 影響の時間軸 |
|---|---|---|---|
| 機器の複雑性と小型化の急増 | +0.8% | 北米とアジア太平洋地域に集中した世界規模 | 中期(2~4年) |
| 世界的な規制調和の拡大(MDSAP、IVDR) | +0.7% | 北米、EU、アジア太平洋地域が主導する世界規模での採用 | 長期(4年以上) |
| 在宅医療とウェアラブル診断の成長 | +0.6% | 北米とEUが主要市場、アジア太平洋地域は新興 | 短期(2年以内) |
| リコール増加が予防的試験支出を促進 | +0.5% | 北米で最も高い影響を持つ世界規模 | 中期(2~4年) |
| AI対応の迅速な試験プロトコル | +0.4% | 北米とEUが早期採用、アジア太平洋地域が追随 | 長期(4年以上) |
| 循環経済の改修試験需要 | +0.3% | EUが主導、北米は選択的採用 | 長期(4年以上) |
| 情報源: Mordor Intelligence | |||
機器の複雑性と小型化の急増
ウェアラブルは現在、センシング、接続性、AIエンジンを組み合わせており、多様な実世界の条件下でセンサー精度、電磁気学、ソフトウェア信頼性、皮膚安全性の同時評価が求められます。現代の検証サイクルは継続的なアルゴリズム学習の検証も必要とし、製造業者は単発プロジェクトではなく継続的な試験パートナーシップを形成するようになっています。[1]FDA、「FDAが在宅睡眠時無呼吸症候群検査用の初のAI対応医療機器を認可」、FDA.GOV人材集約型のプロトコルはプロジェクトコストを引き上げますが、多分野にわたる試験台と高度なシミュレーションツールを維持するTICプロバイダーには予測可能な収益をもたらします。
世界的な規制調和の拡大(MDSAP、IVDR)
MDSAPの枠組みにより、1回の監査で5つの規制機関の要件を満たすことができ、製造業者のコンプライアンス支出を約30~40%削減できますが、米国、カナダ、オーストラリア、日本、ブラジルの同時認定を持つTIC企業への需要が高まっています。[2]カナダ保健省、「医療機器単一監査プログラム」、CANADA.CA欧州でのIVDR採用もこのトレンドを反映しており、厳格な診断性能試験の対象となる機器カテゴリーを拡大し、世界的に認定されたプロバイダーへの事業集中を促しています。
在宅医療とウェアラブル診断の成長
FDAは2024年に50台以上のデジタルヘルス機器を家庭用として認可しました。これにはスマートフォン連携の睡眠時無呼吸症候群モニターやグルコースモニターが含まれており、従来のベンチ試験を超えたサイバーセキュリティ、使いやすさ、多環境堅牢性の評価が必要です。分散型ケアの経済性により、支払者がリモートモニタリングの償還を促進し、在宅シミュレーションラボとIoT侵入試験のスキルセットを持つTIC企業の収益が拡大しています。
リコール増加が予防的試験支出を促進
2013年から2018年にかけてのデバイスリコールの400%増加は、主にソフトウェアとネットワークの脆弱性によって引き起こされ、製造業者は試験予算を開発費の15~25%に引き上げました(従来の8~12%から増加)。予防的検証は現在、平均1,000万~5,000万米ドルのリコールコストを相殺し、TIC専門業者にとってより堅固な初期段階のエンゲージメントを確保しています。
抑制要因の影響分析
| 抑制要因 | (~)CAGR予測への影響(%) | 地理的関連性 | 影響の時間軸 |
|---|---|---|---|
| 資格を持つ生物医学TIC監査員の不足 | -0.4% | 北米とEUで最も深刻な世界規模 | 短期(2年以内) |
| 医療技術スタートアップへのVC資金の縮小 | -0.3% | 北米で最も高い影響を持つ世界規模 | 中期(2~4年) |
| 接続機器におけるデータ整合性のサイバーリスク | -0.2% | デジタル先進市場に集中した世界規模 | 長期(4年以上) |
| 生体適合性動物モデルのコスト上昇 | -0.2% | EUが代替手段の採用を主導する世界規模 | 中期(2~4年) |
| 情報源: Mordor Intelligence | |||
資格を持つ生物医学TIC監査員の不足
専門的な監査員の採用には5~7年の学際的なトレーニングが必要であり、退職者数が新規人材の約2倍のペースで増加しており、25~30%の人員不足が生じ、年間15~20%の賃金インフレを引き起こしています。[3]労働統計局、「医学研究者」、BLS.GOVプロバイダーはボトルネックを緩和するためにデータ収集とリモート評価の自動化を進めていますが、短期的な能力拡大を十分に活用することはできていません。
医療技術スタートアップへのVC資金の縮小
世界の医療技術投資は2021年のピーク時の221億米ドルから2024年には191億米ドルに減少し、初期段階の機器パイプラインが縮小し、TIC契約が後のマイルストーンまで遅延しています。資金制約のあるスタートアップは現在、検証範囲を縮小しており、TICベンダーの収益タイミングをシフトさせています。
セグメント分析
サービスタイプ別:試験サービスが優位を維持しながら認証が加速
試験サービスは2024年のヘルスケア・医療機器の試験、検査、認証市場において53.6%の最大シェアを生み出し、ISO 10993材料評価と必須の電磁適合性チェックによって推進されました。このセグメントの範囲は生体適合性、電気安全性、サイバーセキュリティプロトコルにわたり、それぞれが機器の接続性とAI採用とともに拡大しています。一部の試験が調和された枠組みの下で統合されるにつれて成長は緩やかになりますが、設計の複雑性の高まりが量とマージンの回復力を維持しています。
認証サービスは、ヘルスケア・医療機器の試験、検査、認証市場規模においてより小さな部分を占めていますが、最速の4.2%のCAGRを記録しました。製造業者はMDSAPとIVDRを同時に満たす単一ソース認証への投資を増やし、前払い費用と引き換えにより迅速なグローバル展開を実現しています。収益の約4分の1を占める検査サービスは、サプライチェーンの透明性義務から恩恵を受けていますが、リモート監査が普及するにつれてより緩やかに拡大しています。
二次的な効果がセグメントの相互作用を強化しています。高度な認証は前提条件となる試験をバンドルすることが多く、成功した監査は定期的な監視検査につながります。クラウドプラットフォーム全体で3つのサービスすべてを統合するTICプロバイダーは、エンドツーエンドのコンプライアンスライフサイクルを収益化し、多国籍企業とリソースに制約のある革新者の両方を引き付けています。
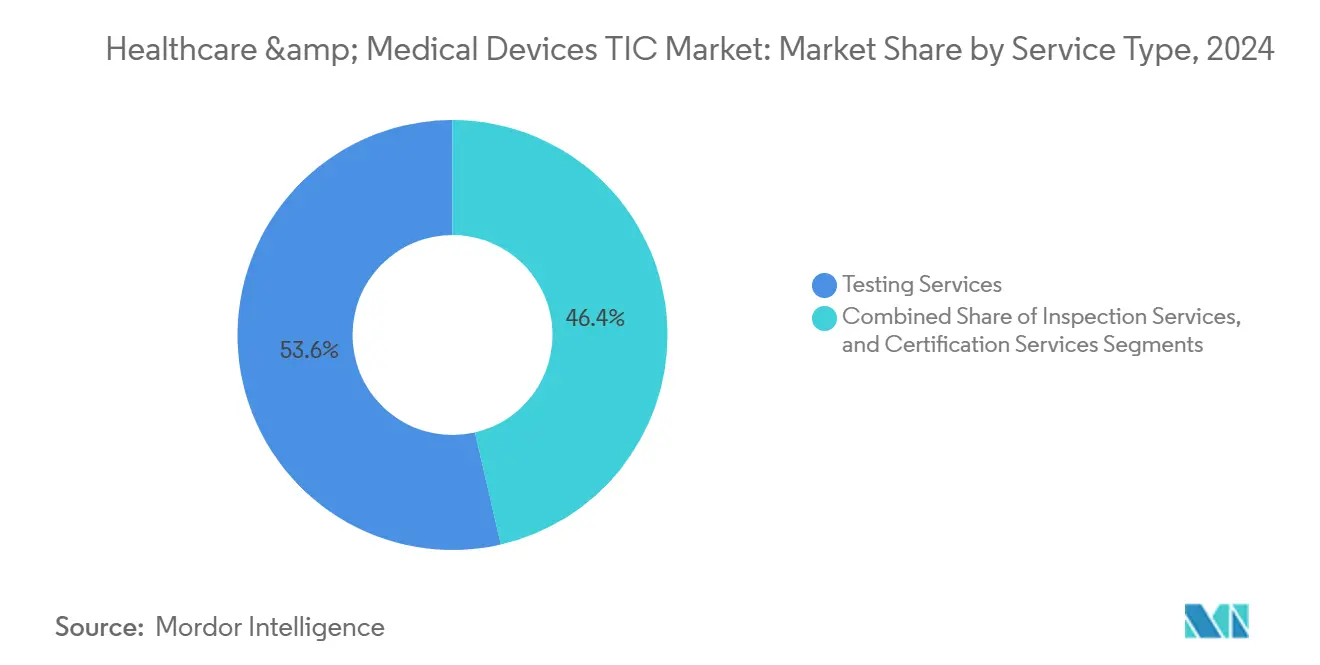
注記: 個別セグメントのセグメントシェアはレポート購入時に入手可能


調達タイプ別:外部委託が社内モデルを上回り続ける
外部委託は2024年のヘルスケア・医療機器の試験、検査、認証市場シェアの69.3%を占め、2030年にかけて3.9%のCAGRを追跡しています。専門的なチャンバー、クリーンルーム、サイバーセキュリティラボへの資本支出の増大(施設あたり多くの場合1,000万~5,000万米ドル)により、スタートアップや急増する能力を求める大手OEMにとっても外部パートナーシップが経済的に合理的となっています。
社内能力は、コア製品ラインにとって戦略的ではありますが、人材制約と標準の進化に伴う急速な陳腐化に直面しています。一部の多国籍企業は現在、重要なソフトウェアや独自材料の試験をオンプレミスに維持しながら、無線共存、AIバイアス、国際的なニッチ認証をサードパーティラボに委託するハイブリッドモデルを採用しています。このダイナミクスにより、TICベンダーは主要な製造クラスターの近くに共同設置し、OEMの設計サイクルと連携した共有インフラとリアルタイムデータポータルを提供するよう促されています。
地域分析
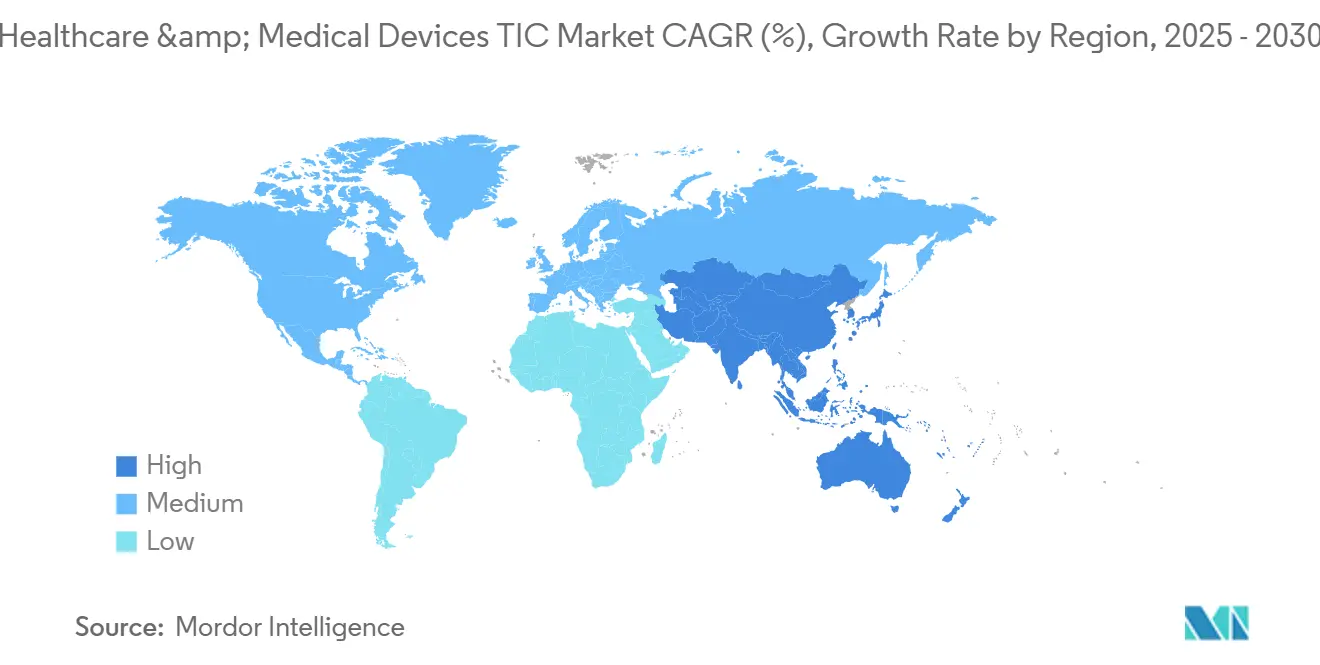
アジア太平洋地域は2024年に世界収益の44.7%を獲得し、2030年にかけて4.5%のCAGRを記録すると予測されており、医療機器の試験、検査、認証市場の成長エンジンとなっています。中国の国家薬品監督管理局(NMPA)の改革は国内規則をISOおよびIEC標準と同期させながら現地試験報告書を義務付け、国際的に認定されたラボへの需要を確固たるものにしています。[4]国家薬品監督管理局、「規制の最新情報」、NMPA.GOV.CN日本と韓国はプレミアムなサイバーセキュリティとAI検証ニーズを加え、東南アジアはASEAN調和の下でコスト効率の高い定常的なアッセイの拠点として台頭しています。
北米は2024年に28%の市場シェアを保持し、3.2%のCAGRで緩やかに拡大すると予測されています。米国は、FDAがソフトウェア部品表の開示を精査する中、接続機器のリスク評価における高マージンプロジェクトで主導しています。カナダのMDSAP参加は国境を越えた監査の相乗効果を維持し、メキシコの低コストラボは地域サプライチェーンの汎用試験セグメントを引き付けています。
欧州はMDRとIVDRが従来の自己認証を正式なTICエンゲージメントに転換したことで、2024年収益の22%を占めました。ドイツと英国が量を支配しており、EU・英国の二重認証がブレグジット後の追加的な機会を開いています。循環経済規制が改修とライフサイクル試験のニッチを触媒し、GDPRが患者データの整合性に対する追加的な精査を促しています。


競合環境
世界的なリーダーシップは分散しており、医療機器の試験、検査、認証産業は中程度に集中した層に位置しています。SGS、Intertek、TÜV SÜD、Bureau Veritasは1,000以上の政府認定と広範なラボネットワークを活用して、地域専門業者との差別化を図っています。SGS上海が米国食品医薬品局フォーム483の指摘事項ゼロで認可を受けた最近の事例は、価格プレミアムを生み出す資格の深さを示しています。
デジタルトランスフォーメーションが競争上の優位性を支えています。シーメンス・ヘルシニアーズのFlexLab X自動化とメルクのロボティクスシステムは、AI駆動のスループットへの転換を示しており、監査員不足を緩和しデータの忠実度を高めています。サイバーセキュリティ、アルゴリズムバイアス監査、改修機器の検証は、小規模な専門業者が急速に規模を拡大するか買収対象となる可能性のある有望なホワイトスペースを構成しており、Mérieux NutriSciencesがBureau Veritasの食品試験事業を4億500万米ドルで買収してアジア太平洋地域のプレゼンスを倍増させた事例がこれを示しています。
M&Aの勢いは、プライベートエクイティの関心と、エンドユーザーの利便性のために環境、製薬、医療技術ポートフォリオを融合させる相乗的なクロスセクタープレイに支えられて継続すると予想されます。認定の希少性と高い切り替えコストにより価格は回復力を維持していますが、賃金インフレと規制技術への投資が規模や自動化ロードマップを持たない企業のマージンを圧迫しています。
ヘルスケア・医療機器TIC産業リーダー
SGS SA
Bureau Veritas SA
Intertek Group plc
TÜV SÜD AG
TÜV Rheinland AG
- *免責事項:主要選手の並び順不同


最近の業界動向
- 2025年3月:メルクは製薬品質管理向けの実験室自動化・ロボティクスソリューションを発売し、エンジニアリング企業と提携して統合された微生物試験システムを提供しました。
- 2025年2月:GN Store Nordは研究開発費として19億デンマーク・クローネを報告し、AI対応補聴器の集中型品質・製品セキュリティフレームワークを強調しました(2億9,000万米ドル)。
- 2025年1月:Eurofins ScientificがSF Analytical Laboratoriesを買収し、米国の環境・食品試験の範囲を拡大しました。
- 2024年10月:Mérieux NutriSciencesがBureau Veritasの食品試験部門を3億6,000万ユーロ(4億500万米ドル)で買収することに合意しました。
世界のヘルスケア・医療機器TIC市場レポートの範囲
| 試験サービス |
| 検査サービス |
| 認証サービス |
| 社内 |
| 外部委託 |
| 北米 | 米国 | |
| カナダ | ||
| メキシコ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他の南米 | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| ロシア | ||
| その他の欧州 | ||
| アジア太平洋 | 中国 | |
| 日本 | ||
| インド | ||
| 韓国 | ||
| 東南アジア | ||
| その他のアジア太平洋 | ||
| 中東・アフリカ | 中東 | サウジアラビア |
| アラブ首長国連邦 | ||
| トルコ | ||
| その他の中東 | ||
| アフリカ | 南アフリカ | |
| ナイジェリア | ||
| その他のアフリカ | ||
| サービスタイプ別 | 試験サービス | ||
| 検査サービス | |||
| 認証サービス | |||
| 調達タイプ別 | 社内 | ||
| 外部委託 | |||
| 地域別 | 北米 | 米国 | |
| カナダ | |||
| メキシコ | |||
| 南米 | ブラジル | ||
| アルゼンチン | |||
| その他の南米 | |||
| 欧州 | ドイツ | ||
| 英国 | |||
| フランス | |||
| イタリア | |||
| スペイン | |||
| ロシア | |||
| その他の欧州 | |||
| アジア太平洋 | 中国 | ||
| 日本 | |||
| インド | |||
| 韓国 | |||
| 東南アジア | |||
| その他のアジア太平洋 | |||
| 中東・アフリカ | 中東 | サウジアラビア | |
| アラブ首長国連邦 | |||
| トルコ | |||
| その他の中東 | |||
| アフリカ | 南アフリカ | ||
| ナイジェリア | |||
| その他のアフリカ | |||


レポートで回答される主要な質問
世界のヘルスケア・医療機器の試験、検査、認証市場の現在の規模はどのくらいですか?
市場は2025年に73億5,000万米ドルに達しており、2030年までに88億7,000万米ドルに達すると予測されています。
医療機器コンプライアンスサービスに最も多くの収益をもたらしている地域はどこですか?
アジア太平洋地域が世界収益の44.7%をリードしており、製造規模と規制の成熟度によって牽引されています。
認証サービスが試験サービスよりも速く成長しているのはなぜですか?
MDSAPやIVDRなどの調和された枠組みにより、1つの認証で複数の市場を開拓できるため、サードパーティ認証の価値が高まっています。
TICプロバイダーの短期的な能力成長を制限する主な課題は何ですか?
資格を持つ生物医学監査員の25~30%の不足が、需要の高まりにもかかわらずサービス拡大を制約しています。
外部委託と社内試験はどのように比較されますか?
外部委託は総支出の69.3%を占めており、専門ラボが資本支出を削減し複数国の承認を加速させるためです。
TIC企業にとって最大の上昇余地を提供する新興ニッチはどれですか?
高マージン分野には、接続機器のサイバーセキュリティ検証、AIアルゴリズムバイアス監査、循環経済の改修試験が含まれます。
最終更新日:








