Taille et part du marché des kits de tests diagnostiques pour naissance prématurée
Analyse du marché des kits de tests diagnostiques pour naissance prématurée par Mordor Intelligence
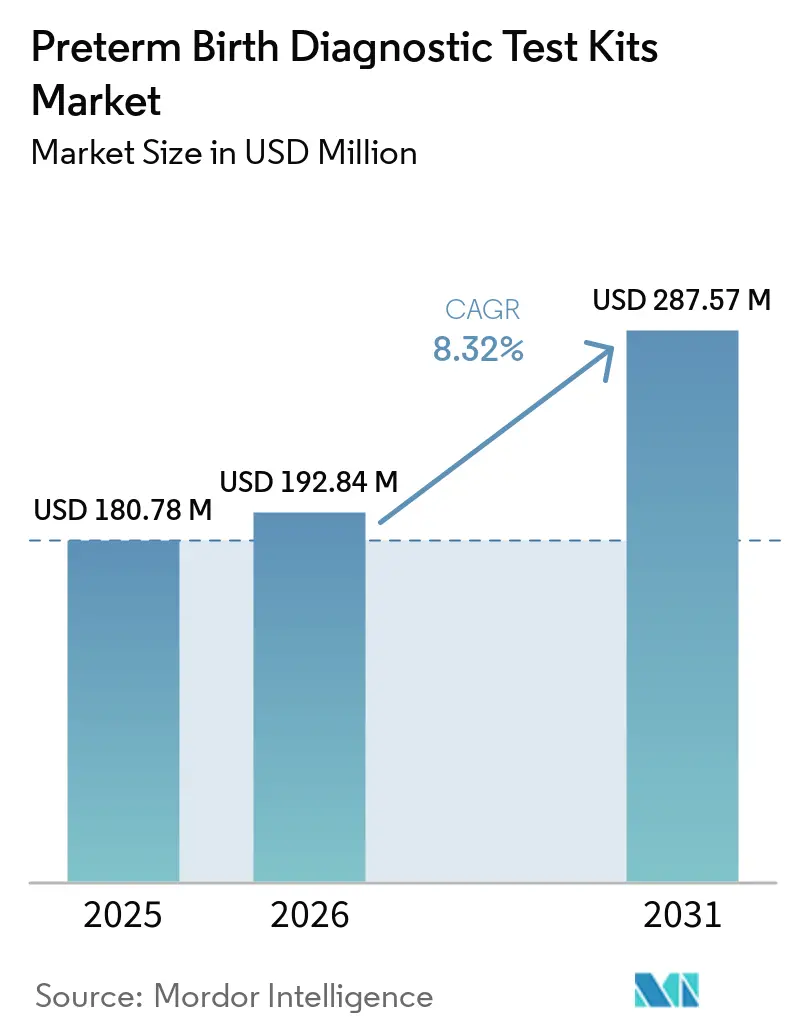
La taille du marché des kits de tests diagnostiques pour naissance prématurée est projetée à 180,78 millions USD en 2025, 192,84 millions USD en 2026, et devrait atteindre 287,57 millions USD d'ici 2031, avec un CAGR de 8,32 % de 2026 à 2031.
La croissance reflète un passage du triage symptomatique à une stratification précoce du risque, les équipes cliniques combinant les tests de biomarqueurs avec l'échographie de longueur cervicale pour réduire les admissions et interventions évitables. L'arrêt des cassettes quantitatives de fibronectine fœtale a perturbé les pratiques hospitalières établies et redirigé les achats vers des biomarqueurs alternatifs et des plateformes binaires d'exclusion. Les tests par écouvillon basés sur le PAMG-1 et l'IGFBP-1, ainsi que les diagnostics de rupture des membranes, continuent d'ancrer les décisions rapides dans les unités de travail où chaque minute compte pour le congé ou le transfert. Les données probantes de 2026 ont renforcé la valeur du dépistage protéomique sanguin, une grande étude randomisée montrant de meilleurs résultats lorsqu'une stratégie de prévention basée sur le PreTRM était appliquée dans les grossesses à faible risque. La dynamique régionale favorise l'échelle et l'engagement des payeurs, l'Amérique du Nord conservant le leadership en termes de part tandis que l'Asie-Pacifique se développe plus rapidement grâce à la construction de laboratoires et aux projets pilotes de remboursement.
Principaux enseignements du rapport
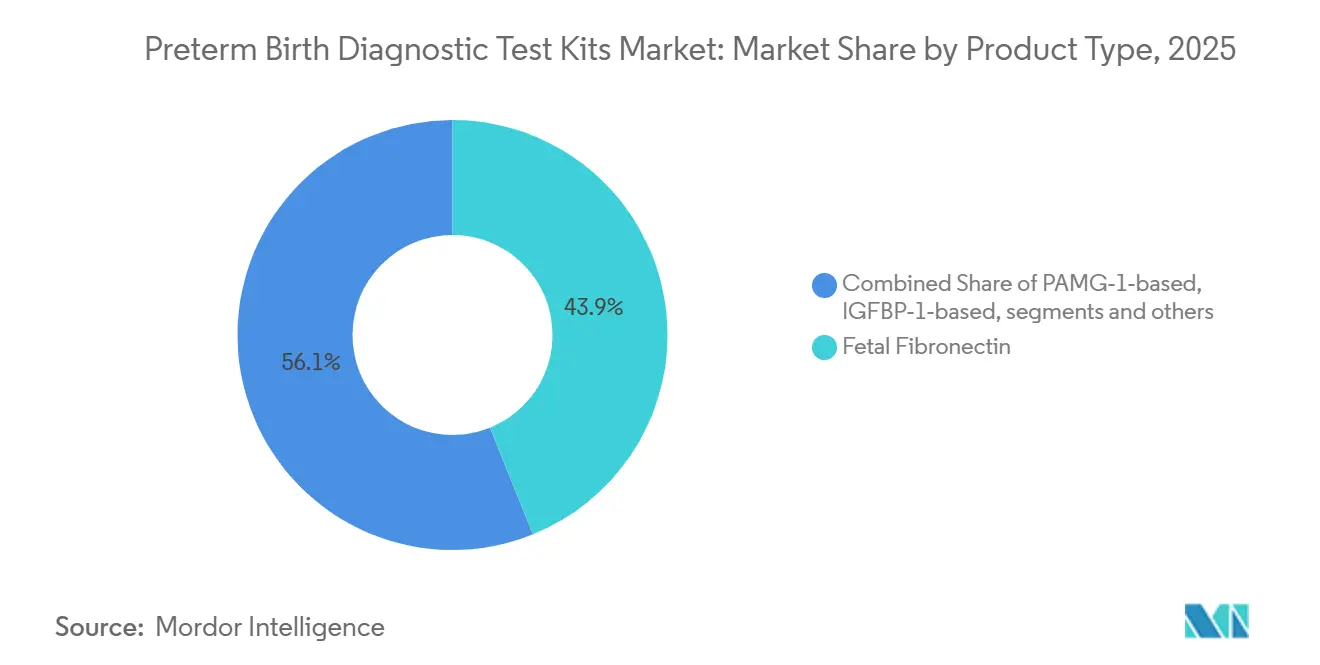
- Par type de produit, la fibronectine fœtale a dominé avec une part de revenus de 43,89 % en 2025, tandis que les plateformes PAMG-1 devraient enregistrer la croissance la plus rapide avec un CAGR de 9,67 % jusqu'en 2031.
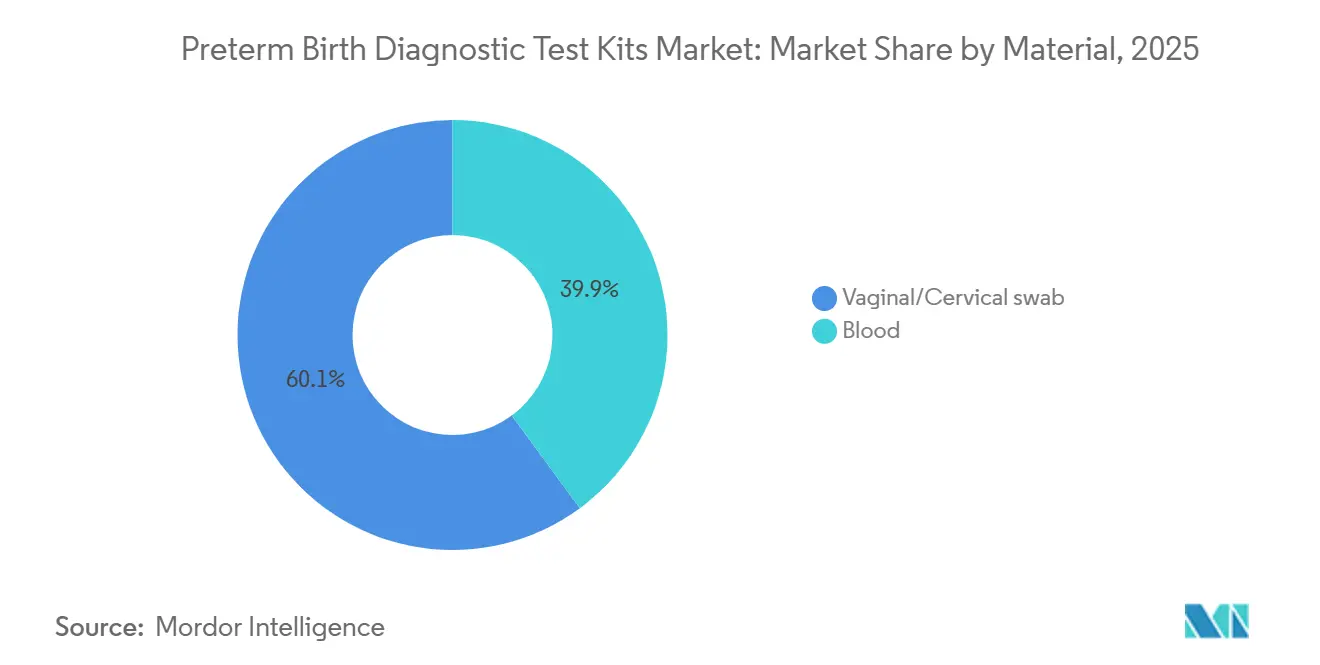
- Par matériau, les écouvillons vaginaux-cervicaux représentaient 60,10 % des revenus de 2025 et les dosages protéomiques sanguins progressent à un CAGR de 9,01 % jusqu'en 2031.
- Par utilisateur final, les hôpitaux et maternités détenaient 58,56 % de la demande de 2025 et les laboratoires de diagnostic affichaient la croissance projetée la plus élevée avec un CAGR de 10,34 %.
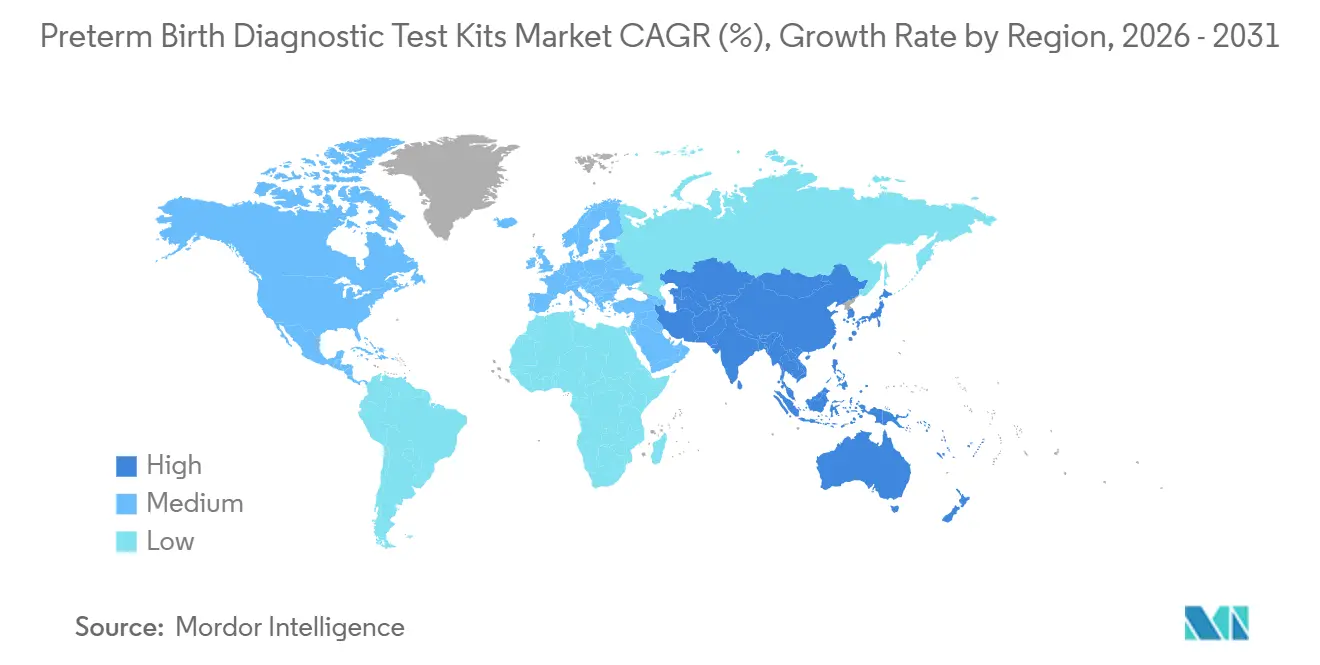
- Par région, l'Amérique du Nord a contribué à 43,64 % des revenus de 2025 et l'Asie-Pacifique devrait croître à un CAGR de 9,45 % jusqu'en 2031.
Note : La taille du marché et les prévisions figurant dans ce rapport sont générées à l'aide du cadre d'estimation exclusif de Mordor Intelligence, mis à jour avec les dernières données et informations disponibles en janvier 2026.
Tendances et perspectives du marché mondial des kits de tests diagnostiques pour naissance prématurée
Analyse de l'impact des moteurs
| Moteur | (~) % d'impact sur les prévisions de CAGR | Pertinence géographique | Horizon temporel de l'impact |
|---|---|---|---|
| Incidence mondiale croissante et charge des naissances prématurées | +2.3% | Mondial, avec une pression aiguë en Afrique subsaharienne et en Asie du Sud | Long terme (≥ 4 ans) |
| Intégration du triage basé sur les biomarqueurs dans les parcours cliniques (fFN, PAMG-1, IGFBP-1) | +2.8% | Amérique du Nord et UE en cœur, extension vers les centres urbains d'Asie-Pacifique | Moyen terme (2-4 ans) |
| Kits à flux latéral rapides au point de soins permettant des décisions rapides d'exclusion dans le triage en maternité | +1.6% | Amérique du Nord, Europe occidentale, Australie | Court terme (≤ 2 ans) |
| Protocoles hospitaliers et soutien au remboursement pour les tests ciblés dans les cas à haut risque/symptomatiques | +1.1% | National, avec des gains précoces dans les plans commerciaux américains et Medicaid, les systèmes publics européens | Moyen terme (2-4 ans) |
| Expansion des tests de risque protéomiques sanguins informant des parcours de soins plus précoces | +0.9% | Axé sur les États-Unis, programmes pilotes dans certains marchés européens | Long terme (≥ 4 ans) |
| Outils de décision numériques combinant des biomarqueurs quantitatifs avec la longueur cervicale | +0.5% | Cœur Asie-Pacifique (Chine, Inde, Corée du Sud), émergent en Amérique latine | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Incidence mondiale croissante et charge des naissances prématurées
La naissance prématurée demeure une cause majeure de morbidité et de mortalité néonatales dans le monde, ce qui soutient la demande clinique pour une évaluation du risque plus précoce et plus précise. Les hôpitaux cherchent à standardiser le triage afin de limiter les transferts inutiles et de soutenir l'utilisation opportune des corticostéroïdes uniquement lorsque le risque est crédible et proche du terme. La charge persistante dans les contextes à faibles ressources expose un écart entre le besoin et l'accès, ce qui soutient l'utilisation de tests plus simples et retarde l'adoption de dosages avancés de biomarqueurs. Les systèmes de santé évaluent la valeur opérationnelle des tests capables d'exclure rapidement un accouchement imminent, prévenant ainsi des hospitalisations évitables et réduisant la pression sur les unités tertiaires. Ces dynamiques maintiennent le marché des kits de tests diagnostiques pour naissance prématurée axé sur la rapidité et la clarté du résultat pour renforcer les décisions en première ligne.
Intégration du triage basé sur les biomarqueurs dans les parcours cliniques (fFN, PAMG-1, IGFBP-1)
De nombreux établissements en Amérique du Nord et en Europe ont intégré le triage basé sur les biomarqueurs dans des protocoles standardisés pour les patientes présentant des symptômes entre 24 et 34 semaines, réduisant les admissions injustifiées lorsqu'un résultat négatif clair est obtenu. L'arrêt des cassettes quantitatives de fibronectine fœtale a incité les recommandations nationales en 2024 à passer à des plateformes alternatives, ce qui a reconfiguré les achats et encouragé une évaluation plus large des options IGFBP-1 et PAMG-1[1]NHS England, "Arrêt des tests de fibronectine fœtale Hologic," NHS England, england.nhs.uk. Le rôle des diagnostics de rupture des membranes persiste dans le cadre du parcours de soins, car le statut membranaire influence directement le risque de travail à court terme et les choix de surveillance clinique. Le triage guidé par les protocoles limite la variabilité entre les cliniciens et oriente les ressources vers les cas présentant un risque mesurable plutôt que vers une observation préventive. Les recommandations professionnelles et les comités institutionnels continuent de façonner l'adoption, ancrant le marché des kits de tests diagnostiques pour naissance prématurée aux tests qui fournissent une clarté binaire ou quasi binaire en quelques minutes.
Kits à flux latéral rapides au point de soins permettant des décisions rapides d'exclusion dans le triage en maternité
Les immunodosages au point de soins fournissent des résultats lors de la même consultation, ce qui permet aux équipes de procéder au congé en toute confiance après un test négatif ou d'intensifier les soins lorsqu'un résultat positif signale un risque à court terme. Le délai d'obtention du résultat détermine la valeur opérationnelle, car les unités d'urgence doivent souvent décider du transfert ou du moment d'administration des stéroïdes dans des délais courts. Les formats stables en rayonnage et les flux de travail simples font des kits à flux latéral un outil pratique pour les unités de travail chargées et pour les centres plus petits cherchant une pratique cohérente. Lorsque le test de rupture des membranes est pertinent, les options à flux latéral permettent une confirmation rapide du statut membranaire et réduisent la dépendance aux méthodes traditionnelles moins précises. Les politiques des payeurs et les formulaires locaux influencent encore les kits utilisés en routine, c'est pourquoi les protocoles et les normes d'achat restent essentiels pour élargir l'accès. Le marché des kits de tests diagnostiques pour naissance prématurée bénéficie lorsque les menus de tests s'intègrent dans des flux de travail au point de soins qui règlent les décisions de triage en quelques minutes.
Protocoles hospitaliers et soutien au remboursement pour les tests ciblés dans les cas à haut risque/symptomatiques
La couverture et les protocoles internes déterminent ensemble la régularité avec laquelle les tests sont utilisés dans les soins obstétricaux de première ligne. Lorsque les comités hospitaliers codifient les séquences de tests pour les femmes symptomatiques, la variabilité clinique diminue et les résultats deviennent plus faciles à gérer et à mesurer. Au Royaume-Uni, les recommandations nationales faisant suite à l'arrêt du fFN ont illustré comment les systèmes publics peuvent orienter la sélection des produits et stabiliser les pratiques entre les sites. Aux États-Unis, les modèles de laboratoire centralisés pour les tests protéomiques sanguins opèrent sous la supervision du CLIA et du CAP, ce qui permet une qualité constante à grande échelle à mesure que les payeurs examinent les données de résultats pour une couverture élargie. Les entreprises ont signalé des engagements avec les payeurs et des discussions actives concernant le remboursement des stratégies de prévention éclairées par les résultats de risque protéomique, ce qui reflète une dynamique vers des arrangements basés sur la valeur. Ces tendances renforcent l'orientation du marché des kits de tests diagnostiques pour naissance prématurée vers des tests liés à des actions cliniques claires et à des compensations de coûts mesurables.
Analyse de l'impact des freins
| Frein | (~) % d'impact sur les prévisions de CAGR | Pertinence géographique | Horizon temporel de l'impact |
|---|---|---|---|
| Recommandations mixtes/conditionnelles pour certains biomarqueurs et utilisations | -0.7% | Mondial, variabilité la plus élevée au Moyen-Orient et en Amérique latine | Moyen terme (2-4 ans) |
| VPP modeste/faux positifs nécessitant une évaluation confirmatoire | -0.4% | Mondial, charge opérationnelle concentrée dans les contextes à faibles ressources | Court terme (≤ 2 ans) |
| Contraintes opérationnelles d'échantillonnage (délai, co-interférence) limitant le déploiement universel | -0.3% | Afrique subsaharienne, Asie du Sud rurale, Australie éloignée | Moyen terme (2-4 ans) |
| Le règlement européen sur les dispositifs de diagnostic in vitro élève les exigences en matière de preuves cliniques, de coûts et de délais de mise sur le marché pour les dispositifs de diagnostic in vitro | -0.8% | UE27, extension aux pays reconnaissant le marquage CE | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Recommandations mixtes/conditionnelles pour certains biomarqueurs et utilisations
La variabilité des recommandations selon les régions ralentit l'adoption standardisée et maintient un patchwork de pratiques de test au sein des pays et entre eux. Les documents professionnels font souvent référence aux classes de biomarqueurs plutôt qu'à des marques spécifiques, ce qui laisse aux équipes d'achat le soin de décider en fonction du prix, de la disponibilité et de la familiarité locale. L'approbation incohérente pour des cas d'utilisation tels que le dépistage asymptomatique contribue à une adoption inégale en dehors des centres tertiaires. Les cliniciens sont également confrontés à des règles de remboursement divergentes selon les payeurs sur les tests remboursés dans des scénarios spécifiques, ce qui ajoute des frictions à la prescription de routine. Ces facteurs tempèrent le rythme auquel le marché des kits de tests diagnostiques pour naissance prématurée peut passer d'une utilisation pilote à un déploiement stable guidé par les protocoles.
Le règlement européen sur les dispositifs de diagnostic in vitro élève les exigences en matière de preuves cliniques, de coûts et de délais de mise sur le marché pour les dispositifs de diagnostic in vitro
Les exigences réglementaires européennes ont élargi les obligations en matière de preuves et de surveillance post-commercialisation, ce qui augmente le coût et la complexité de la mise sur le marché des diagnostics obstétricaux. La capacité des organismes notifiés et les exigences documentaires prolongent les délais pour les mises à jour et les nouvelles revendications, ce qui peut retarder les transitions de l'utilisation pilote à la disponibilité élargie. Les entreprises disposant de systèmes qualité matures et de soumissions antérieures ont tendance à naviguer dans les examens de manière plus prévisible, tandis que les nouveaux entrants font face à des besoins en ressources plus importants. Il en résulte une barre plus haute pour les données de performance et la surveillance continue, ce qui peut consolider les parts avec les acteurs établis au fil du temps. Cet environnement encourage les fournisseurs à prioriser les revendications de tests qui s'alignent étroitement sur l'utilité clinique et la valeur pour les payeurs, afin que les investissements en conformité se traduisent en traction d'adoption.
Analyse des segments
Par type de produit : la protéomique sanguine réduit l'écart de triage
La fibronectine fœtale représentait 43,89 % de la taille du marché des kits de tests diagnostiques pour naissance prématurée en 2025, reflétant l'ancrage historique avant qu'un changement d'approvisionnement ne modifie les comportements de commande. L'arrêt des cassettes quantitatives de fFN en 2024 a remplacé la norme quantitative par des biomarqueurs qualitatifs et alternatifs dans de nombreux parcours hospitaliers. Les plateformes PAMG-1 devraient croître à un CAGR de 9,67 % jusqu'en 2031, à mesure que les hôpitaux adoptent des formats binaires d'exclusion qui rationalisent les décisions de triage pour les femmes symptomatiques. Les diagnostics de rupture des membranes restent un pilier complémentaire dans le parcours, car la confirmation du statut membranaire influence substantiellement la gestion du risque à court terme. Le marché des kits de tests diagnostiques pour naissance prématurée redéfinit également le calendrier, les tests sanguins protéomiques, menés par PreTRM, se concentrant sur le risque entre 18 et 20 semaines avec une stratégie de prévention basée sur la progestérone, l'aspirine et une navigation de soins intensifiée[2]Sera Prognostics, "La science derrière le test PreTRM," PreTRM, pretrm.com. Les données probantes randomisées rapportées en 2026 ont montré une réduction des naissances très prématurées et moins de complications néonatales lorsque le dépistage PreTRM était associé à des interventions ciblées. Ces évolutions déplacent le centre de gravité en amont, de la gestion de crise entre 24 et 34 semaines vers une stratification précoce du risque susceptible d'éviter des épisodes à coût élevé. Les hôpitaux valorisent toujours une valeur prédictive négative exploitable pour éviter les transferts, tandis que les laboratoires privilégient les flux de travail centralisés pour les dosages complexes. Ensemble, ces dynamiques de produits soutiennent un marché à deux vitesses dans lequel les kits à écouvillon rapides soutiennent le triage aigu et la protéomique sanguine s'étend aux soins préventifs.
Le mix de produits reflète des compromis opérationnels clairs qui façonnent les préférences des acheteurs. Les écouvillons au point de soins qui retournent des résultats en quelques minutes conviennent aux unités d'urgence et d'observation qui ont besoin d'une clarté immédiate pour les décisions d'exclusion. Les options PAMG-1 et IGFBP-1 se concurrencent sur le prix, la disponibilité et la familiarité avec les recommandations locales, à mesure que les équipes d'achat cherchent un approvisionnement fiable après les perturbations du fFN. Les dosages protéomiques sanguins nécessitent un traitement centralisé mais ouvrent un nouveau levier de prévention ciblant les nombreuses naissances prématurées spontanées qui manquent de facteurs de risque traditionnels. Le marché des kits de tests diagnostiques pour naissance prématurée aligne donc les produits sur le calendrier clinique, le triage symptomatique étant ancré par les kits à flux latéral et le risque asymptomatique étant traité par des tests protéomiques qui influencent les plans de soins des semaines avant l'apparition des symptômes. Ce positionnement complémentaire aide les fournisseurs à se défendre contre la concurrence uniquement par les prix en liant les tests aux résultats et à l'impact budgétaire.
Note: Les parts de segment de tous les segments individuels sont disponibles à l'achat du rapport
Par matériau : les écouvillons vaginaux ancrent le volume, les dosages sanguins captent la valeur
Les tests par écouvillon vaginal-cervical représentaient 60,10 % de la part du marché des kits de tests diagnostiques pour naissance prématurée en 2025, reflétant les flux de travail hospitaliers établis et la rapidité des résultats que ces formats offrent. La collecte par écouvillon s'aligne sur les protocoles qui privilégient le confort des patientes et le soutien immédiat à la décision pour les cas symptomatiques. Les réalités opérationnelles telles que le délai d'échantillonnage et les interférences potentielles nécessitent encore de la rigueur, ce qui souligne l'importance des parcours de triage standardisés. Les plateformes sanguines devraient se développer à un CAGR de 9,01 % jusqu'en 2031, à mesure que les laboratoires centralisés utilisent le traitement par lots et les contrôles de qualité pour élargir l'accès aux fenêtres de dépistage préventif. Sera Prognostics a mis en avant la logistique du sang total ambiant et les opérations CLIA centralisées comme principaux facteurs permettant des tests protéomiques cohérents à l'échelle nationale. Des recherches indépendantes ont également rapporté des panels de protéines plasmatiques prometteurs au deuxième trimestre pour la prédiction des naissances prématurées spontanées, ce qui signale un potentiel supplémentaire pour l'innovation des tests sanguins. Ces différences de matériaux correspondent à des moments de soins distincts et créent une voie équilibrée pour la croissance dans les contextes aigus et préventifs.
Le choix du matériau affecte également le débit et le flux de données vers les équipes soignantes. Les écouvillons à flux latéral fournissent des résultats au point de soins et soutiennent les décisions de congé en temps réel dans les salles d'urgence et les unités de triage du travail. La protéomique sanguine favorise les visites prénatales programmées et l'interprétation centralisée qui retourne un risque individualisé en jours plutôt qu'en minutes. À mesure que les systèmes de santé combinent les biomarqueurs avec l'échographie de longueur cervicale, les deux matériaux contribuent à des algorithmes d'inclusion et d'exclusion plus clairs qui optimisent l'utilisation des ressources. Le marché des kits de tests diagnostiques pour naissance prématurée accommode donc un rôle durable pour les écouvillons tout en élargissant la valeur des tests sanguins pour une planification d'intervention plus précoce.
Par utilisateur final : les laboratoires dépassent les hôpitaux sur les flux de travail à haute complexité
Les hôpitaux et maternités représentaient 58,56 % de la part du marché des kits de tests diagnostiques pour naissance prématurée en 2025, portés par l'utilisation constante d'écouvillons au point de soins dans les contextes de triage où la rapidité est centrale. Les résultats négatifs permettent le congé le jour même et limitent les séjours d'observation qui ne sont pas cliniquement nécessaires. Les laboratoires de diagnostic ont enregistré un CAGR de 10,34 % jusqu'en 2031 en absorbant les panels envoyés à l'extérieur et la protéomique sanguine qui nécessitent des flux de travail centralisés et des instruments spécialisés. Sera Prognostics exploite un seul laboratoire certifié CLIA et accrédité CAP pour traiter tous les échantillons PreTRM à l'échelle nationale, ce qui permet une surveillance étroite des performances à grande échelle. Cette division du travail s'aligne sur la manière dont les soins sont dispensés, les hôpitaux privilégiant l'immédiateté et les laboratoires faisant progresser la prévention et la gestion des risques.
Une dynamique se construit pour des modèles intégrés qui unifient les décisions au point de soins avec l'analyse centralisée. Les hôpitaux conservent un rôle fort dans le triage symptomatique, tandis que les laboratoires élargissent l'empreinte de dépistage en amont avec des évaluations protéomiques pouvant déclencher des interventions ciblées. Les payeurs évaluant les données de résultats peuvent encourager des modèles combinant des tests de triage immédiats avec des stratégies préventives réduisant les jours en unité de soins intensifs néonatals et les coûts. Le marché des kits de tests diagnostiques pour naissance prématurée reflète donc les atouts des utilisateurs finaux tant en termes d'immédiateté que de bénéfices de soins longitudinaux.
Analyse géographique
L'Amérique du Nord détenait 43,64 % des revenus de 2025 et ancre le marché des kits de tests diagnostiques pour naissance prématurée avec des protocoles intégrant l'utilisation des biomarqueurs dans les unités de travail et d'accouchement. L'arrêt en 2024 du fFN quantitatif a entraîné des transitions accélérées vers des biomarqueurs alternatifs et a renforcé le poids des recommandations nationales dans la définition des pratiques. Le Canada et le Mexique sont en retard par rapport à l'adoption américaine, les règles d'achat et de couverture variant selon les provinces et les mix de payeurs. La croissance américaine inclut désormais des projets pilotes de dépistage asymptomatique dans le cadre de plans commerciaux et Medicaid, ce qui pousse l'adoption au-delà du triage de crise vers la prévention. Le marché des kits de tests diagnostiques pour naissance prématurée en Amérique du Nord continue d'équilibrer l'utilisation rapide des écouvillons avec les flux de travail protéomiques émergents capables de démontrer des résultats mesurables.
L'Asie-Pacifique devrait croître à un CAGR de 9,45 % jusqu'en 2031, à mesure que les laboratoires se développent en Chine, en Inde et en Corée du Sud et que des projets pilotes publics examinent la couverture pour les dosages plus récents. La fabrication nationale et les appels d'offres sensibles aux prix influencent l'adoption des écouvillons dans les réseaux publics, tandis que les chaînes d'hôpitaux privés se concentrent sur le PAMG-1 et l'IGFBP-1 dans les centres urbains. Le déclin du taux de natalité au Japon et une main-d'œuvre obstétricale contrainte tempèrent la croissance de la demande, mais une adoption ciblée persiste dans les centres tertiaires. En Australie, les groupes cliniques ont surveillé les implications des changements d'approvisionnement en fFN sur les pratiques de transfert rural et ont cherché des alternatives cohérentes pour préserver la confiance dans le triage. Dans toute l'Asie du Sud-Est, la chaîne du froid limitée et les voies réglementaires fragmentées ralentissent l'adoption de nouveaux biomarqueurs, ce qui maintient le marché des kits de tests diagnostiques pour naissance prématurée ancré à des options abordables et robustes.
L'Europe a maintenu sa part à mesure que les établissements naviguaient dans l'évolution des exigences réglementaires et des délais de conformité pour les dispositifs de diagnostic in vitro. L'Allemagne, la France et le Royaume-Uni intègrent les tests de biomarqueurs dans les parcours de maternité, bien que les évaluations budgétaires puissent ralentir l'inclusion dans les calendriers de remboursement nationaux. Le changement de 2024 au Royaume-Uni vers des tests de triage alternatifs après l'arrêt du fFN a mis en évidence la sensibilité aux coûts du secteur public et le rôle central des recommandations nationales. L'Europe du Sud et de l'Est présente une adoption inégale en raison de l'administration sanitaire régionalisée et d'une dépense par habitant plus faible, ce qui maintient la dépendance au jugement clinique et aux tests plus anciens dans certains contextes. Le marché des kits de tests diagnostiques pour naissance prématurée en Europe récompense de plus en plus les fournisseurs capables de répondre aux besoins documentaires et post-commercialisation sans interrompre l'approvisionnement.
Le Moyen-Orient et l'Afrique affichent une croissance naissante, les hôpitaux privés du Golfe important des plateformes de biomarqueurs occidentales et les centres tertiaires d'Afrique du Sud utilisant les diagnostics de manière sélective. L'Afrique subsaharienne supporte une charge élevée de naissances prématurées mais fait face à des contraintes d'infrastructure qui limitent l'utilisation des tests aux centres urbains. Les efforts programmatiques continuent de cibler les complications connexes telles que la prééclampsie, où de nouveaux tests rapides en développement cherchent à élargir l'accès dans les contextes à ressources limitées. Les secteurs privés d'Amérique du Sud au Brésil et en Argentine soutiennent l'adoption dans les cliniques urbaines, tandis que les systèmes publics font face à des pressions budgétaires qui modèrent l'échelle. Ces facteurs régionaux maintiennent la croissance du marché des kits de tests diagnostiques pour naissance prématurée liée à la sophistication des achats, à la capacité des laboratoires et à la volonté des payeurs de lier les tests à des résultats mesurables.
Paysage concurrentiel
Le marché des kits de tests diagnostiques pour naissance prématurée reste fragmenté, et l'arrêt du fFN en 2024 a redistribué les opportunités de parts à plusieurs fournisseurs de biomarqueurs. QIAGEN exploite un portefeuille de rupture des membranes et de travail prématuré pour la vente croisée dans les programmes de santé féminine, ce qui permet des contrats groupés à travers les réseaux hospitaliers. Sera Prognostics fait progresser un modèle de laboratoire centralisé axé sur les fenêtres de dépistage préventif et les résultats pour les payeurs, renforcé par des données probantes randomisées de 2026 soutenant des réductions des naissances très prématurées et des complications néonatales. Ces stratégies se différencient selon le calendrier et le contexte de soins, ce qui permet aux fournisseurs de défendre la valeur malgré la concurrence par les prix dans les catégories d'écouvillons de base.
Les mouvements stratégiques soulignent la génération de preuves et la couverture comme différenciateurs essentiels. Sera a signalé des engagements avec les payeurs et l'expansion de sa présence commerciale sur le terrain pour accélérer l'adoption parmi les réseaux de prestation intégrés. Dans les troubles hypertensifs de la grossesse, Roche a obtenu l'autorisation 510(k) de la FDA américaine pour un test de ratio qui informe l'intensité de la surveillance et le calendrier d'accouchement, ce qui élargit indirectement l'ensemble des problèmes adressables liés à la naissance prématurée. De telles avancées réglementaires et données cliniques aident les entreprises à articuler les bénéfices des résultats au-delà de la précision prédictive, ce qui importe pour les contrats basés sur la valeur et les achats basés sur le budget.
Les pressions sur les coûts et la conformité façonnent les incitations à la consolidation sans éliminer la place pour les spécialistes. Les entreprises disposant de systèmes qualité robustes et d'une expérience réglementaire multi-régions sont mieux positionnées pour naviguer dans l'évolution des preuves et des obligations post-commercialisation, ce qui stabilise l'approvisionnement et soutient la discipline des prix. Les nouveaux entrants qui s'appuient sur des produits uniques se concurrencent en mettant l'accent sur l'accessibilité financière, la stabilité en rayonnage ou des avantages discrets de flux de travail qui résolvent des points de douleur dans les contextes à ressources limitées. Le marché des kits de tests diagnostiques pour naissance prématurée se concentre donc sur la rapidité, l'agilité réglementaire et la valeur liée aux résultats qui ensemble favorisent une adoption durable.
Leaders du secteur des kits de tests diagnostiques pour naissance prématurée
BIOSYNEX S.A.
Laborie Medical Technologies (Clinical Innovations)
Medix Biochemica (Actim)
QIAGEN N.V.
Hologic, Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents du secteur
- Janvier 2026 : Sera Prognostics a publié l'étude PRIME dans PREGNANCY, démontrant que le dépistage par test sanguin PreTRM associé à la progestérone vaginale quotidienne, à l'aspirine à faible dose et à la gestion des soins infirmiers a réduit les naissances avant 32 semaines de 56 % et les admissions en unité de soins intensifs néonatals de 20 % parmi 5 018 femmes inscrites dans 19 sites américains. L'essai contrôlé randomisé a atteint les deux critères d'évaluation primaires et a économisé un jour en unité de soins intensifs néonatals pour chaque 4,2 patients dépistés, fournissant des preuves que le dépistage par biomarqueurs en amont combiné à des interventions ciblées améliore les résultats néonatals et réduit les coûts de santé.
- Mars 2026 : Sera Prognostics a publié les résultats financiers de l'exercice 2025 complet et a noté que des commentaires européens dans The Journal of Maternal-Fetal & Neonatal Medicine ont soutenu l'approche test-et-traitement PreTRM comme évolutive pour les systèmes financés par les fonds publics. La société a divulgué des discussions actives avec les payeurs dans le cadre de plans commerciaux et Medicaid et a élargi son organisation commerciale américaine pour cibler une adoption plus large parmi les réseaux de prestation intégrés.
- Février 2025 : Roche Diagnostics a reçu l'autorisation 510(k) de la FDA américaine pour le test de ratio Elecsys sFlt-1/PlGF afin de stratifier les femmes enceintes hospitalisées présentant des troubles hypertensifs selon le risque à court terme de développer une prééclampsie sévère, ce qui peut informer la surveillance ou des décisions d'accouchement plus précoces qui recoupent le risque de naissance prématurée.
Portée du rapport mondial sur le marché des kits de tests diagnostiques pour naissance prématurée
Selon la portée du rapport, les kits de tests diagnostiques pour naissance prématurée sont des dosages rapides, soit au point de soins soit en laboratoire, conçus pour évaluer le risque d'accouchement prématuré chez les femmes enceintes. Ces kits fonctionnent en détectant des biomarqueurs spécifiques dans le liquide cervico-vaginal ou le sang, permettant aux prestataires de soins de santé de déterminer si une femme symptomatique est susceptible d'accoucher dans les 7 à 14 prochains jours.
Le marché des kits de tests diagnostiques pour naissance prématurée est segmenté par type de produit, matériau, utilisateur final et géographie. Par type de produit, le marché est segmenté en fibronectine fœtale, basé sur le PAMG-1, basé sur l'IGFBP-1, tests de rupture des membranes à double marqueur et tests de risque protéomiques sanguins. Par matériau, le marché est segmenté en écouvillon vaginal/cervical et sang. Par utilisateur final, le marché est segmenté en hôpitaux et maternités, laboratoires de diagnostic, centres d'accouchement/cliniques ambulatoires d'obstétrique-gynécologie et autres. Par géographie, le marché est segmenté en Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique et Amérique du Sud. Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays dans les principales régions du monde. Le rapport offre la valeur (en USD) pour les segments ci-dessus.
| Fibronectine fœtale |
| Basé sur le PAMG-1 |
| Basé sur l'IGFBP-1 |
| Tests de rupture des membranes à double marqueur |
| Tests de risque protéomiques sanguins |
| Écouvillon vaginal/cervical |
| Sang |
| Hôpitaux et maternités |
| Laboratoires de diagnostic |
| Centres d'accouchement / cliniques ambulatoires d'obstétrique-gynécologie |
| Autres |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par type de produit | Fibronectine fœtale | |
| Basé sur le PAMG-1 | ||
| Basé sur l'IGFBP-1 | ||
| Tests de rupture des membranes à double marqueur | ||
| Tests de risque protéomiques sanguins | ||
| Par matériau | Écouvillon vaginal/cervical | |
| Sang | ||
| Par utilisateur final | Hôpitaux et maternités | |
| Laboratoires de diagnostic | ||
| Centres d'accouchement / cliniques ambulatoires d'obstétrique-gynécologie | ||
| Autres | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés auxquelles le rapport répond
Quelle est la taille actuelle et les perspectives de croissance du marché des kits de tests diagnostiques pour naissance prématurée ?
La taille du marché des kits de tests diagnostiques pour naissance prématurée est de 180,78 millions USD en 2025 et devrait atteindre 287,57 millions USD d'ici 2031 avec un CAGR de 8,32 % sur 2026-2031.
Quel segment connaît la croissance la plus rapide au sein du marché des kits de tests diagnostiques pour naissance prématurée ?
Les plateformes PAMG-1 et les dosages protéomiques sanguins sont les plus en croissance, avec des CAGR projetés de 9,67 % et 9,01 % respectivement jusqu'en 2031.
Comment l'arrêt du fFN a-t-il affecté le marché des kits de tests diagnostiques pour naissance prématurée ?
L'arrêt en 2024 des cassettes quantitatives de fFN a déplacé les achats vers des biomarqueurs alternatifs et a renforcé le rôle des protocoles hospitaliers et des recommandations nationales dans la sélection des produits.
Quelles preuves soutiennent un dépistage plus précoce et asymptomatique dans ce domaine ?
En 2026, une grande étude randomisée a rapporté moins de naissances très prématurées et moins de complications néonatales lorsqu'une stratégie de prévention basée sur le PreTRM était utilisée dans les grossesses à faible risque.
Quelles régions sont en tête et lesquelles s'accélèrent sur le marché des kits de tests diagnostiques pour naissance prématurée ?
L'Amérique du Nord est en tête par part de revenus en 2025, tandis que l'Asie-Pacifique devrait se développer le plus rapidement jusqu'en 2031, à mesure que les laboratoires se développent et que les projets pilotes élargissent l'accès.
Comment le mix d'utilisateurs finaux influence-t-il les schémas d'adoption pour les tests de prématurité ?
Les hôpitaux dominent le triage urgent avec des écouvillons rapides, tandis que les laboratoires de diagnostic croissent plus rapidement en développant les tests protéomiques centralisés et les panels envoyés à l'extérieur nécessitant des flux de travail spécialisés.
Dernière mise à jour de la page le: