Taille et Part du Marché des Systèmes d'Exécution de la Fabrication Pharmaceutique
Analyse du Marché des Systèmes d'Exécution de la Fabrication Pharmaceutique par Mordor Intelligence
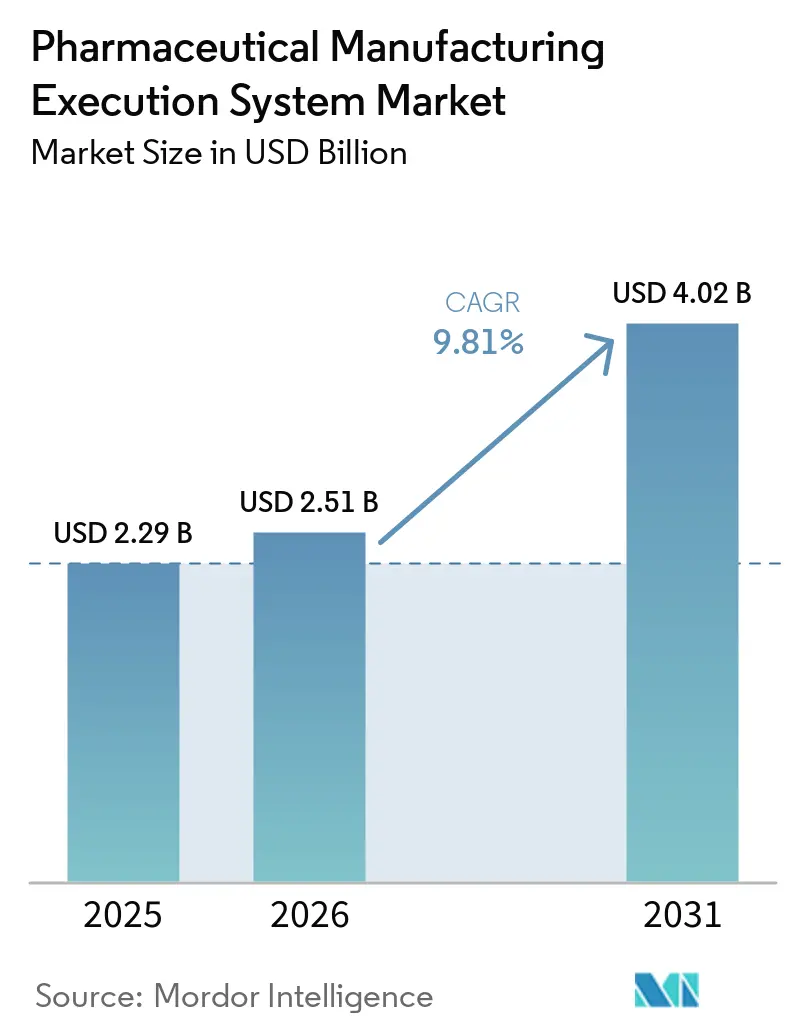
La taille du Marché des Systèmes d'Exécution de la Fabrication Pharmaceutique est projetée à 2,29 milliards USD en 2025, 2,51 milliards USD en 2026, et devrait atteindre 4,02 milliards USD d'ici 2031, avec un TCAC de 9,81 % de 2026 à 2031.
La numérisation réglementaire, les pratiques de validation fondées sur les risques et la pression constante sur l'intégrité des données et la sérialisation continuent d'orienter les investissements vers des plateformes MES validées capables d'orchestrer des opérations conformes sur plusieurs sites. Le marché des systèmes d'exécution de la fabrication pharmaceutique bénéficie également de déploiements natifs en cloud qui réduisent la charge d'infrastructure et accélèrent les déploiements mondiaux tout en maintenant l'état validé et la traçabilité des audits. En parallèle, les exigences de sérialisation et de traçabilité interopérable dans le cadre de réglementations matures intègrent la connectivité de niveau 4 et la messagerie EPCIS dans les flux de travail MES de base pour une visibilité de bout en bout. La croissance rapide des produits biologiques et des thérapies cellulaires et géniques élargit la demande de capacités MES permettant de gérer la chaîne d'identité et la chaîne de custody avec un contrôle déterministe, des listes de contrôle standardisées et une intégration étroite avec la planification, le LIMS et la chaîne du froid. Le marché des systèmes d'exécution de la fabrication pharmaceutique évolue donc d'une numérisation discrète au niveau des sites vers des architectures multi-usines activées par le cloud qui standardisent les recettes maîtresses, réduisent les cycles de révision et améliorent la résilience de la chaîne d'approvisionnement.
Points Clés du Rapport
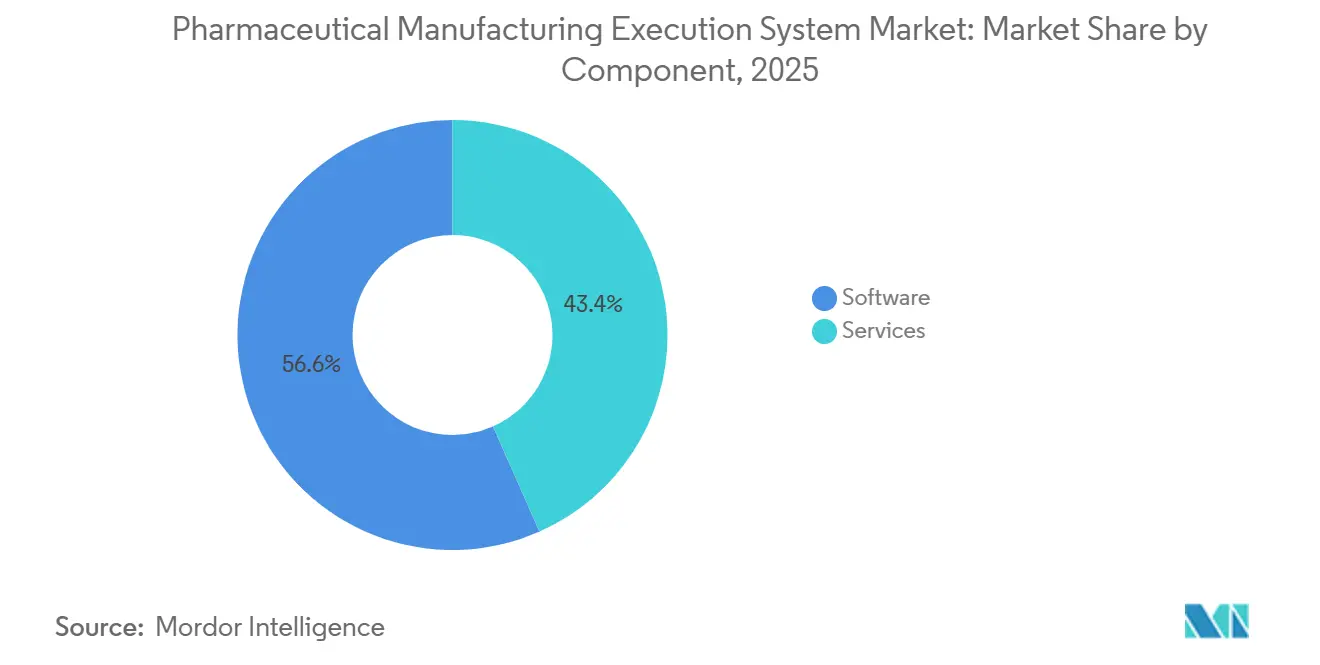
- Par composant, les logiciels ont capturé 56,64 % de la part de revenus en 2025, tandis que les services devraient afficher un TCAC de 10,23 % sur 2026-2031 dans le marché des systèmes d'exécution de la fabrication pharmaceutique.
- Par déploiement, le sur site détenait 55,81 % en 2025, et le cloud/SaaS devrait se développer à un TCAC de 13,65 % jusqu'en 2031.
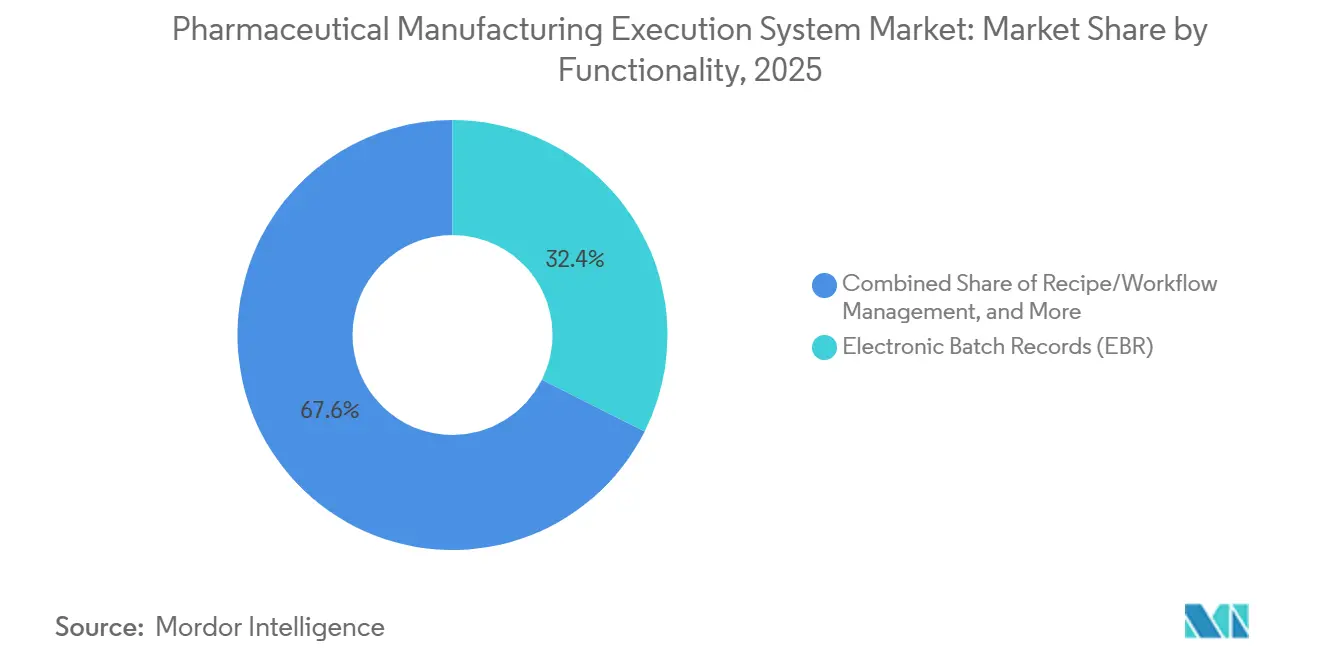
- Par fonctionnalité, les dossiers de lots électroniques étaient en tête avec 32,40 % en 2025, et l'intégration de la sérialisation progresse à un TCAC de 12,78 % jusqu'en 2031 dans le marché des systèmes d'exécution de la fabrication pharmaceutique.
- Par utilisateur final, les fabricants pharmaceutiques représentaient 42,54 % en 2025, tandis que les fabricants de thérapies cellulaires et géniques sont projetés à un TCAC de 14,93 % entre 2026 et 2031 dans le marché des systèmes d'exécution de la fabrication pharmaceutique.
- Par géographie, l'Amérique du Nord détenait 37,23 % de la part du marché des systèmes d'exécution de la fabrication pharmaceutique en 2025, tandis que l'Asie-Pacifique enregistrait le TCAC projeté le plus élevé à 15,83 % jusqu'en 2031.
Note : La taille du marché et les prévisions figurant dans ce rapport sont générées à l'aide du cadre d'estimation exclusif de Mordor Intelligence, mis à jour avec les dernières données et informations disponibles en janvier 2026.
Tendances et Perspectives du Marché Mondial des Systèmes d'Exécution de la Fabrication Pharmaceutique
Analyse de l'Impact des Moteurs
| Moteur | (~) % d'Impact sur les Prévisions de TCAC | Pertinence Géographique | Calendrier d'Impact |
|---|---|---|---|
| Conformité Réglementaire et Exigences d'Intégrité des Données | +3.2% | Mondial, avec un poids plus élevé en Amérique du Nord et dans l'UE en raison de l'escalade de l'application par la FDA et l'EMA | Court terme (≤ 2 ans) |
| Dynamique de Numérisation Pharma 4.0 (ISPE) | +2.1% | Amérique du Nord en tête, APAC suiveurs rapides | Moyen terme (2-4 ans) |
| Besoin de Visibilité en Temps Réel et de Traçabilité de Bout en Bout | +1.8% | Mondial, particulièrement critique dans les pôles de produits biologiques (États-Unis, UE, Singapour) | Court terme (≤ 2 ans) |
| Croissance des Produits Biologiques, des Thérapies Cellulaires et Géniques | +2.4% | Corridor biotechnologique américain, UE (Allemagne, Suisse), premiers adoptants en Chine/Singapour | Long terme (≥ 4 ans) |
| Assurance des Logiciels Informatiques (CSA) Permettant une Validation Fondée sur les Risques | +1.3% | Amérique du Nord, sites progressifs de l'UE | Moyen terme (2-4 ans) |
| Fabrication Continue (ICH Q13) et Libération en Temps Réel | +1.6% | Premiers adoptants aux États-Unis, dans l'UE, projets pilotes en Asie-Pacifique | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
La Conformité Réglementaire et les Exigences d'Intégrité des Données Accélèrent l'Investissement dans les MES
Les fabricants réglementés renforcent les systèmes électroniques validés pour se conformer aux exigences de la 21 CFR Partie 11 concernant les enregistrements électroniques fiables, les signatures électroniques et les pistes d'audit pouvant étayer des investigations rigoureuses. Les plateformes MES répondent à cela avec des flux de travail contrôlés, des actions horodatées et des journaux d'audit immuables qui réduisent le risque d'erreur et renforcent l'intégrité des données.[1]Équipe Dot Compliance, "Conformité FDA 21 CFR Partie 11 : Ce que vous devez savoir en 2026," Dot Compliance La sérialisation et la traçabilité interopérable poussent à une intégration plus profonde entre les MES et les référentiels d'entreprise pour garantir une visibilité au niveau de l'unité, du lot et de l'expédition sur l'ensemble du cycle de vie du produit. [2]SAP, "SAP Advanced Track and Trace for Pharmaceuticals," SAP Alors que les fabricants remplacent les enregistrements papier et hybrides par une exécution de lots numérisée et une révision par exception, ils compriment les délais de cycle et améliorent la préparation à la libération avec des déviations exploitables, des signatures et une complétude probatoire.[3]Honeywell, "Honeywell dévoile une plateforme d'automatisation assistée par IA pour transformer le secteur de la fabrication en sciences de la vie," Ce changement axé sur la conformité est visible dans la définition des projets et les évaluations des fournisseurs qui privilégient les modèles validés, les cycles de développement sécurisés et la préparation aux audits éprouvée.[4]Rockwell Automation, "Rockwell Automation lance PharmaSuite 12.00 pour accélérer les déploiements sécurisés et évolutifs," Le marché des systèmes d'exécution de la fabrication pharmaceutique s'oriente donc vers des plateformes capables de démontrer une intégrité des données pleinement conforme aux principes ALCOA et une génération de preuves simplifiée pour les audits et les inspections.
La Dynamique de Numérisation Pharma 4.0 Remodèle les Modèles Opérationnels
La numérisation des opérations progresse vers des architectures prêtes pour le cloud, conteneurisées et à faible code qui apportent de l'agilité à la validation et au contrôle des changements tout en préservant l'état validé. Les plateformes MES qui unifient l'exécution en atelier avec la qualité et l'analytique créent une image opérationnelle commune pour les opérateurs, les superviseurs et l'assurance qualité, ce qui favorise la prise de décision en temps réel et une meilleure disposition des lots. Les programmes d'amélioration continue s'appuient également sur des recettes maîtresses standardisées et des instructions de travail électroniques pour éliminer la variabilité et réduire les temps d'attente, ce qui est cohérent avec les ambitions de libération en temps réel. À mesure que les outils à faible code s'intègrent dans les écosystèmes MES, les ingénieurs de procédés peuvent itérer plus rapidement sur les flux de travail et les formulaires sans code personnalisé lourd, ce qui raccourcit les cycles de conception-validation dans le cadre d'approches fondées sur les risques.[5]Tulip, "Système d'Exécution de la Fabrication (MES) pour le Pharmaceutique," L'effet net est que le marché des systèmes d'exécution de la fabrication pharmaceutique s'aligne sur les principes Pharma 4.0 en faisant converger l'exécution, la qualité, la sérialisation et l'analytique avec des choix de déploiement flexibles qui s'adaptent d'une seule ligne à des réseaux multi-usines.
Le Besoin de Visibilité en Temps Réel Stimule l'Adoption de la Révision par Exception
Les fabricants font évoluer la révision des lots de la post-production vers une révision par exception simultanée afin de réduire les cycles de libération et de diminuer les contrôles manuels. En pratique, le MES applique des règles d'acceptation aux actions et résultats enregistrés, fait remonter les exceptions pour intervention humaine et achemine les problèmes vers des flux de travail CAPA standardisés qui accélèrent la clôture. Le même socle numérique permet des tableaux de bord d'équipements en temps réel et la généalogie des matériaux, ce qui favorise une replanification plus rapide, des rappels ciblés et des réponses plus résilientes aux arrêts imprévus. À mesure que les équipes gagnent en confiance dans la saisie contemporaine des données à partir des MES et des systèmes connectés, la dépendance aux enregistrements papier diminue et la préparation aux audits se renforce. Le marché des systèmes d'exécution de la fabrication pharmaceutique connaît donc une demande soutenue pour les modules EBR permettant la révision par exception et la gestion intégrée des déviations, car ils offrent des gains de temps mesurables et une cohérence qualité à grande échelle.
La Croissance des Produits Biologiques, des Thérapies Cellulaires et Géniques Exige une Infrastructure d'Exécution Spécialisée
Les programmes de produits biologiques et de thérapies cellulaires et géniques nécessitent une orchestration précise entre la planification des patients, les matériaux, l'analytique et la logistique, avec une chaîne d'identité et une chaîne de custody de bout en bout. Les fournisseurs répondent avec des couches d'orchestration spécialisées, du matériel à système fermé et des flux de travail numériques validés pour gérer les runs spécifiques aux patients sans risque de contamination croisée. Les déploiements MES hébergés dans le cloud gagnent du terrain dans les environnements cliniques et commerciaux précoces de thérapies cellulaires et géniques pour simplifier les opérations mondiales tout en préservant l'intégrité des données et les pistes d'audit. À mesure que les programmes de thérapies cellulaires et géniques se développent, l'intégration entre MES, LIMS, sérialisation et ERP devient essentielle pour maintenir l'identité des lots, coordonner les délais d'aphérèse à perfusion et assurer un suivi correct des doses. Ce profil de besoins spécialisés stimule la demande dans le marché des systèmes d'exécution de la fabrication pharmaceutique pour des capacités nativement centrées sur le patient et interopérables sur le continuum clinique et commercial.
Analyse de l'Impact des Freins
| Frein | (~) % d'Impact sur les Prévisions de TCAC | Pertinence Géographique | Calendrier d'Impact |
|---|---|---|---|
| Coût Élevé de Mise en Œuvre et Complexité du Programme | -1.4% | Entreprises de taille moyenne à l'échelle mondiale, particulièrement aiguë sur les marchés APAC sensibles aux coûts | Court terme (≤ 2 ans) |
| Intégration avec les Systèmes Hérités et les Silos de Données | -0.9% | Pharma mature avec des sites existants (Amérique du Nord, Europe occidentale) | Moyen terme (2-4 ans) |
| Lacunes en Talents de Validation et Goulots d'Étranglement dans la Transition CSV/CSA | -0.7% | Mondial, particulièrement aigu dans les CDMO d'Asie-Pacifique | Moyen terme (2-4 ans) |
| Insuffisances de Préparation à la Standardisation des Données Maîtresses et des Processus | -0.5% | Pharma multi-sites (Amérique du Nord, UE), CDMO à croissance rapide en APAC | Court terme (≤ 2 ans) |
| Source: Mordor Intelligence | |||
Le Coût Élevé de Mise en Œuvre et la Complexité du Programme Retardent l'Adoption par le Marché Intermédiaire
La complexité du programme reste un obstacle pour les organisations disposant d'équipes informatiques et d'assurance qualité réduites, car le MES est un programme de transformation plutôt qu'une simple installation de logiciel. Les modèles natifs en cloud et de services gérés gagnent la faveur car ils réduisent la propriété de l'infrastructure, simplifient la qualification et transfèrent davantage de documentation de validation aux fournisseurs qui appliquent des pratiques sécurisées de développement et de mise en production. Les boîtes à outils à faible code émergent également pour accélérer la création de valeur en permettant aux équipes de fabrication de configurer plus rapidement des flux de travail et des formulaires validés avec moins de code personnalisé. Certains fournisseurs proposent désormais du contenu pré-validé, des heures de conseil et des modèles sectoriels pour réduire l'effort de validation pour les équipes pharmaceutiques et biotechnologiques émergentes. Même avec ces avancées, de nombreux acheteurs du marché intermédiaire rythment les déploiements en fonction de la capacité de contrôle des changements et de la préparation des sites, ce qui peut allonger les délais globaux malgré les gains technologiques. Le marché des systèmes d'exécution de la fabrication pharmaceutique continue de répondre à ce frein avec des feuilles de route par phases, des projets pilotes hébergés dans le cloud et du contenu prédéfini pouvant être répliqué entre les usines sans retravail.
L'Intégration avec les Systèmes Hérités Fragmente la Continuité Numérique
Les sites existants hétérogènes doivent connecter les automates programmables, les SCADA, les historiens, les LIMS, les ERP et les référentiels de sérialisation dans un tissu de données cohérent et gouverné sans liens point à point fragiles. De nombreuses entreprises pharmaceutiques identifient l'intégration des équipements hérités comme un obstacle principal au succès des MES, ce qui suscite de l'intérêt pour des intergiciels riches en connecteurs et des interfaces standardisées qui réduisent les frais généraux de validation et de maintenance. Les silos de données augmentent également les coûts de reporting et ralentissent les investigations, c'est pourquoi les projets incluent de plus en plus une couche de données gouvernée qui unifie les enregistrements de lots, de qualité et d'approvisionnement dans un cadre de conformité unique. Les mandats de sérialisation s'ajoutent à cet agenda d'intégration en exigeant une association étroite entre le contexte de lot dans le MES et les identifiants au niveau de l'unité dans les référentiels d'entreprise pour le reporting mondial. Les fournisseurs répondent avec des gestionnaires de sites modulaires, la messagerie EPCIS 1.2 et la mise à l'échelle dans le cloud qui réduisent les interfaces personnalisées tout en maintenant les garde-fous d'intégrité des données. Le marché des systèmes d'exécution de la fabrication pharmaceutique évolue donc vers des connecteurs indépendants des fournisseurs, des packs d'intégration prédéfinis et des services cloud gérés sur le cycle de vie qui simplifient l'intégration dans des parcs d'usines diversifiés.
Analyse des Segments
Par Composant : La Croissance des Services Reflète la Complexité des Écosystèmes Informatiques Pharmaceutiques
Les logiciels ont capturé 56,64 % de la part du marché des systèmes d'exécution de la fabrication pharmaceutique en 2025, et les services devraient se développer à un TCAC de 10,23 % sur 2026-2031, reflétant une demande croissante pour des déploiements dirigés par des experts, la validation et le support du cycle de vie. Les acheteurs continuent de privilégier les fournisseurs disposant d'EBR éprouvés, de gestion des déviations et d'intégration de la sérialisation, ainsi que de pratiques de développement sécurisées et de pistes d'audit robustes. À mesure que les organisations étendent les déploiements multi-sites, elles ont également besoin de services soutenus pour gérer les versions, les tests de régression et les notes de mise à jour conformément aux systèmes qualité. Le marché des systèmes d'exécution de la fabrication pharmaceutique connaît donc des taux d'attachement plus larges pour la formation, la validation gérée et le support 24h/24 et 7j/7 afin de maintenir un état validé lors des mises à niveau. Du côté de la main-d'œuvre, les fournisseurs et les intégrateurs aident à combler les lacunes en compétences avec des programmes certifiés afin que les opérateurs, l'assurance qualité et les administrateurs informatiques puissent maintenir des opérations conformes. Ce modèle centré sur les services est renforcé par les MES en cloud, où les fournisseurs qualifient l'infrastructure et fournissent du contenu pré-validé qui réduit la charge des clients lors des déploiements et des mises à jour de routine.
La croissance des services reflète également la complexité de l'intégration des MES avec les systèmes d'automatisation, de qualité et d'entreprise dans les environnements existants. Les équipes industrielles favorisent de plus en plus les partenaires qui apportent des connecteurs prédéfinis, des modèles de validation et des accélérateurs de recettes pour réduire les délais de projet sans sacrifier la conformité. Le secteur des systèmes d'exécution de la fabrication pharmaceutique adopte des outils à faible code pour accélérer la configuration des formulaires et des flux de travail sous contrôle des changements, ce qui à son tour élève la demande de services de gouvernance et de gestion du cycle de vie. Les fournisseurs regroupent également des heures de conseil avec de nouvelles licences et des offres en tant que service pour aligner la portée avec les activités d'assurance fondées sur les risques et la préparation des sites. Cette migration vers une livraison de valeur axée sur les services positionne le marché des systèmes d'exécution de la fabrication pharmaceutique pour une expansion soutenue des services à mesure que la maturité numérique progresse dans les grandes entreprises pharmaceutiques, les biotechs et les CDMO.
Par Déploiement : Le Cloud/SaaS Gagne du Terrain à Mesure que la Charge de Validation se Déplace vers les Fournisseurs
Les déploiements sur site détenaient 55,81 % en 2025, tandis que le Cloud/SaaS devrait être la voie de croissance la plus rapide à un TCAC de 13,65 % sur 2026-2031, les acheteurs équilibrant la souveraineté des données avec l'agilité et la rapidité de création de valeur. Les MES natifs en cloud et les modèles en tant que service réduisent la propriété de l'infrastructure, permettent des déploiements mondiaux plus rapides et standardisent les mises à niveau avec des packages de tests automatisés gérés par le fournisseur. Les plateformes conteneurisées ajoutent de la flexibilité en permettant des topologies hybrides qui maintiennent l'exécution de la production proche de la ligne tout en déplaçant l'analytique et le reporting vers le calcul cloud élastique. Les capacités à faible code dans les suites modernes aident les équipes de procédés à configurer des formulaires et des flux de travail sans code personnalisé lourd, ce qui comprime les cycles de conception et réduit le carnet de commandes informatique. Les fournisseurs renforcent également les contrôles de cybersécurité avec des pratiques de développement sécurisées, des conseils de durcissement et des packs de documentation qui s'alignent sur les attentes qualité des clients pour les opérations validées.
Les modèles hybrides servent désormais de pont pragmatique à mesure que les équipes modernisent les usines existantes tout en maintenant la disponibilité et le contrôle déterministe pour les étapes réglementées. À mesure que les CDMO développent leurs portefeuilles dans les régions, le SaaS multi-locataires devient attractif pour les recettes maîtresses standardisées, les flux de travail qualité spécifiques aux clients et un intégration plus rapide avec une gouvernance centralisée. L'orchestration cloud de la sérialisation soutient en outre les réseaux d'approvisionnement distribués en reliant les événements d'emballage, la mise en service et les messages d'expédition avec le contexte de lot pour les requêtes en aval. Le marché des systèmes d'exécution de la fabrication pharmaceutique converge donc vers la flexibilité de déploiement, où les options sur site, en cloud privé et en cloud public peuvent être combinées pour équilibrer le contrôle, l'évolutivité et la conformité. Les fournisseurs qui livrent du contenu pré-validé, des mises à jour gérées et des piles sécurisées par conception continueront de se distinguer à mesure que les acheteurs cherchent à simplifier le coût total de possession sans compromettre la préparation aux audits.
Par Fonctionnalité : L'Intégration de la Sérialisation Émerge comme le Module à la Croissance la Plus Rapide
Les dossiers de lots électroniques sont restés la fonctionnalité la plus importante en 2025 à 32,40 %, tandis que l'intégration de la sérialisation devrait être la capacité à la croissance la plus rapide à un TCAC de 12,78 % sur 2026-2031, la traçabilité interopérable devenant une attente de base. La DSCSA et les directives mondiales connexes exigent un échange de données interopérable qui lie les numéros de série, les lots et les expéditions avec le contexte d'exécution des lots, ce qui pousse à une intégration plus profonde entre les MES et les référentiels de niveau 4. Les modules de sérialisation modernes agissent comme des gestionnaires de sites et des hubs de messagerie qui unifient les lignes d'emballage, les MES, les ERP et les systèmes nationaux en utilisant des normes comme EPCIS avec une mise à l'échelle cloud pour les événements de pointe. Dans les investigations qualité, de déviation et CAPA, les données de sérialisation sont désormais régulièrement référencées pour réduire la portée des rappels et identifier plus rapidement les lots de fournisseurs suspects. Le marché des systèmes d'exécution de la fabrication pharmaceutique aligne les EBR, la gestion des déviations et la sérialisation pour soutenir les rappels ciblés et une disposition plus rapide avec une forte intégrité des données.
À mesure que les référentiels s'étendent et que les règles spécifiques aux pays évoluent, des interfaces évolutives et des connecteurs gérés sur le cycle de vie réduisent le code personnalisé et le retravail de validation. Les plateformes de sérialisation natives en cloud pouvant fonctionner sur site, dans les clouds des clients ou en tant que SaaS géré aident à harmoniser les opérations dans les portefeuilles multi-régions. L'intégration avec les MES apporte également des pistes d'audit horodatées avec des signatures électroniques à chaque événement de mise en service, d'agrégation et de décommissionnement. Pour les fabricants, cette convergence soutient la révision par exception, les analyses de lots de référence et les améliorations continues ancrées dans des données cohérentes et interrogeables. La taille du marché des systèmes d'exécution de la fabrication pharmaceutique pour les modules axés sur la sérialisation est donc positionnée pour une croissance soutenue, la conformité et la résilience de la chaîne d'approvisionnement restant en tête des agendas des dirigeants.
Note: Les parts de segment de tous les segments individuels sont disponibles à l'achat du rapport
Par Utilisateur Final : Les Fabricants de Thérapies Cellulaires et Géniques Stimulent l'Expansion la Plus Rapide du Segment
Les fabricants pharmaceutiques représentaient 42,54 % en 2025, tandis que les fabricants de thérapies cellulaires et géniques devraient afficher un TCAC de 14,93 % sur 2026-2031, les opérations spécifiques aux patients nécessitant une orchestration numérique approfondie. La fabrication centrée sur le patient nécessite une chaîne d'identité et une chaîne de custody de bout en bout appliquées électroniquement à chaque étape, ce qui crée une demande pour l'orchestration intégrée aux MES et les points de contrôle qualité. Les fournisseurs lancent des plateformes d'orchestration spécialisées et à système fermé qui réduisent les empreintes de salles blanches et permettent à un seul opérateur de traiter plusieurs lots de patients tout en maintenant l'isolation et la traçabilité. Les MES en cloud entrent également dans les environnements cliniques et commerciaux précoces pour accélérer la mise en place mondiale et maintenir la documentation de validation à jour avec des mises à jour fréquentes dans le cadre d'un service géré. Le marché des systèmes d'exécution de la fabrication pharmaceutique étend donc sa couverture pour les vérifications de chaîne d'identité, le suivi des doses sérialisées et la planification sensible au temps tout en garantissant des pistes d'audit conformes.
Les fabricants biopharmaceutiques continuent de standardiser les EBR et la gestion des déviations pour les opérations biologiques complexes où des volumes de données élevés et une surveillance continue exigent des contrôles d'intégrité robustes. Les CDMO s'appuient sur le SaaS multi-locataires et les bibliothèques de modèles pour intégrer rapidement les clients et harmoniser les processus qualité dans des portefeuilles de produits diversifiés. L'interopérabilité avec les LIMS et la sérialisation garantit que les matériaux, les échantillons et les doses restent étroitement liés au contexte de lot pour la libération et le reporting de pharmacovigilance. En conséquence, le secteur des systèmes d'exécution de la fabrication pharmaceutique élargit ses ensembles de fonctionnalités pour soutenir les transitions cliniques vers commerciales avec des recettes standardisées, des données maîtresses de référence et un contrôle des changements gouverné. Le marché des systèmes d'exécution de la fabrication pharmaceutique continuera de prioriser les modules qui gèrent les produits sérialisés, la planification des patients et l'analytique multi-sites qui raccourcissent le délai de mise à l'échelle.
Analyse Géographique
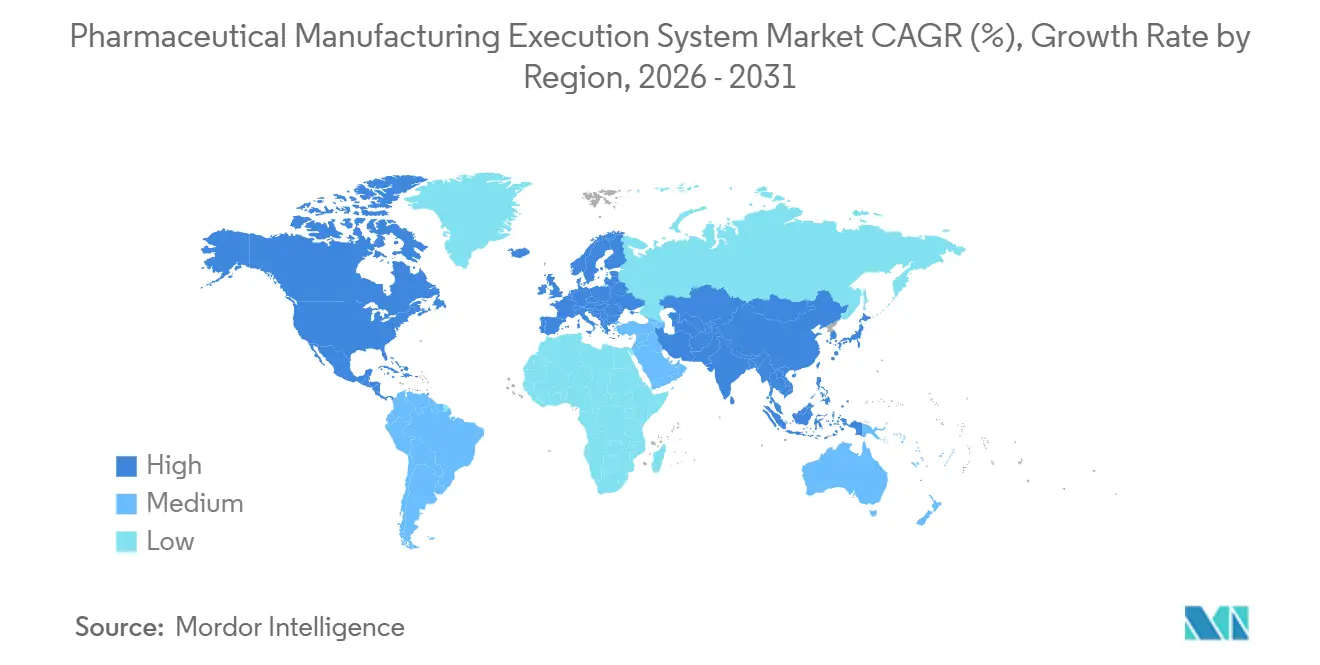
L'Amérique du Nord détenait 37,23 % de la part du marché des systèmes d'exécution de la fabrication pharmaceutique en 2025, ancrée par des cadres réglementaires matures et une base profonde d'innovateurs dans les pôles biotechnologiques. Les priorités des acheteurs en 2026 se concentrent sur les déploiements MES activés par le cloud qui préservent l'état validé tout en améliorant la vitesse de changement dans plusieurs usines. Les grandes entreprises pharmaceutiques et les CDMO leaders poursuivent les modernisations des sites hérités pour standardiser les EBR, intégrer la sérialisation et permettre la révision par exception dans des portefeuilles de produits diversifiés. La région investit également dans des plateformes de thérapie cellulaire à système fermé et des outils d'orchestration qui unifient la planification, l'exécution des lots et les preuves de contrôle qualité de manière conforme. Cette base soutient une croissance continue dans le marché des systèmes d'exécution de la fabrication pharmaceutique à mesure que les entreprises étendent les modèles multi-sites, renforcent l'intégrité des données et construisent la résilience de la chaîne d'approvisionnement.
L'Asie-Pacifique est la région à la croissance la plus rapide avec un TCAC de 15,83 % sur 2026-2031 pour la taille du marché des systèmes d'exécution de la fabrication pharmaceutique, portée par les extensions de capacité dans les produits biologiques et la montée en puissance des services CDMO. À mesure que les fabricants ajoutent de nouvelles lignes et installations, la demande augmente pour des EBR standardisés, des options cloud validées et des mises à niveau gérées par les fournisseurs qui réduisent le délai de qualification. Les CDMO régionaux adoptent du contenu MES modulaire pour intégrer rapidement les commanditaires et maintenir des pratiques qualité harmonisées dans des portefeuilles multi-clients. Les fournisseurs travaillent également avec les clients sur des stratégies de connecteurs pour les équipements anciens et les systèmes ponctuels afin de minimiser le code personnalisé et de simplifier la validation. Ces priorités maintiennent le marché des systèmes d'exécution de la fabrication pharmaceutique axé sur l'interopérabilité, la mise à l'échelle cloud et les opérations sécurisées par conception dans l'empreinte de fabrication en expansion de l'APAC.
L'Europe continue de progresser grâce à une gouvernance des données standardisée, des attentes plus fortes en matière de cybersécurité et des approches de qualité par conception qui favorisent les systèmes numériques validés. Dans toute l'UE, l'harmonisation de la sérialisation, du suivi et de la traçabilité, et de la qualification au niveau des sites incite à un couplage plus étroit entre les MES, les ERP et les référentiels d'entreprise. Le marché des systèmes d'exécution de la fabrication pharmaceutique en Europe met également l'accent sur les déploiements cloud et hybrides qui préservent le contrôle local tout en centralisant l'analytique et les données maîtresses. À mesure que les fournisseurs approfondissent les capacités à faible code et le contenu pré-validé, les fabricants européens accélèrent les mises à niveau sans compromettre la discipline de validation, notamment dans les pôles de produits biologiques. Ces tendances renforcent une demande stable dans le marché des systèmes d'exécution de la fabrication pharmaceutique à mesure que les entreprises modernisent leurs opérations, étendent la couverture de sérialisation et développent les modèles multi-sites.
Paysage Concurrentiel
Le marché des systèmes d'exécution de la fabrication pharmaceutique reste concurrentiel avec les grands acteurs mondiaux de l'automatisation, les fournisseurs de logiciels d'entreprise et les challengers natifs en cloud répondant à des besoins d'acheteurs qui se chevauchent mais sont distincts. Les fournisseurs se différencient avec des services cloud validés, du contenu EBR prédéfini et une intégration éprouvée aux ERP et aux référentiels de sérialisation pour une création de valeur plus rapide. Les plateformes qui combinent exécution, qualité et analytique gagnent des parts au sein des comptes à mesure que les clients passent d'une numérisation ponctuelle à des opérations intégrées et à la révision par exception. Les acheteurs continuent de valoriser les flux de travail configurables, le développement sécurisé et les pistes d'audit de bout en bout, ce qui favorise les fournisseurs disposant de modèles validés et d'une gestion rigoureuse du cycle de vie.
Les mouvements stratégiques illustrent la direction du marché. Rockwell a introduit une version conteneurisée qui prend en charge les modèles de déploiement hybrides et cloud avec des installateurs automatisés et la cybersécurité intégrée dans le processus de développement, ce qui aide à standardiser les déploiements dans les usines. Körber a étendu une solution de sérialisation native en cloud qui intègre les lignes d'emballage, les MES et les ERP tout en gérant les diverses exigences nationales sous une plateforme gérée sur le cycle de vie. Honeywell a lancé une plateforme native en cloud assistée par IA qui relie le contrôle critique à la qualité numérique pour réduire les erreurs des méthodes papier et accélérer l'introduction numérique de nouveaux produits. Siemens a intégré le développement à faible code qui permet aux équipes de procédés de configurer des applications nativement, ce qui raccourcit les cycles de conception-validation et soutient les pratiques Pharma 4.0.
La livraison de valeur axée sur les services est également un thème définissant. Les fournisseurs et les intégrateurs regroupent des heures de conseil, du contenu pré-validé et des tests automatisés qui s'alignent sur les approches d'assurance fondées sur les risques et réduisent la charge de documentation des clients. Les architectures SaaS multi-locataires ciblent les CDMO qui ont besoin de modèles partagés et de flux de travail qualité spécifiques aux clients, tandis que les plateformes à système fermé pour la thérapie cellulaire réduisent les empreintes de salles blanches et augmentent le débit par opérateur. À travers ces mouvements, le marché des systèmes d'exécution de la fabrication pharmaceutique tend vers des stratégies modulaires, évolutives dans le cloud et axées sur l'interopérabilité qui accélèrent les déploiements sans diluer l'intégrité des données ou la préparation aux audits.
Leaders du Secteur des Systèmes d'Exécution de la Fabrication Pharmaceutique
ABB Ltd.
Emerson Electric Co.
Honeywell International Inc.
Körber AG
Rockwell Automation, Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements Récents du Secteur
- Mars 2026 : Sartorius a lancé la Plateforme de Thérapie Cellulaire Eveo, un système modulaire intégré pour la production de thérapie cellulaire autologue, permettant une augmentation quadruple de la production dans les espaces de salles blanches existants. Un opérateur peut traiter simultanément huit lots de patients, produisant plus de 350 doses annuellement contre environ 100 doses auparavant, réduisant potentiellement les coûts de fabrication des CAR-T d'environ 90 % grâce à une conception compacte et à l'automatisation des flux de travail.
- Mai 2025 : Rockwell Automation a lancé FactoryTalk PharmaSuite 12.00, introduisant le déploiement basé sur le cloud via des conteneurs Kubernetes avec compatibilité Linux, une installation automatisée via l'outil de configuration MICKA, et une cybersécurité renforcée développée selon des pratiques de développement sécurisé certifiées.
- Avril 2025 : Honeywell a introduit TrackWise Manufacturing, une plateforme native en cloud assistée par IA parmi les premières en sciences de la vie à intégrer les environnements de fabrication numérique et physique. La plateforme conteneurisée exploite le Contrôleur d'Opérations Unitaires de Honeywell pour le contrôle critique et intègre un cadre qualité pour la fabrication par qualité par conception, accélérant l'introduction des médicaments tout en réduisant les erreurs et les inefficacités des méthodes papier.
Portée du Rapport sur le Marché Mondial des Systèmes d'Exécution de la Fabrication Pharmaceutique
Selon la portée du rapport, un système d'exécution de la fabrication pharmaceutique (MES) est un système logiciel utilisé pour surveiller, contrôler et documenter les processus de fabrication de médicaments en temps réel. Il connecte les opérations en atelier avec les systèmes d'entreprise pour assurer une production efficace, l'intégrité des données et la visibilité des processus. Dans les environnements pharmaceutiques, le MES est essentiel pour gérer les dossiers de lots électroniques, assurer la conformité réglementaire et permettre la traçabilité complète des matériaux et des processus.
Le marché des systèmes d'exécution de la fabrication pharmaceutique est segmenté par composant, déploiement, fonctionnalité, utilisateur final et géographie. Par composant, le marché est segmenté en logiciels et services. Par déploiement, le marché est segmenté en sur site et cloud / SaaS. Par fonctionnalité, le marché est segmenté en dossiers de lots électroniques (EBR), gestion des recettes/flux de travail, gestion des équipements, intégration des déviations et CAPA, intégration de la sérialisation, et autres. Par utilisateur final, le marché est segmenté en fabricants pharmaceutiques, fabricants biopharmaceutiques, fabricants de thérapies cellulaires et géniques, et CMO / CDMO. Par géographie, le marché est segmenté en Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud. Le rapport de marché couvre également les tailles de marché estimées et les tendances du marché pour 17 pays dans les principales régions du monde. Le rapport offre la valeur de marché (en USD) pour les segments ci-dessus.
| Logiciels |
| Services |
| Sur Site |
| Cloud / SaaS |
| Dossiers de Lots Électroniques (EBR) |
| Gestion des Recettes / Flux de Travail |
| Gestion des Équipements |
| Intégration des Déviations et CAPA |
| Intégration de la Sérialisation |
| Autres |
| Fabricants Pharmaceutiques |
| Fabricants Biopharmaceutiques |
| Fabricants de Thérapies Cellulaires et Géniques |
| CMO / CDMO |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Inde | |
| Japon | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par Composant | Logiciels | |
| Services | ||
| Par Déploiement | Sur Site | |
| Cloud / SaaS | ||
| Par Fonctionnalité | Dossiers de Lots Électroniques (EBR) | |
| Gestion des Recettes / Flux de Travail | ||
| Gestion des Équipements | ||
| Intégration des Déviations et CAPA | ||
| Intégration de la Sérialisation | ||
| Autres | ||
| Par Utilisateur Final | Fabricants Pharmaceutiques | |
| Fabricants Biopharmaceutiques | ||
| Fabricants de Thérapies Cellulaires et Géniques | ||
| CMO / CDMO | ||
| Par Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Inde | ||
| Japon | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions Clés Répondues dans le Rapport
Quelle est la taille projetée et le TCAC du marché des systèmes d'exécution de la fabrication pharmaceutique jusqu'en 2031 ?
La taille du marché des systèmes d'exécution de la fabrication pharmaceutique devrait atteindre 4,02 milliards USD d'ici 2031, enregistrant un TCAC de 9,81 % sur 2026-2031.
Quel modèle de déploiement connaît la croissance la plus rapide dans le domaine des systèmes d'exécution de la fabrication pharmaceutique ?
Le Cloud/SaaS affiche la croissance la plus rapide avec un TCAC projeté de 13,65 % sur 2026-2031, les acheteurs adoptant des services validés et gérés par les fournisseurs pour la rapidité et l'évolutivité.
Quels domaines fonctionnels connaissent l'adoption la plus rapide ?
L'intégration de la sérialisation progresse le plus rapidement à mesure que la traçabilité interopérable devient obligatoire et étroitement couplée aux flux de travail MES pour une visibilité de bout en bout et un reporting conforme.
Qu'est-ce qui stimule l'adoption de la révision par exception dans la libération des lots ?
Les EBR numérisés avec des contrôles basés sur des règles, des déviations intégrées et une révision simultanée par l'assurance qualité raccourcissent les cycles de libération et améliorent la préparation aux audits par rapport aux processus à forte utilisation de papier.
Pourquoi la demande de MES augmente-t-elle dans les thérapies cellulaires et géniques ?
La production spécifique aux patients nécessite une chaîne d'identité et de custody rigoureuse, une orchestration spécialisée et une intégration avec les LIMS et la sérialisation, que le MES peut unifier avec des pistes d'audit conformes.
Comment les fournisseurs aident-ils à réduire la complexité et le coût des programmes MES ?
Les fournisseurs proposent des services cloud validés, des modèles prédéfinis et des heures de conseil pour accélérer les déploiements tout en maintenant l'intégrité des données et la discipline de validation.
Dernière mise à jour de la page le:



