Taille et Part du Marché de l'Étiquetage des Dispositifs Médicaux
Analyse du Marché de l'Étiquetage des Dispositifs Médicaux par Mordor Intelligence
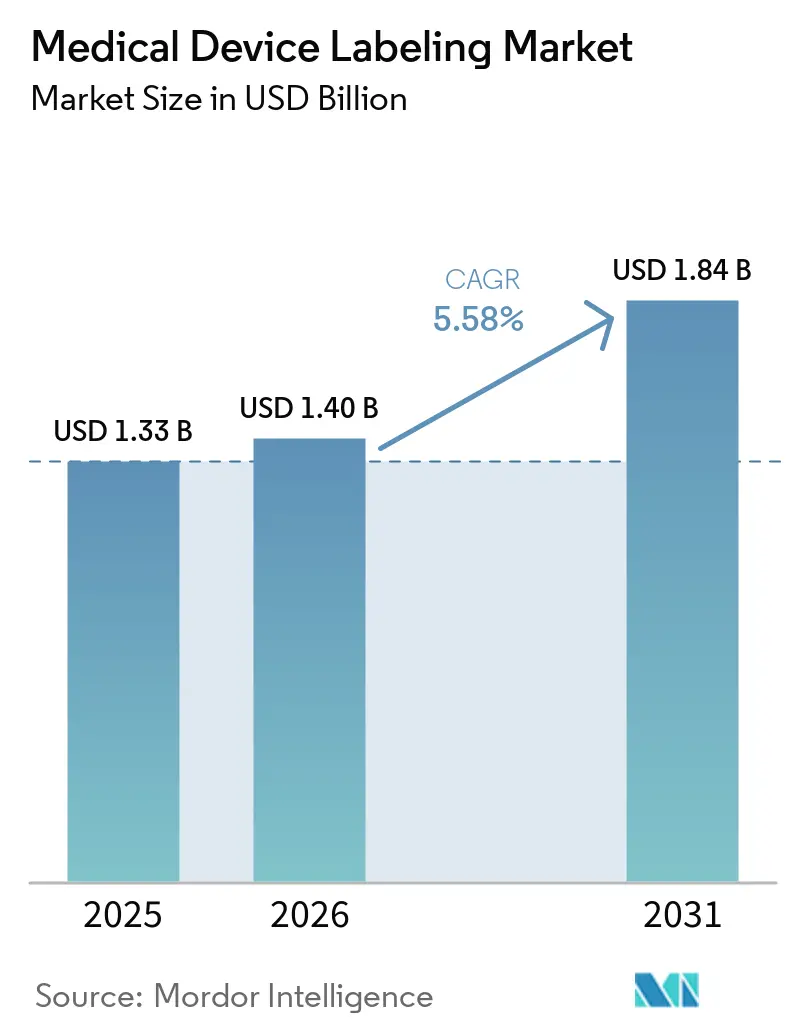
La taille du marché de l'étiquetage des dispositifs médicaux était évaluée à 1,33 milliard USD en 2025 et devrait croître de 1,40 milliard USD en 2026 pour atteindre 1,84 milliard USD d'ici 2031, à un CAGR de 5,58 % durant la période de prévision (2026-2031).
La croissance de la demande reflète l'accélération des mandats d'identification unique des dispositifs (UDI), l'adoption plus large des instructions d'utilisation électroniques (eIFU) et la conformité multilingue croissante qui transforme les étiquettes en vecteurs de données critiques plutôt qu'en simples marqueurs passifs [1]U.S. Food and Drug Administration, Notions de base sur l'UDI - Système d'identification unique des dispositifs,
fda.gov. Les hôpitaux s'appuient sur des codes QR ou Data Matrix sérialisés pour automatiser les flux de rappel, tandis que les fabricants font face à une multiplication des références de gestion des stocks, chaque variante linguistique nécessitant désormais une conception d'étiquette dédiée. La consolidation parmi les convertisseurs d'étiquettes est en cours, car les entreprises de dispositifs négocient des remises sur volume et exigent une impression compatible avec la stérilisation certifiée ISO 13485. Parallèlement, le marquage direct des pièces sur les instruments réutilisables réduit l'utilisation des étiquettes externes pour les dispositifs orthopédiques et d'endoscopie, obligeant les convertisseurs à se repositionner vers l'encodage RFID et l'impression multi-substrats pour défendre leurs parts de marché.
Principaux Enseignements du Rapport
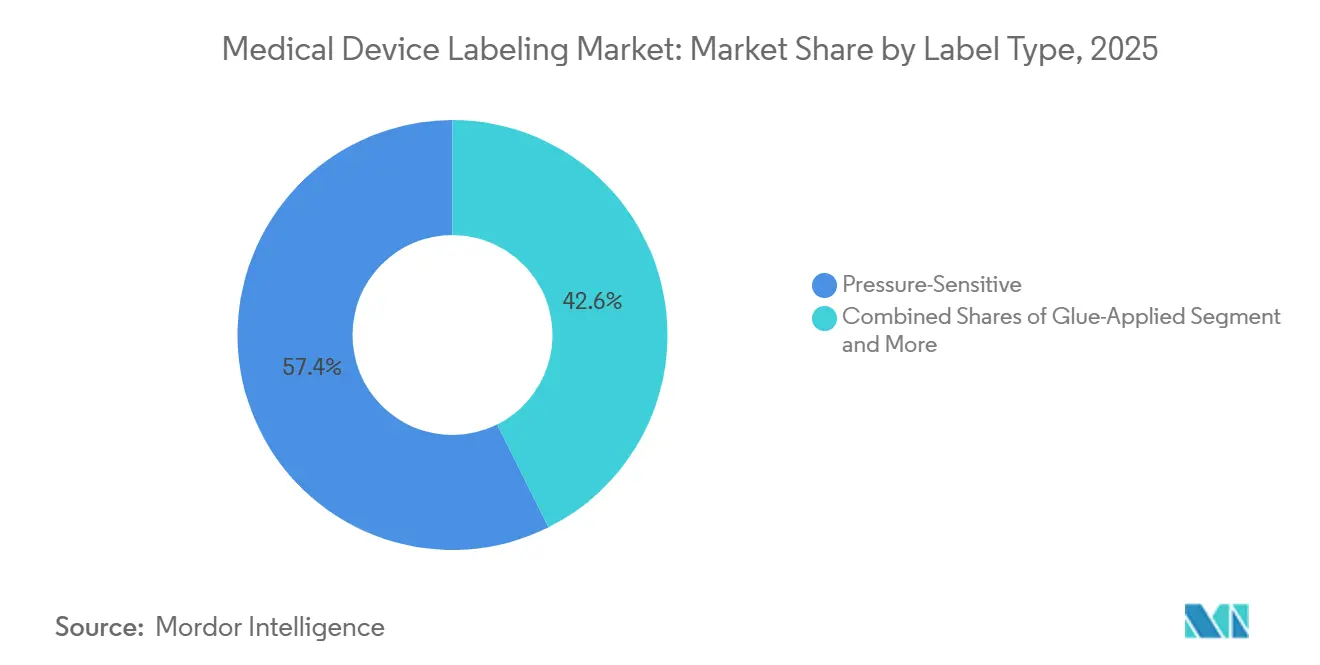
- Par type d'étiquette, les constructions autocollantes ont représenté 57,37 % de la part du marché de l'étiquetage des dispositifs médicaux en 2025, tandis que les étiquettes encollées ont affiché le CAGR le plus rapide, prévu à 5,89 % jusqu'en 2031.
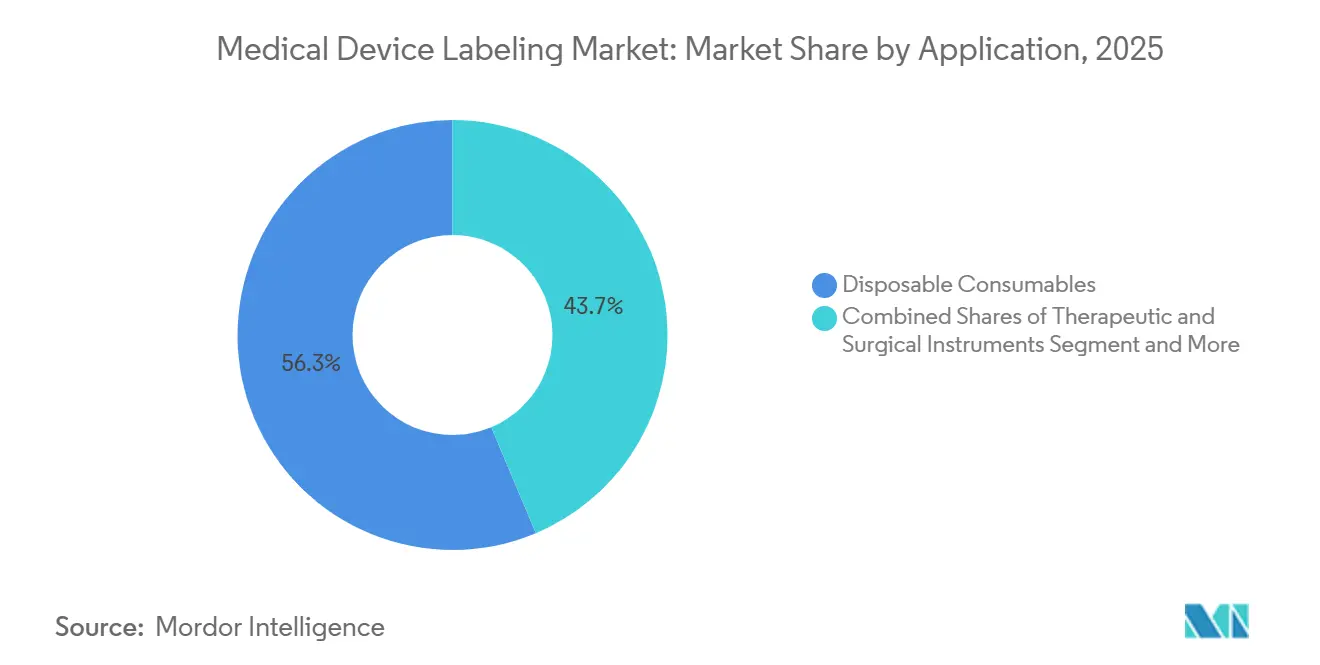
- Par application, les consommables jetables ont représenté 56,34 % de la taille du marché de l'étiquetage des dispositifs médicaux en 2025, tandis que les instruments thérapeutiques et chirurgicaux progressent à un CAGR de 6,12 % jusqu'en 2031.
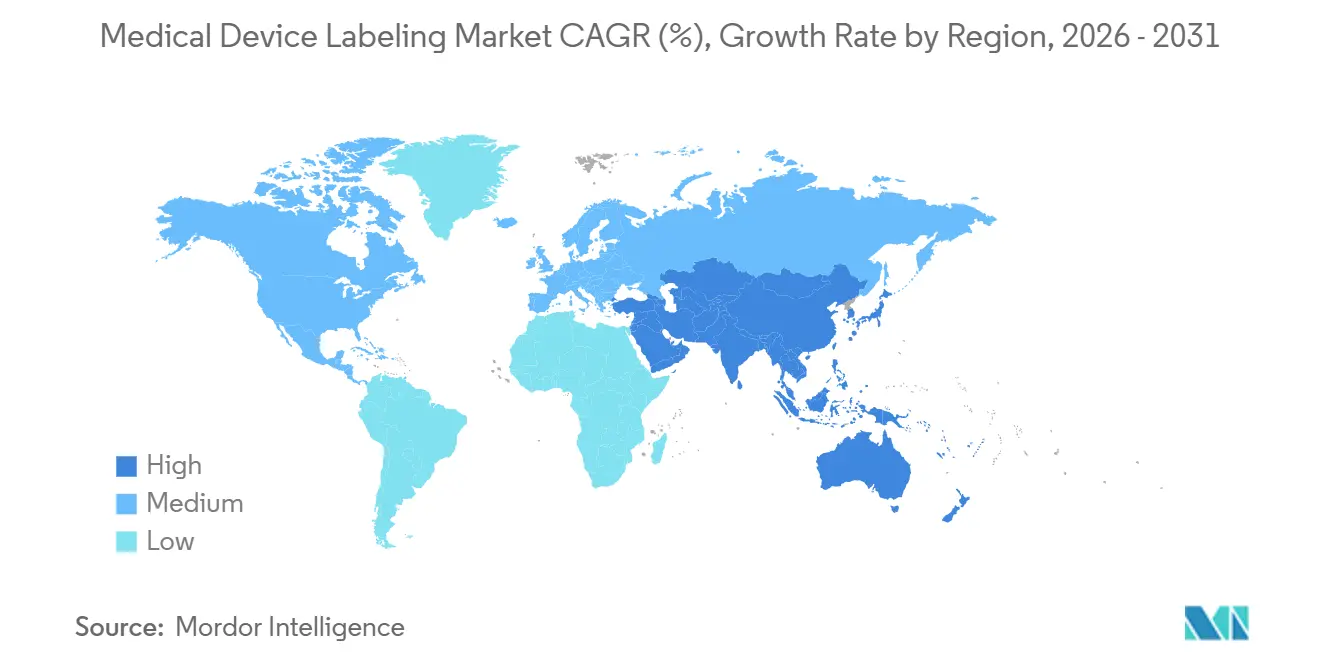
- Par géographie, l'Amérique du Nord a représenté 45,85 % des revenus en 2025, mais l'Asie-Pacifique devrait croître à un CAGR de 6,08 % jusqu'en 2031.
Note : La taille du marché et les prévisions figurant dans ce rapport sont générées à l'aide du cadre d'estimation exclusif de Mordor Intelligence, mis à jour avec les dernières données et informations disponibles en janvier 2026.
Tendances et Perspectives du Marché Mondial de l'Étiquetage des Dispositifs Médicaux
Analyse de l'Impact des Facteurs de Croissance
| Facteur de Croissance | (~) % d'Impact sur le CAGR Prévu | Pertinence Géographique | Horizon Temporel de l'Impact |
|---|---|---|---|
| Les mandats UDI mondiaux et les soumissions aux bases de données élargissent les données d'étiquetage et les exigences de codes-barres en double format | +1.2% | Mondial ; Amérique du Nord et UE en tête | Moyen terme (2-4 ans) |
| Les règles de traduction multilingue MDR/IVDR augmentent les références d'étiquettes et le volume de contenu | +0.9% | Europe ; répercussions au Royaume-Uni et en Suisse | Court terme (≤ 2 ans) |
| La demande croissante de dispositifs à usage domestique, portables et POCT stimule la demande d'étiquettes durables et conviviales pour les patients | +0.8% | Amérique du Nord et Europe en tête ; centres urbains d'Asie-Pacifique | Moyen terme (2-4 ans) |
| Les besoins accrus en rappels et en traçabilité accélèrent l'étiquetage UDI enrichi en codes-barres 2D | +0.7% | Mondial ; application la plus stricte dans les juridictions FDA et UE | Court terme (≤ 2 ans) |
| Adoption d'étiquettes intelligentes RFID/NFC pour la traçabilité au niveau de l'article dans les kits chirurgicaux et les implants | +0.6% | Hôpitaux d'Amérique du Nord et d'Europe ; projets pilotes en Asie-Pacifique | Long terme (≥ 4 ans) |
| Les flux de traitement stérile stimulent l'utilisation des étiquettes indicatrices et de la documentation | +0.5% | Hôpitaux et centres de chirurgie ambulatoire à l'échelle mondiale | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Les Mandats UDI Mondiaux et les Soumissions aux Bases de Données Élargissent les Données d'Étiquetage et les Exigences de Codes-Barres en Double Format
La FDA américaine a intensifié l'application du GUDID en 2025, émettant des lettres d'avertissement lorsque le contenu des codes-barres et les champs de la base de données divergeaient, de sorte que les convertisseurs valident désormais les symboles 2D jusqu'aux étiquettes de 10 mm × 15 mm. La Chine a achevé son déploiement progressif de l'UDI en 2024, exigeant que les dispositifs de classe I portent des identifiants lisibles par machine, poussant les exportateurs à reconcevoir les étiquettes pour le texte bilingue et les symbologies GS1 ou HIBC [2]Administration nationale des produits médicaux, Système d'identification unique des dispositifs (UDI),
nmpa.gov.cn. Le Japon, Singapour, la Malaisie et le Brésil ont adopté des cadres similaires, ce qui signifie qu'un même modèle de dispositif peut être expédié avec cinq variantes d'étiquettes régionales ou plus. Ces mandats poussent les entreprises de dispositifs vers des systèmes de gestion des étiquettes en nuage qui automatisent la gestion des versions des maquettes et le suivi des modifications réglementaires.
Les Règles de Traduction Multilingue MDR/IVDR Augmentent les Références d'Étiquettes et le Volume de Contenu
En vertu du règlement UE 2025/1234, en vigueur depuis juillet 2025, les dispositifs à usage professionnel peuvent remplacer les brochures papier par des eIFU, mais chaque langue nécessite toujours un lien QR unique sur l'étiquette, multipliant les références [3]Commission européenne, Dispositifs médicaux - Nouvelles réglementations - Orientations,
ec.europa.eu. Une seule pompe à perfusion peut nécessiter 24 conceptions d'étiquettes pour le bloc, augmentant le risque de stocks car les stocks imprimés en allemand ne peuvent légalement pas être expédiés en Espagne. Les fournisseurs de traduction signalent une hausse de 30 % des projets d'étiquettes de dispositifs depuis 2024, et les convertisseurs qui proposent une validation linguistique en interne remportent des contrats en raccourcissant les délais de certification.
La Demande Croissante de Dispositifs à Usage Domestique, Portables et POCT Stimule la Demande d'Étiquettes Durables et Conviviales pour les Patients
Les orientations de la FDA publiées en 2024 obligent les fabricants à tester la lisibilité auprès des utilisateurs non professionnels, faisant passer la taille des polices de 6 points à au moins 8 points et exigeant des avertissements en langage clair. Les moniteurs de glycémie en continu et les pompes portables nécessitent des étiquettes capables de résister à la transpiration, aux désinfectants et à des périodes de port de 10 à 14 jours sans irritation cutanée. Les ventes de dispositifs à usage domestique aux États-Unis ont augmenté de 12 % en 2025 à la suite de l'extension du remboursement pour la surveillance à distance, stimulant directement les volumes d'étiquettes.
Les Besoins Accrus en Rappels et en Traçabilité Accélèrent l'Étiquetage UDI Enrichi en Codes-Barres 2D
La FDA a enregistré 87 rappels de dispositifs de classe I en 2024, et les hôpitaux ont répondu en intégrant les scans de codes-barres dans les routines d'admission et de stérilisation. Les identifiants d'application de GS1 permettent à un seul Data Matrix de contenir le numéro de série, le lot et la date d'expiration, minimisant l'espace sur l'étiquette tout en maximisant la densité des données. La base de données européenne EUDAMED, obligatoire pour les nouvelles inscriptions depuis 2024, lie davantage les étiquettes physiques aux enregistrements en nuage pour la surveillance post-commercialisation
Analyse de l'Impact des Facteurs Limitants
| Facteur Limitant | (~) % d'Impact sur le CAGR Prévu | Pertinence Géographique | Horizon Temporel de l'Impact |
|---|---|---|---|
| La charge de conformité et les mises à jour réglementaires fréquentes augmentent les coûts et les délais de mise sur le marché pour les étiqueteurs | -0.6% | Mondial, avec une pression aiguë dans l'UE (MDR/IVDR) et en Chine (NMPA) | Court terme (≤ 2 ans) |
| Le paysage fragmenté de la conversion d'étiquettes intensifie la pression sur les prix et la compression des marges | -0.4% | Mondial, plus sévère en Amérique du Nord et en Europe où la consolidation des acheteurs est avancée | Moyen terme (2-4 ans) |
| Le marquage direct des pièces (UDI permanent) déplace certaines étiquettes externes pour les instruments réutilisables | -0.5% | Amérique du Nord et Europe, sous l'impulsion des orientations FDA et EU MDR sur le marquage direct | Moyen terme (2-4 ans) |
| L'adoption des eIFU réduit l'étiquetage par brochures/notices papier pour les dispositifs à usage professionnel | -0.3% | Europe en tête après le règlement 2025/1234 ; Amérique du Nord et Asie-Pacifique suivent | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
La Charge de Conformité et les Mises à Jour Réglementaires Fréquentes Augmentent les Coûts et les Délais de Mise sur le Marché pour les Étiqueteurs
L'UE a publié 89 documents d'orientation entre 2021 et 2025, chacun pouvant modifier le contenu des étiquettes, tandis que les arriérés des organismes notifiés s'étendent jusqu'à 12 mois, forçant de multiples révisions de maquettes coûtant entre 5 000 et 15 000 USD par itération. La Chine a publié 14 circulaires UDI en 2024, et l'application provinciale incohérente ajoute de l'incertitude pour les exportateurs. Les petits fabricants consacrent jusqu'à une part notable de leurs ventes aux affaires réglementaires, contre 2 % pour les multinationales, accélérant la consolidation du secteur.
Le Paysage Fragmenté de la Conversion d'Étiquettes Intensifie la Pression sur les Prix et la Compression des Marges
Plus de 300 convertisseurs régionaux sont en concurrence, dont beaucoup sont des opérateurs sur un seul site avec un pouvoir de négociation limité. Les contrats d'achat groupé concentrent une part significative des dépenses en étiquettes auprès de cinq convertisseurs, tandis que les clients exigent des réductions de prix annuelles de 2 à 3 % malgré la hausse des coûts de certification ISO 13485 et de salle blanche. Les marges brutes se sont comprimées de 28 % en 2020 à 22 % en 2025, entraînant des sorties du marché et des regroupements par capital-investissement. Le marquage direct des pièces érode davantage la demande d'étiquettes pour instruments réutilisables.
Analyse des Segments
Par Type d'Étiquette : La Chimie des Adhésifs Détermine la Compatibilité avec la Stérilisation
Les étiquettes autocollantes ont représenté 57,37 % du marché de l'étiquetage des dispositifs médicaux en 2025, portées par leur compatibilité avec les lignes d'application de 300 à 600 étiquettes par minute et la stérilisation par rayonnement gamma, oxyde d'éthylène et vapeur. Les adhésifs acryliques ou caoutchouc maintiennent leur résistance à la liaison jusqu'à 50 kGy d'irradiation sans jaunissement. Les étiquettes encollées ou à colle humide devraient croître à 5,89 % jusqu'en 2031, le taux le plus rapide, car les entreprises pharmaceutiques conditionnent des injectables liquides dans des flacons en verre où l'adhésion permanente l'emporte sur la commodité du décollement et du recollage. Les systèmes à colle humide créent des liaisons mécaniques en pénétrant les substrats, empêchant le soulèvement lors de la condensation en chaîne du froid, mais ils nécessitent des temps de maintien de 10 à 15 secondes qui ralentissent les lignes à 150 à 250 unités par minute.
Les manchons rétractables représentaient une part notable du volume en 2025, privilégiés pour les produits combinés tels que les seringues préremplies avec aiguilles de sécurité intégrées, où les graphiques à 360 degrés justifient une prime de 30 à 40 %. Les étiquettes en moule restent une niche, appliquées lors du soufflage ou du moulage par injection de godets à spécimen, éliminant les étapes post-moulage. La directive européenne sur les plastiques à usage unique, en vigueur en 2024, exempte les dispositifs médicaux mais a incité à l'évaluation de faces recyclables correspondant à la résine du contenant. UPM Raflatac a lancé une construction sans doublure en 2025 qui réduit les déchets de matériaux de 15 % et diminue les coûts de fret, séduisant les fabricants soucieux de durabilité.
Note: Les parts de segment de tous les segments individuels sont disponibles à l'achat du rapport
Par Application : Les Instruments Chirurgicaux Dépassent les Consommables en Intégration RFID
Les consommables jetables ont représenté 56,34 % de la taille du marché de l'étiquetage des dispositifs médicaux en 2025, reflétant les 16 milliards de seringues utilisées annuellement aux seuls États-Unis. Pourtant, les instruments thérapeutiques et chirurgicaux se développent à 6,12 % jusqu'en 2031, la croissance d'application la plus rapide, car les hôpitaux achètent des équipements d'investissement et intègrent des étiquettes RFID dans les plateaux réutilisables. Une seule procédure orthopédique consomme 40 à 60 instruments, chacun étiqueté et stérilisé 200 à 300 fois sur cinq ans, générant une demande récurrente qui dépasse largement l'étiquetage unique des seringues. Les équipements de surveillance et de diagnostic représentaient des parts notables du volume en 2025, nécessitant des étiquettes durables capables de résister à des années de nettoyage à l'alcool isopropylique et à l'exposition aux UV.
Les dispositifs à usage domestique et portables remodèlent les spécifications des consommables. Les moniteurs de glycémie en continu nécessitent des adhésifs en silicone ou hydrocolloïde qui équilibrent un port de 10 à 14 jours avec un retrait sans douleur, remplaçant les acryliques agressifs. Les orientations de la FDA de 2024 sur l'étiquetage des patients imposent des tests de compréhension, conduisant à des polices plus grandes et des avertissements en langage clair. Les dispositifs de test au point de soins ont connu une croissance significative en 2025 avec le déplacement de la distribution vers les pharmacies, multipliant les variantes d'étiquettes car les dispositifs en vente libre nécessitent des instructions d'élimination conviviales pour les consommateurs, absentes des équivalents professionnels. La convergence de la sérialisation UDI, de l'adoption du RFID et de la conception centrée sur le patient élève la complexité technique et la valeur unitaire dans toutes les applications, même si la tarification concurrentielle comprime les marges des convertisseurs.
Note: Les parts de segment de tous les segments individuels sont disponibles à l'achat du rapport
Analyse Géographique
L'Amérique du Nord a détenu 45,85 % de la part du marché de l'étiquetage des dispositifs médicaux en 2025, ancrée par l'application de l'UDI par la FDA et les exigences de synchronisation du GUDID. L'agence a émis 14 lettres d'avertissement en 2024 pour non-conformité, ciblant les fabricants nationaux et étrangers. Le Canada a aligné sa réglementation sur les dispositifs médicaux sur les normes de la FDA en 2024 et a introduit le signalement obligatoire des événements indésirables liés aux étiquettes, imposant un étiquetage bilingue français-anglais pour le Québec. La COFEPRIS du Mexique a adopté l'UDI en 2025, créant un bloc réglementaire nord-américain qui simplifie la conception mais impose des obligations trilingues anglais-français-espagnol pour la distribution dans le cadre de l'ACEUM.
L'Europe navigue dans les transitions MDR et IVDR qui imposent des instructions en langue locale en Allemagne, en France, en Italie, en Espagne et en Pologne, fragmentant les références d'étiquettes. Le marquage UKCA du Royaume-Uni, obligatoire en 2024, exige des étiquettes séparées pour la Grande-Bretagne et l'Irlande du Nord, qui suit le MDR de l'UE, forçant des stocks parallèles. Le règlement 2025/1234, en vigueur depuis juillet 2025, autorise les eIFU pour les dispositifs professionnels mais maintient les exigences de code QR et d'URL pour chaque langue, multipliant les conceptions sans réduire les coûts d'impression.
L'Asie-Pacifique devrait croître à 6,08 % jusqu'en 2031, le CAGR régional le plus rapide. La Chine a achevé le déploiement de l'UDI en 2024, rendant obligatoires les identifiants des dispositifs de classe I dans la base de données de la NMPA et stimulant l'adoption des codes-barres en double format. Le programme d'incitation liée à la production de l'Inde canalise 1,4 milliard USD dans la fabrication nationale, favorisant l'approvisionnement local en étiquettes et attirant les investissements des convertisseurs multinationaux à Pune, Ahmedabad et Chennai. La PMDA du Japon a accepté les eIFU en 2024, s'alignant sur les précédents de la FDA et de l'UE, tout en maintenant des normes strictes de lisibilité en japonais et en kanji sur les étiquettes. Le Moyen-Orient et l'Afrique, l'Amérique du Sud et les marchés plus petits d'Asie-Pacifique représentaient collectivement une part notable des revenus en 2025. L'ANVISA du Brésil a publié des lignes directrices UDI en 2024, exigeant le codage GS1 ou HIBC pour les dispositifs de classe III et IV d'ici 2026. La TGA d'Australie a harmonisé les exigences UDI avec les cadres de la FDA et de l'UE en 2024, simplifiant la conception dans la région Pacifique, tandis que la MFDS de Corée du Sud a rendu obligatoire l'étiquetage en langue coréenne pour les importations.
Paysage Concurrentiel
Le marché de l'étiquetage des dispositifs médicaux reste fragmenté, les 10 premiers convertisseurs captant la majorité des revenus mondiaux. CCL Industries a acquis trois convertisseurs d'étiquettes médicales en Amérique du Nord et en Europe durant 2024-2025, intégrant les listes de clients dans sa division Santé & Spécialités et proposant des solutions RFID en vente croisée. Avery Dennison a investi 25 millions USD dans l'infrastructure RFID en 2025, installant des lignes d'encodage d'inlays dans ses installations d'Oegstgeest, aux Pays-Bas, et de Mentor, dans l'Ohio, pour servir les fabricants d'instruments chirurgicaux et d'implants. Les convertisseurs plus petits se taillent des niches dans des applications à haute complexité telles que les étiquettes livret multicouches, les constructions sans doublure et les produits hybrides indicateur-code-barres, où la différenciation technique compense la pression tarifaire des produits de base.
Des opportunités dans les espaces non exploités émergent à l'intersection de l'étiquetage numérique et des dispositifs connectés. Schreiner Group a déposé quatre brevets en 2024-2025 pour des constructions RFID capables de résister à 1 000 cycles de stérilisation et pour des conceptions d'antennes optimisées pour la traçabilité des instruments métalliques. L'intégration de la chaîne de blocs reste naissante, mais des projets pilotes de Johnson & Johnson et Medtronic en 2025 ont démontré des registres immuables reliant l'UDI sérialisé aux dossiers de fabrication et aux résultats cliniques. La certification ISO 13485 est devenue un prérequis, les fabricants de dispositifs exigeant que les convertisseurs démontrent un contrôle validé des modifications de maquettes, un suivi de la généalogie des lots et une assurance de stérilité, favorisant les acteurs de grande taille dotés d'équipes dédiées aux affaires réglementaires et d'une inspection automatisée par rapport aux petits ateliers qui s'appuient sur des contrôles qualité manuels.
Leaders du Secteur de l'Étiquetage des Dispositifs Médicaux
CCL Industries
Avery Dennison
Schreiner Group
Brady Corporation
All4Labels Group
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements Récents du Secteur
- Février 2026 : Danaher a finalisé l'acquisition de Masimo pour 9,9 milliards USD, une avancée majeure dans les soins aux patients axés sur la surveillance et les données.
- Mars 2025 : CCL Industries a finalisé l'acquisition de CleanMark Labels, un convertisseur américain spécialisé dans les étiquettes autocollantes pour salle blanche destinées aux dispositifs de classe II et III, ajoutant une capacité certifiée ISO 13485 en Caroline du Nord.
- Janvier 2025 : La division MediPharm de Schreiner Group a lancé une étiquette hybride indicateur chimique et code-barres 2D qui intègre la validation de la stérilisation à la vapeur avec le suivi automatisé des plateaux, réduisant le temps de documentation du traitement stérile de 40 % lors de déploiements pilotes dans 12 hôpitaux européens.
Périmètre du Rapport Mondial sur le Marché de l'Étiquetage des Dispositifs Médicaux
Selon le périmètre du rapport, l'étiquetage des dispositifs médicaux est un cadre de communication complet qui va bien au-delà des simples autocollants apposés sur un produit. Il englobe toutes les informations écrites, imprimées ou graphiques fournies avec un dispositif, y compris son emballage, les instructions d'utilisation (IFU), les manuels d'utilisation et même les supports promotionnels.
Le marché de l'étiquetage des dispositifs médicaux est segmenté par type d'étiquette, applications et géographie. Par type d'étiquette, le marché est segmenté en étiquettes autocollantes, encollées, manchons rétractables et étiquettes en moule. Par type de plateforme, le marché est segmenté en consommables jetables, équipements de surveillance & de diagnostic, et instruments thérapeutiques & chirurgicaux. Géographiquement, le marché est segmenté en Amérique du Nord, Europe, région Asie-Pacifique, Moyen-Orient & Afrique et Amérique du Sud. Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays dans les principales régions du monde. Pour chaque segment, la taille du marché et les prévisions sont fournies en termes de valeur (USD).
| Autocollantes |
| Encollées |
| Manchons rétractables |
| Étiquettes en moule |
| Consommables jetables |
| Équipements de surveillance et de diagnostic |
| Instruments thérapeutiques et chirurgicaux |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par Type d'Étiquette | Autocollantes | |
| Encollées | ||
| Manchons rétractables | ||
| Étiquettes en moule | ||
| Par Application | Consommables jetables | |
| Équipements de surveillance et de diagnostic | ||
| Instruments thérapeutiques et chirurgicaux | ||
| Par Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions Clés Répondues dans le Rapport
Quelle est la valeur projetée d'ici 2031 ?
Le marché de l'étiquetage des dispositifs médicaux devrait atteindre 1,84 milliard USD d'ici 2031, avec un CAGR de 5,58 % à partir de 2026.
Quel type d'étiquette détient la plus grande part ?
Les étiquettes autocollantes ont représenté 57,37 % de la part en 2025, portées par leur compatibilité avec les lignes à grande vitesse et les cycles de stérilisation.
Quel segment d'application connaît la croissance la plus rapide ?
Les instruments thérapeutiques et chirurgicaux se développent à 6,12 % jusqu'en 2031, portés par l'intégration du RFID dans les plateaux d'instruments réutilisables.
Quelle région est en tête en termes de revenus ?
L'Amérique du Nord a représenté 45,85 % des revenus en 2025, ancrée par l'application de l'UDI par la FDA et les audits de soumission au GUDID.
Dernière mise à jour de la page le:



