Taille et Part du Marché des TIC pour la Santé et les Dispositifs Médicaux
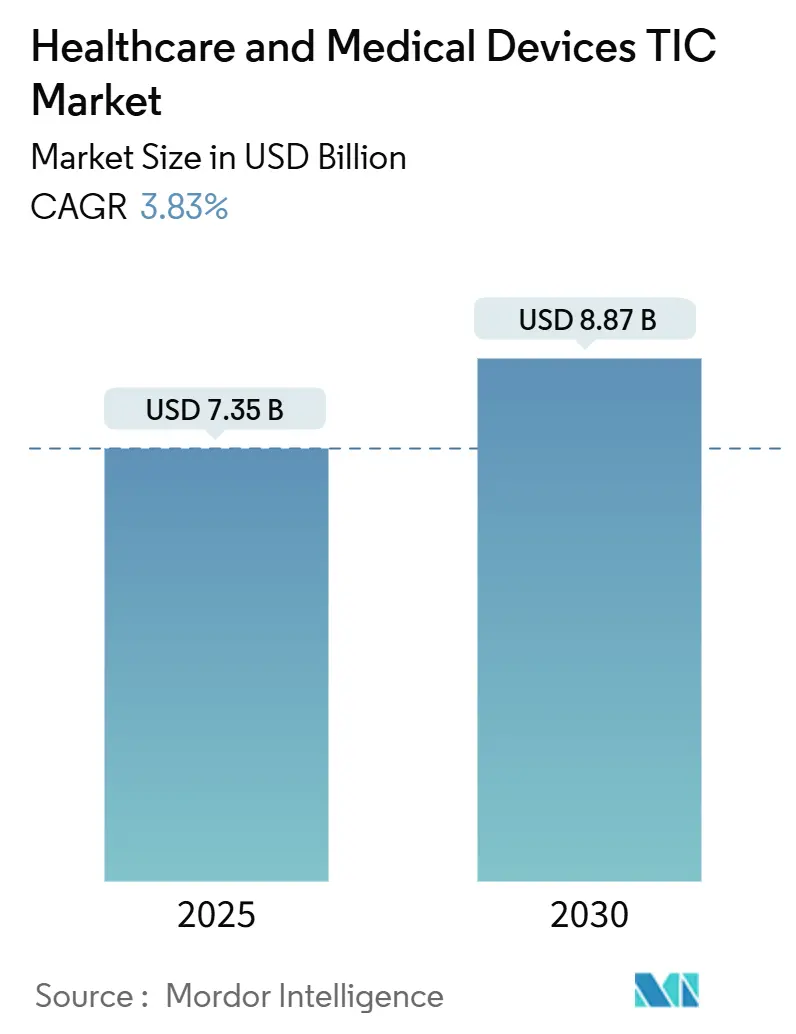
Analyse du Marché des TIC pour la Santé et les Dispositifs Médicaux par Mordor Intelligence
Le marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux est actuellement évalué à 7,35 milliards USD en 2025 et devrait atteindre 8,87 milliards USD d'ici 2030, reflétant un CAGR de 3,83 % durant la période de prévision. Les cadres de conformité mondiaux obligatoires, la complexité croissante des dispositifs et l'harmonisation réglementaire accélérée ancrent une demande stable même lorsque les budgets de santé se resserrent. La concentration manufacturière de l'Asie-Pacifique et l'évolution réglementaire rapide soutiennent la domination régionale, tandis que les rappels liés à la cybersécurité et les diagnostics assistés par l'IA élargissent le périmètre de validation. Les prestataires de TIC établis s'appuient sur des accréditations multijuridictionnelles et l'automatisation des laboratoires pour maintenir leur pouvoir de fixation des prix face aux spécialistes régionaux fragmentés. Les pénuries de talents accrues, notamment pour les auditeurs biomédicaux, et la hausse des coûts des modèles de biocompatibilité tempèrent les perspectives de croissance, mais d'importantes opportunités de consolidation et de spécialisation de niche persistent.
Points Clés du Rapport
- Par type de service, les services de test ont dominé avec 53,6 % de la part du marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux en 2024, tandis que les services de certification progressent à un CAGR de 4,2 % jusqu'en 2030.
- Par type d'approvisionnement, les modèles externalisés représentaient 69,3 % de la taille du marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux en 2024 et devraient se développer à un CAGR de 3,9 % entre 2025 et 2030.
- Par géographie, l'Asie-Pacifique a capturé 44,7 % de la part des revenus du marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux en 2024 ; la région devrait afficher le CAGR le plus rapide de 4,5 % jusqu'en 2030.
Tendances et Perspectives du Marché Mondial des TIC pour la Santé et les Dispositifs Médicaux
Analyse de l'Impact des Moteurs
| Moteur | (~) % d'Impact sur les Prévisions de CAGR | Pertinence Géographique | Calendrier d'Impact |
|---|---|---|---|
| Hausse de la complexité et de la miniaturisation des dispositifs | +0.8% | Mondial, avec une concentration en Amérique du Nord et en Asie-Pacifique | Moyen terme (2 à 4 ans) |
| Expansion de l'harmonisation réglementaire mondiale (MDSAP, IVDR) | +0.7% | Mondial, porté par l'Amérique du Nord, l'UE et l'adoption en Asie-Pacifique | Long terme (≥ 4 ans) |
| Croissance des diagnostics à domicile et des dispositifs de diagnostic portables | +0.6% | L'Amérique du Nord et l'UE sont primaires, l'Asie-Pacifique est émergente | Court terme (≤ 2 ans) |
| L'augmentation des rappels stimule les dépenses de tests préventifs | +0.5% | Mondial, avec l'impact le plus élevé en Amérique du Nord | Moyen terme (2 à 4 ans) |
| Protocoles de tests rapides assistés par l'IA | +0.4% | L'Amérique du Nord et l'UE sont en adoption précoce, et l'Asie-Pacifique suit. | Long terme (≥ 4 ans) |
| Demande de tests de remise en état dans le cadre de l'économie circulaire | +0.3% | L'UE en tête, adoption sélective en Amérique du Nord | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Hausse de la Complexité et de la Miniaturisation des Dispositifs
Les dispositifs portables combinent désormais des capteurs, une connectivité et des moteurs d'IA qui exigent une évaluation simultanée de la précision des capteurs, de l'électromagnétisme, de la fiabilité des logiciels et de la sécurité cutanée dans diverses conditions réelles. Les cycles de validation modernes doivent également vérifier l'apprentissage continu des algorithmes, ce qui conduit les fabricants à former des partenariats de test récurrents plutôt que des projets ponctuels.[1]FDA, "La FDA autorise le premier dispositif médical assisté par l'IA pour le test du syndrome d'apnée du sommeil à domicile," FDA.GOV Les protocoles à forte intensité de talents augmentent les coûts des projets tout en ancrant des revenus prévisibles pour les prestataires de TIC qui maintiennent des équipes multidisciplinaires et des outils de simulation avancés.
Expansion de l'Harmonisation Réglementaire Mondiale (MDSAP, IVDR)
Le cadre MDSAP permet à un seul audit de satisfaire cinq agences réglementaires, réduisant les dépenses de conformité des fabricants d'environ 30 à 40 %, tout en renforçant la demande pour les entreprises de TIC bénéficiant d'une reconnaissance simultanée aux États-Unis, au Canada, en Australie, au Japon et au Brésil.[2]Santé Canada, "Programme d'audit unique des dispositifs médicaux," CANADA.CA L'adoption de l'IVDR en Europe reflète cette tendance, élargissant les catégories de dispositifs soumis à des tests de performance diagnostique rigoureux et concentrant ainsi les activités auprès des prestataires accrédités à l'échelle mondiale.
Croissance des Diagnostics à Domicile et des Dispositifs de Diagnostic Portables
La FDA a autorisé plus de 50 dispositifs de santé numérique à usage domestique en 2024, notamment des moniteurs d'apnée du sommeil et de glycémie connectés aux smartphones, qui nécessitent des évaluations de cybersécurité, d'utilisabilité et de robustesse dans des environnements multiples, au-delà des tests classiques en laboratoire. L'économie des soins décentralisés encourage les payeurs à rembourser la surveillance à distance, élargissant les revenus pour les entreprises de TIC disposant de laboratoires de simulation à domicile et de compétences en tests de pénétration IoT.
L'Augmentation des Rappels Stimule les Dépenses de Tests Préventifs
Une hausse de 400 % des rappels de dispositifs entre 2013 et 2018, principalement due aux vulnérabilités logicielles et réseau, a poussé les fabricants à augmenter leurs budgets de test à 15-25 % des dépenses de développement, contre 8-12 % historiquement. La validation préventive compense désormais les coûts de rappel, en moyenne de 10 à 50 millions USD, ancrant des engagements plus robustes en phase précoce pour les spécialistes des TIC.
Analyse de l'Impact des Contraintes
| Contrainte | (~) % d'Impact sur les Prévisions de CAGR | Pertinence Géographique | Calendrier d'Impact |
|---|---|---|---|
| Pénurie d'auditeurs TIC biomédicaux qualifiés | -0.4% | Mondial, plus aiguë en Amérique du Nord et dans l'UE | Court terme (≤ 2 ans) |
| Réduction du financement par capital-risque dans les start-ups de technologie médicale | -0.3% | Mondial, avec l'impact le plus élevé en Amérique du Nord | Moyen terme (2 à 4 ans) |
| Cyberrisques liés à l'intégrité des données dans les dispositifs connectés | -0.2% | Mondial, concentré dans les marchés numériquement avancés | Long terme (≥ 4 ans) |
| Hausse des coûts des modèles animaux pour la biocompatibilité | -0.2% | Mondial, avec l'UE en tête pour l'adoption d'alternatives | Moyen terme (2 à 4 ans) |
| Source: Mordor Intelligence | |||
Pénurie d'Auditeurs TIC Biomédicaux Qualifiés
Le recrutement d'auditeurs spécialisés nécessite 5 à 7 ans de formation pluridisciplinaire ; les départs à la retraite dépassent les nouvelles recrues dans un rapport d'environ deux pour un, créant un déficit de personnel de 25 à 30 % et alimentant une inflation salariale annuelle de 15 à 20 %.[3]Bureau of Labor Statistics, "Scientifiques médicaux," BLS.GOV Les prestataires automatisent la saisie des données et les évaluations à distance pour atténuer les goulots d'étranglement, mais ne peuvent toujours pas capitaliser sur une expansion de capacité à court terme.
Réduction du Financement par Capital-Risque dans les Start-ups de Technologie Médicale
L'investissement mondial dans la technologie médicale a reculé à 19,1 milliards USD en 2024, contre un pic de 22,1 milliards USD en 2021, réduisant les pipelines de dispositifs en phase précoce et retardant les contrats de TIC jusqu'à des jalons plus tardifs. Les start-ups à trésorerie limitée compriment désormais les périmètres de validation, décalant le calendrier des revenus pour les prestataires de TIC.
Analyse des Segments
Par Type de Service : Les Services de Test Conservent la Primauté Tandis que les Certifications s'Accélèrent
Les services de test ont généré la plus grande part du marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux, soit 53,6 % en 2024, portés par les évaluations de matériaux selon la norme ISO 10993 et les contrôles obligatoires de compatibilité électromagnétique. L'étendue du segment couvre les protocoles de biocompatibilité, de sécurité électrique et de cybersécurité, chacun évoluant avec la connectivité des dispositifs et l'adoption de l'IA. Bien que la croissance se modère à mesure que certains tests se consolident dans des cadres harmonisés, la complexité croissante des conceptions soutient le volume et la résilience des marges.
Les services de certification, bien qu'ils représentent une part plus modeste de la taille du marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux, ont affiché le CAGR le plus rapide de 4,2 %. Les fabricants investissent de plus en plus dans des certifications à source unique qui satisfont simultanément le MDSAP et l'IVDR, échangeant des frais initiaux contre des lancements mondiaux plus rapides. Les services d'inspection, représentant environ un quart des revenus, bénéficient des mandats de transparence de la chaîne d'approvisionnement mais se développent plus lentement à mesure que les audits à distance gagnent du terrain.
Les effets de second ordre renforcent l'interaction entre les segments : les certifications avancées intègrent souvent des tests préalables, et les audits réussis alimentent des inspections de surveillance récurrentes. Les prestataires de TIC qui intègrent les trois offres sur des plateformes cloud monétisent les cycles de conformité de bout en bout, attirant à la fois les multinationales et les innovateurs aux ressources limitées.
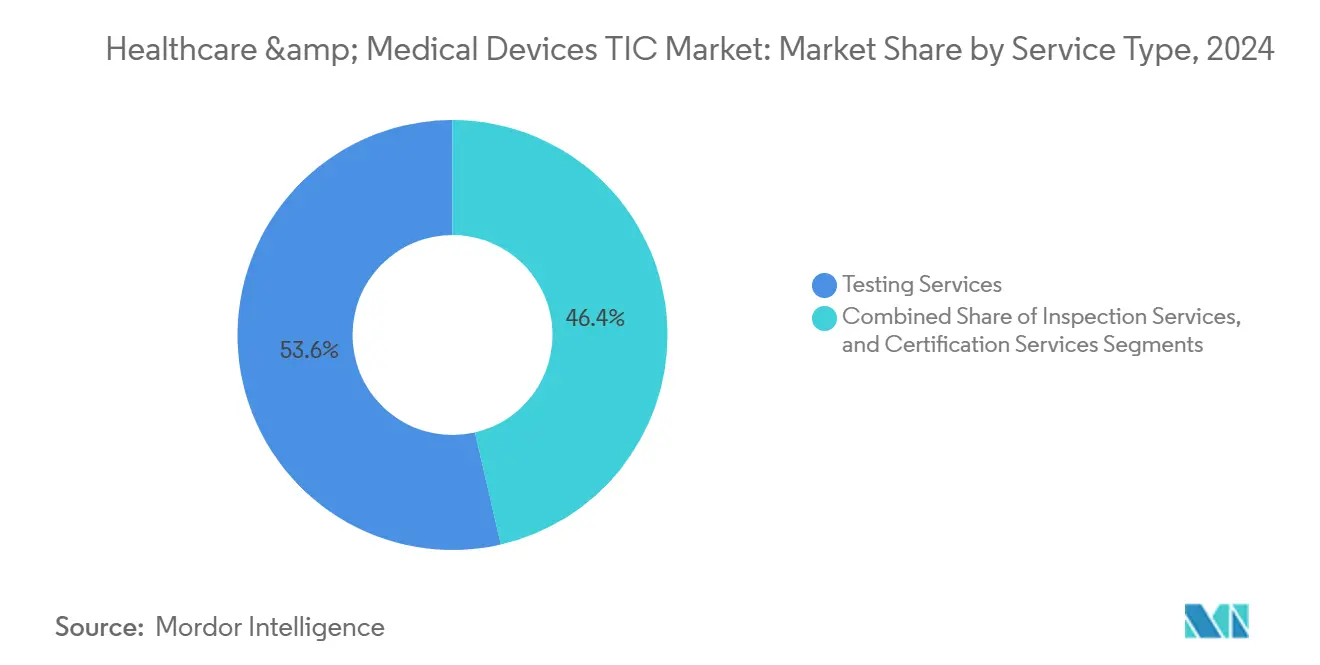
Note: Les parts de segment de tous les segments individuels sont disponibles à l'achat du rapport
Par Type d'Approvisionnement : L'Externalisation Continue de Dépasser les Modèles Internes
L'externalisation représentait 69,3 % de la part du marché des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux en 2024 et suit un CAGR de 3,9 % jusqu'en 2030. Les dépenses en capital croissantes pour les chambres spécialisées, les salles blanches et les laboratoires de cybersécurité — souvent de 10 à 50 millions USD par installation — rendent les partenariats externes économiques pour les start-ups et même les grands équipementiers cherchant une capacité supplémentaire.
Les capacités internes, bien que stratégiques pour les gammes de produits principales, font face à des contraintes de talents et à une obsolescence rapide à mesure que les normes évoluent. Certaines multinationales opèrent désormais des modèles hybrides dans lesquels les tests de logiciels critiques ou de matériaux propriétaires restent sur site, tandis que des laboratoires tiers gèrent la coexistence sans fil, les biais des algorithmes d'IA et les certifications de niche internationales. Cette dynamique encourage les prestataires de TIC à se co-localiser près des principaux pôles de fabrication, en offrant une infrastructure partagée et des portails de données en temps réel qui s'articulent avec les cycles de conception des équipementiers.
Analyse Géographique
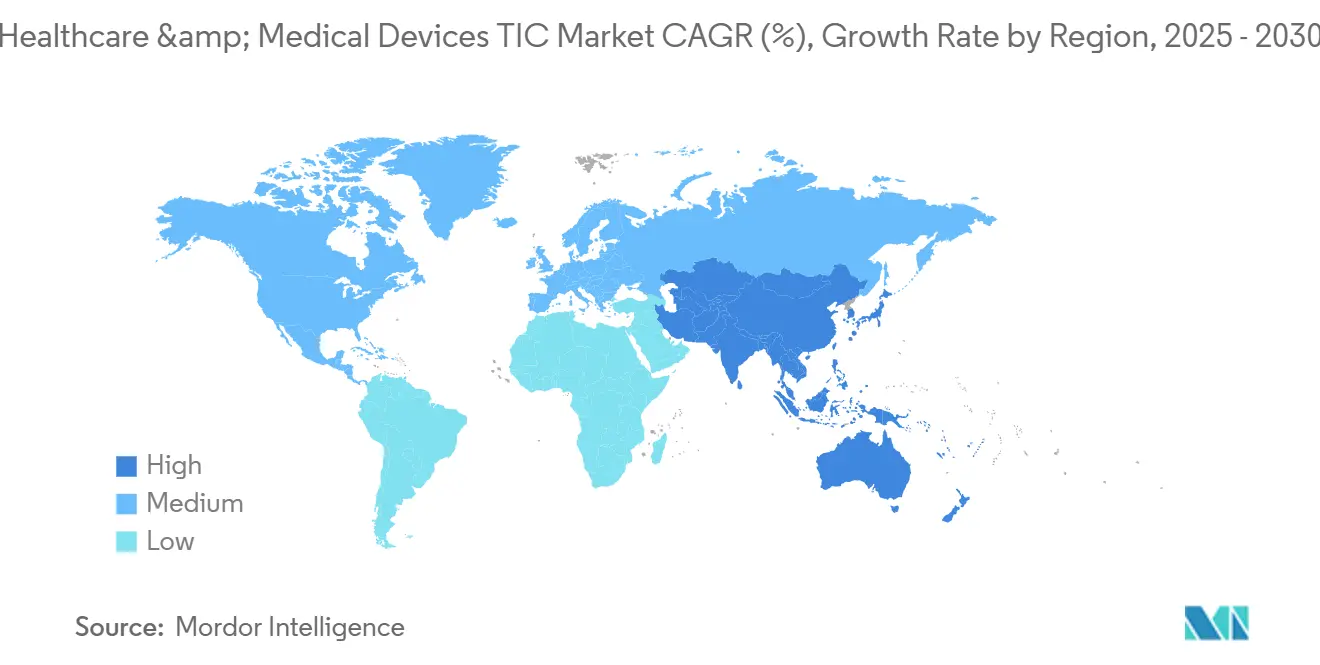
L'Asie-Pacifique a capturé 44,7 % des revenus mondiaux en 2024 et devrait enregistrer un CAGR de 4,5 % jusqu'en 2030, faisant de la région le moteur de croissance du marché des tests, de l'inspection et de la certification des dispositifs médicaux. Les réformes de la National Medical Products Administration (NMPA) de Chine synchronisent les règles nationales avec les normes ISO et IEC tout en imposant des rapports de test locaux, cimentant la demande pour des laboratoires accrédités à l'échelle internationale.[4]Administration nationale des produits médicaux, "Mises à jour réglementaires," NMPA.GOV.CN Le Japon et la Corée du Sud ajoutent des besoins de validation en cybersécurité et en IA haut de gamme, tandis que l'Asie du Sud-Est gagne en traction pour des analyses de routine rentables dans le cadre de l'harmonisation de l'ASEAN.
L'Amérique du Nord détenait 28 % de la part de marché en 2024 et devrait se développer modérément à un CAGR de 3,2 %. Les États-Unis sont en tête avec des projets à haute marge dans les évaluations des risques des dispositifs connectés, alors que la FDA examine les divulgations des nomenclatures logicielles. La participation du Canada au MDSAP maintient des synergies d'audit transfrontalières, tandis que les laboratoires à moindre coût du Mexique attirent des segments de tests de base pour les chaînes d'approvisionnement régionales.
L'Europe représentait 22 % des revenus de 2024, le MDR et l'IVDR ayant transformé les auto-certifications héritées en engagements formels de TIC. L'Allemagne et le Royaume-Uni dominent le volume, les doubles certifications UE-Royaume-Uni ouvrant des opportunités supplémentaires après le Brexit. Les réglementations sur l'économie circulaire catalysent des niches de tests de remise en état et de cycle de vie, et le RGPD entraîne un contrôle accru de l'intégrité des données des patients.
Paysage Concurrentiel
Le leadership mondial reste dispersé, plaçant le secteur des tests, de l'inspection et de la certification des dispositifs médicaux dans un niveau modérément concentré. SGS, Intertek, TÜV SÜD et Bureau Veritas s'appuient sur plus de 1 000 reconnaissances gouvernementales et de vastes réseaux de laboratoires pour se différencier des spécialistes régionaux. La récente autorisation de SGS Shanghai sans aucune observation sur le formulaire FDA 483 illustre la profondeur des accréditations qui justifient des primes de prix.
La transformation numérique sous-tend les avantages concurrentiels. L'automatisation FlexLab X de Siemens Healthineers et les suites robotiques de Merck illustrent le pivot vers un débit piloté par l'IA, atténuant les pénuries d'auditeurs et élevant la fidélité des données. La cybersécurité, les audits de biais algorithmiques et la validation des dispositifs remis en état constituent des espaces blancs lucratifs où des experts plus petits peuvent évoluer rapidement ou devenir des cibles d'acquisition, comme le montre l'acquisition par Mérieux NutriSciences de l'activité de tests alimentaires de Bureau Veritas pour 405 millions USD afin de doubler sa présence en Asie-Pacifique.
La dynamique des fusions et acquisitions devrait se poursuivre, soutenue par l'intérêt du capital-investissement et des opérations intersectorielles synergiques qui combinent des portefeuilles environnementaux, pharmaceutiques et de technologie médicale pour la commodité des utilisateurs finaux. Les prix restent résilients compte tenu de la rareté des accréditations et des coûts de changement élevés, mais l'inflation salariale et les investissements dans les technologies réglementaires compriment les marges pour les entreprises manquant d'échelle ou de feuilles de route d'automatisation.
Leaders du Secteur des TIC pour la Santé et les Dispositifs Médicaux
SGS SA
Bureau Veritas SA
Intertek Group plc
TÜV SÜD AG
TÜV Rheinland AG
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements Récents du Secteur
- Mars 2025 : Merck a lancé des solutions d'automatisation de laboratoire et de robotique pour le contrôle qualité pharmaceutique, en partenariat avec des sociétés d'ingénierie pour fournir des systèmes de tests microbiologiques intégrés.
- Février 2025 : GN Store Nord a déclaré des dépenses de R&D de 1,9 milliard DKK, mettant l'accent sur des cadres centralisés de qualité et de sécurité des produits pour les dispositifs auditifs assistés par l'IA (0,29 milliard USD).
- Janvier 2025 : Eurofins Scientific a acquis SF Analytical Laboratories, élargissant sa portée en matière de tests environnementaux et alimentaires aux États-Unis.
- Octobre 2024 : Mérieux NutriSciences a accepté d'acquérir la division de tests alimentaires de Bureau Veritas pour 360 millions EUR (405 millions USD).
Portée du Rapport Mondial sur le Marché des TIC pour la Santé et les Dispositifs Médicaux
| Services de Test |
| Services d'Inspection |
| Services de Certification |
| Interne |
| Externalisé |
| Amérique du Nord | États-Unis | |
| Canada | ||
| Mexique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Russie | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Corée du Sud | ||
| Asie du Sud-Est | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | Moyen-Orient | Arabie Saoudite |
| Émirats Arabes Unis | ||
| Turquie | ||
| Reste du Moyen-Orient | ||
| Afrique | Afrique du Sud | |
| Nigéria | ||
| Reste de l'Afrique | ||
| Par Type de Service | Services de Test | ||
| Services d'Inspection | |||
| Services de Certification | |||
| Par Type d'Approvisionnement | Interne | ||
| Externalisé | |||
| Par Géographie | Amérique du Nord | États-Unis | |
| Canada | |||
| Mexique | |||
| Amérique du Sud | Brésil | ||
| Argentine | |||
| Reste de l'Amérique du Sud | |||
| Europe | Allemagne | ||
| Royaume-Uni | |||
| France | |||
| Italie | |||
| Espagne | |||
| Russie | |||
| Reste de l'Europe | |||
| Asie-Pacifique | Chine | ||
| Japon | |||
| Inde | |||
| Corée du Sud | |||
| Asie du Sud-Est | |||
| Reste de l'Asie-Pacifique | |||
| Moyen-Orient et Afrique | Moyen-Orient | Arabie Saoudite | |
| Émirats Arabes Unis | |||
| Turquie | |||
| Reste du Moyen-Orient | |||
| Afrique | Afrique du Sud | ||
| Nigéria | |||
| Reste de l'Afrique | |||
Questions Clés Répondues dans le Rapport
Quelle est la taille actuelle du marché mondial des tests, de l'inspection et de la certification pour la santé et les dispositifs médicaux ?
Le marché s'élève à 7,35 milliards USD en 2025 et devrait atteindre 8,87 milliards USD d'ici 2030.
Quelle région contribue le plus aux revenus des services de conformité des dispositifs médicaux ?
L'Asie-Pacifique est en tête avec 44,7 % des revenus mondiaux, portée par l'échelle manufacturière et la maturité réglementaire.
Pourquoi les services de certification croissent-ils plus vite que les services de test ?
Les cadres harmonisés tels que le MDSAP et l'IVDR permettent à un seul certificat d'ouvrir plusieurs marchés, rendant la certification par des tiers plus précieuse.
Quel est le principal défi limitant la croissance de la capacité à court terme pour les prestataires de TIC ?
Une pénurie de 25 à 30 % d'auditeurs biomédicaux qualifiés contraint l'expansion des services malgré une demande croissante.
Comment l'externalisation se compare-t-elle aux tests internes ?
L'externalisation contrôle 69,3 % des dépenses totales car les laboratoires spécialisés réduisent les dépenses en capital et accélèrent les approbations dans plusieurs pays.
Quelles niches émergentes offrent le plus grand potentiel de croissance pour les entreprises de TIC ?
Les domaines à haute marge comprennent la validation de la cybersécurité pour les dispositifs connectés, les audits de biais des algorithmes d'IA et les tests de remise en état dans le cadre de l'économie circulaire.
Dernière mise à jour de la page le:



