Tamaño y Participación del Mercado de Kits de Pruebas Diagnósticas para Parto Prematuro
Análisis del Mercado de Kits de Pruebas Diagnósticas para Parto Prematuro por Mordor Intelligence
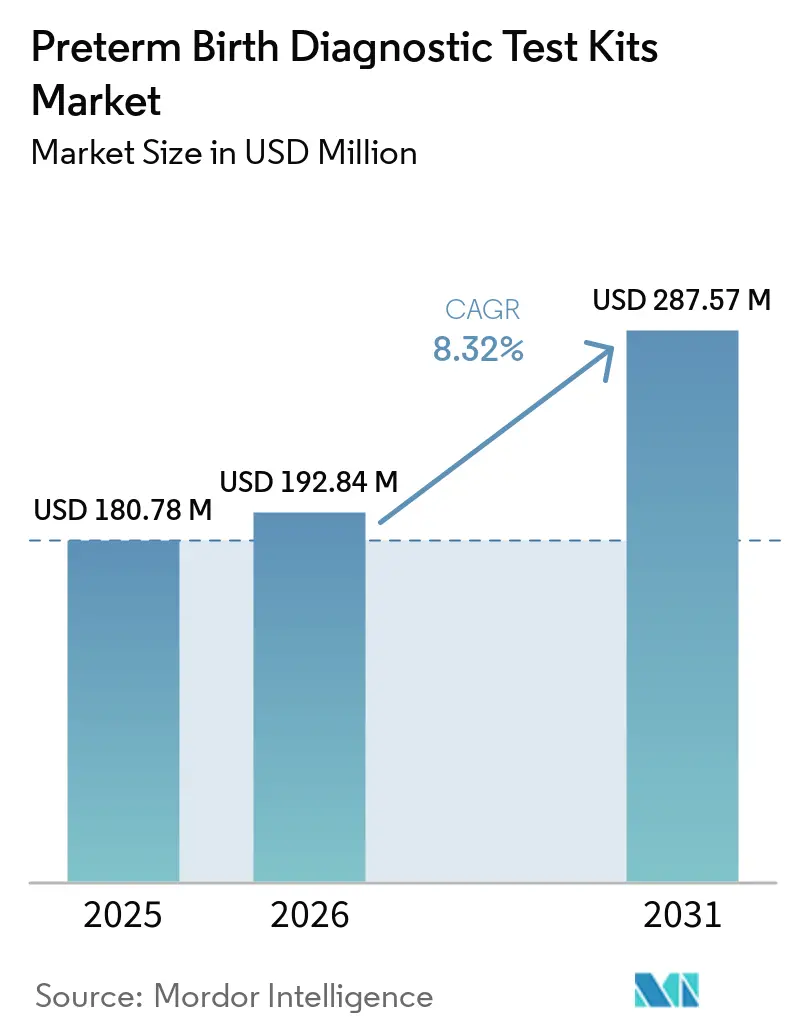
El tamaño del Mercado de Kits de Pruebas Diagnósticas para Parto Prematuro está proyectado en USD 180,78 millones en 2025, USD 192,84 millones en 2026, y alcanzará USD 287,57 millones en 2031, creciendo a una CAGR del 8,32% de 2026 a 2031.
El crecimiento refleja un cambio del triaje sintomático hacia una estratificación de riesgo más temprana, a medida que los equipos clínicos combinan pruebas de biomarcadores con ecografía de longitud cervical para reducir ingresos e intervenciones evitables. La discontinuación de los casetes cuantitativos de fibronectina fetal perturbó las rutinas hospitalarias establecidas y redirigió las adquisiciones hacia biomarcadores alternativos y plataformas binarias de descarte. Las pruebas basadas en hisopo de PAMG-1 e IGFBP-1, junto con los diagnósticos de rotura de membranas, continúan siendo el pilar de las decisiones rápidas en las unidades de parto donde los minutos son cruciales para el alta o el traslado. La evidencia de 2026 reforzó el valor del cribado proteómico basado en sangre, con un gran estudio aleatorizado que demostró mejores resultados cuando se aplicó una estrategia de prevención basada en PreTRM en embarazos de bajo riesgo. La dinámica regional favorece la escala y el compromiso de los pagadores, con América del Norte manteniendo el liderazgo en participación mientras Asia-Pacífico se expande más rápidamente a través de la construcción de laboratorios y proyectos piloto de reembolso.
Conclusiones Clave del Informe
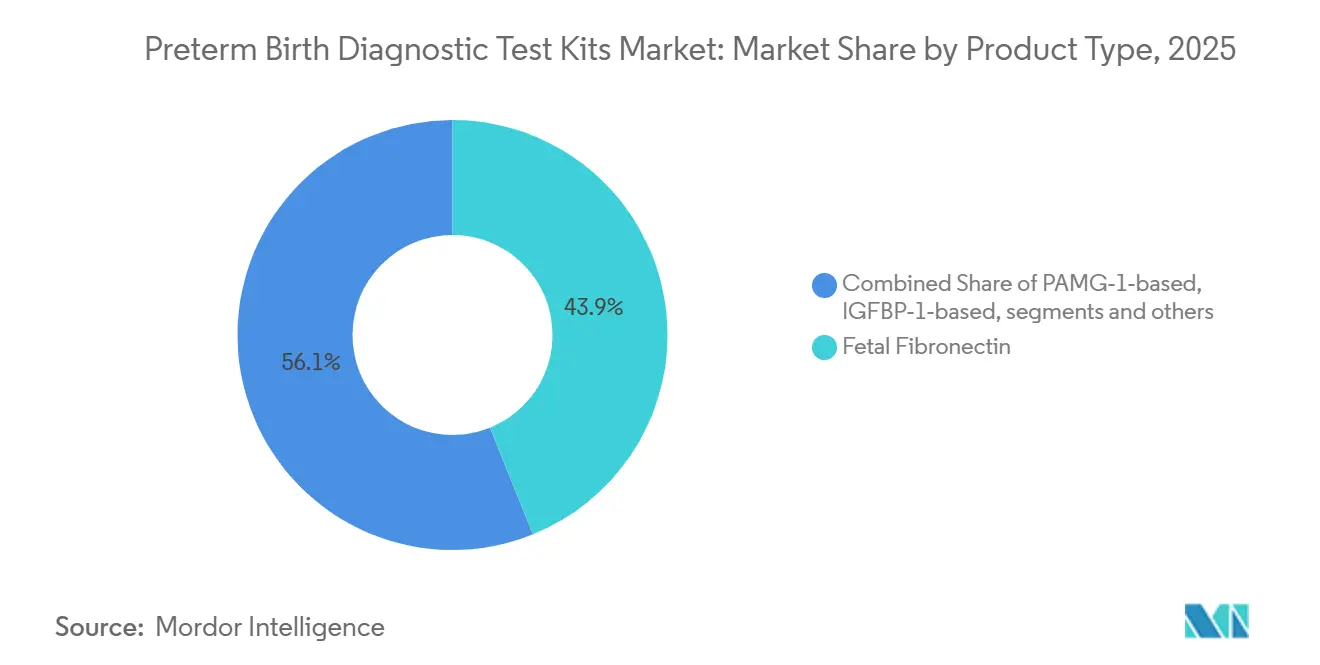
- Por tipo de producto, la fibronectina fetal lideró con una participación de ingresos del 43,89% en 2025, mientras que se proyecta que las plataformas PAMG-1 registren el crecimiento más rápido con una CAGR del 9,67% hasta 2031.
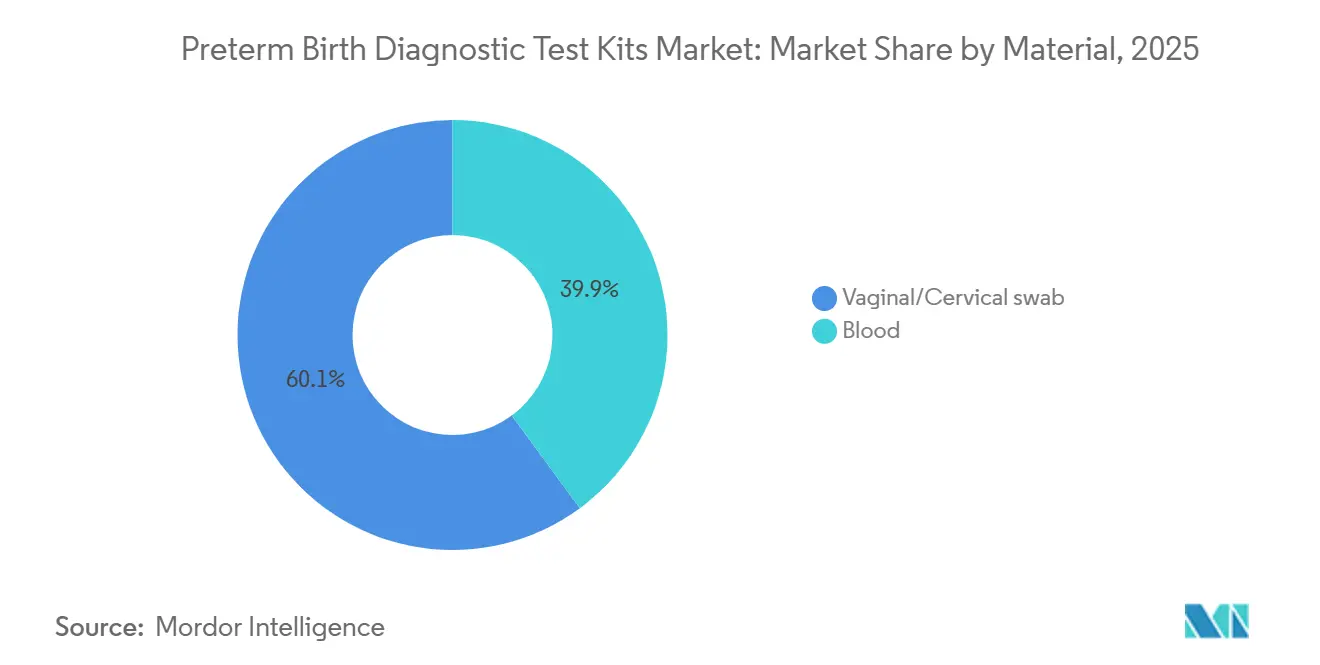
- Por material, los hisopos vaginales-cervicales representaron el 60,10% de los ingresos de 2025 y los ensayos proteómicos basados en sangre avanzan a una CAGR del 9,01% hasta 2031.
- Por usuario final, los hospitales y centros de maternidad concentraron el 58,56% de la demanda de 2025 y los laboratorios de diagnóstico registraron el mayor crecimiento proyectado con una CAGR del 10,34%.
- Por región, América del Norte contribuyó con el 43,64% de los ingresos de 2025 y Asia-Pacífico está proyectada para crecer a una CAGR del 9,45% hasta 2031.
Nota: Las cifras del tamaño del mercado y los pronósticos de este informe se generan utilizando el marco de estimación patentado de Mordor Intelligence, actualizado con los datos y conocimientos más recientes disponibles a partir de enero de 2026.
Tendencias e Información del Mercado Global de Kits de Pruebas Diagnósticas para Parto Prematuro
Análisis del Impacto de los Impulsores
| Impulsor | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Aumento de la incidencia global y la carga de los partos prematuros | +2.3% | Global, con presión aguda en África Subsahariana y Asia del Sur | Largo plazo (≥ 4 años) |
| Integración del triaje basado en biomarcadores en las vías clínicas (fFN, PAMG-1, IGFBP-1) | +2.8% | América del Norte y la Unión Europea como núcleo, con expansión a centros urbanos de Asia-Pacífico | Mediano plazo (2-4 años) |
| Kits de flujo lateral rápidos en el punto de atención que permiten decisiones rápidas de descarte en el triaje de maternidad | +1.6% | América del Norte, Europa Occidental, Australia | Corto plazo (≤ 2 años) |
| Apoyo de protocolos hospitalarios y reembolso para pruebas dirigidas en casos de alto riesgo/sintomáticos | +1.1% | Nacional, con ganancias tempranas en planes comerciales y Medicaid de EE. UU., sistemas públicos europeos | Mediano plazo (2-4 años) |
| Expansión de pruebas de riesgo proteómico basadas en sangre que informan vías de atención más tempranas | +0.9% | Enfoque en EE. UU., programas piloto en mercados europeos seleccionados | Largo plazo (≥ 4 años) |
| Herramientas de decisión digital que combinan biomarcadores cuantitativos con longitud cervical | +0.5% | Núcleo en Asia-Pacífico (China, India, Corea del Sur), emergente en América Latina | Largo plazo (≥ 4 años) |
| Fuente: Mordor Intelligence | |||
Aumento de la Incidencia Global y la Carga de los Partos Prematuros
El parto prematuro sigue siendo una de las principales causas de morbilidad y mortalidad neonatal en todo el mundo, lo que sostiene la demanda clínica de una evaluación de riesgo más temprana y precisa. Los hospitales buscan estandarizar el triaje para limitar los traslados innecesarios y apoyar el uso oportuno de corticosteroides solo cuando el riesgo es creíble y cercano al término. La carga persistente en entornos de bajos recursos expone una brecha entre la necesidad y el acceso, lo que sostiene el uso de pruebas más simples y retrasa la adopción de ensayos avanzados de biomarcadores. Los sistemas de salud evalúan el valor operativo de las pruebas que pueden descartar rápidamente el parto inminente, previniendo hospitalizaciones evitables y reduciendo la presión sobre las unidades terciarias. Estas dinámicas mantienen al mercado de kits de pruebas diagnósticas para parto prematuro enfocado en la velocidad y claridad del resultado para fortalecer las decisiones de primera línea.
Integración del Triaje Basado en Biomarcadores en las Vías Clínicas (fFN, PAMG-1, IGFBP-1)
Muchas instituciones en América del Norte y Europa han integrado el triaje basado en biomarcadores en protocolos estandarizados para pacientes con síntomas entre las semanas 24 y 34, reduciendo los ingresos injustificados cuando se obtiene un resultado negativo claro. La discontinuación de los casetes cuantitativos de fibronectina fetal impulsó la orientación nacional en 2024 para la transición a plataformas alternativas, lo que reformuló las adquisiciones y fomentó una evaluación más amplia de las opciones de IGFBP-1 y PAMG-1[1]NHS England, "Discontinuación de las pruebas de fibronectina fetal de Hologic," NHS England, england.nhs.uk. El papel de los diagnósticos de rotura de membranas persiste como parte de la vía de atención, ya que el estado de las membranas influye directamente en el riesgo de parto a corto plazo y en las decisiones de vigilancia clínica. El triaje basado en protocolos limita la variación entre los clínicos y canaliza los recursos hacia los casos con riesgo medible en lugar de la observación preventiva. La orientación profesional y los comités institucionales continúan dando forma a la adopción, anclando el mercado de kits de pruebas diagnósticas para parto prematuro a pruebas que ofrecen claridad binaria o casi binaria en minutos.
Kits de Flujo Lateral Rápidos en el Punto de Atención que Permiten Decisiones Rápidas de Descarte en el Triaje de Maternidad
Los inmunoensayos en el punto de atención proporcionan resultados durante la misma consulta, lo que permite a los equipos dar el alta con confianza tras una prueba negativa o escalar la atención cuando un resultado positivo señala un riesgo a corto plazo. El tiempo hasta el resultado impulsa el valor operativo, ya que las unidades de urgencias a menudo deben decidir sobre el traslado o el momento de administrar esteroides en ventanas de tiempo cortas. Los formatos estables en almacén y los flujos de trabajo sencillos hacen que los kits de flujo lateral sean una herramienta práctica para las concurridas unidades de parto y para los centros más pequeños que buscan una práctica consistente. Donde el diagnóstico de rotura de membranas es relevante, las opciones de flujo lateral apoyan la confirmación rápida del estado de las membranas y reducen la dependencia de métodos heredados menos precisos. Las políticas de los pagadores y los formularios locales aún influyen en qué kits se utilizan de forma rutinaria, razón por la cual los protocolos y los estándares de compra siguen siendo fundamentales para escalar el acceso. El mercado de kits de pruebas diagnósticas para parto prematuro se beneficia cuando los menús de pruebas se integran en flujos de trabajo en el punto de atención que resuelven las decisiones de triaje en minutos.
Apoyo de Protocolos Hospitalarios y Reembolso para Pruebas Dirigidas en Casos de Alto Riesgo/Sintomáticos
La cobertura y los protocolos internos determinan conjuntamente la consistencia con que se utilizan las pruebas en la atención obstétrica de primera línea. Cuando los comités hospitalarios codifican las escalas de pruebas para mujeres sintomáticas, la variación clínica disminuye y los resultados se vuelven más fáciles de gestionar y medir. En el Reino Unido, la orientación nacional tras la discontinuación del fFN ilustró cómo los sistemas públicos pueden orientar la selección de productos y estabilizar la práctica en todos los centros. En los Estados Unidos, los modelos de laboratorio centralizado para pruebas proteómicas basadas en sangre operan bajo la supervisión de CLIA y CAP, lo que permite una calidad consistente a escala a medida que los pagadores revisan los datos de resultados para una cobertura amplia. Las empresas han informado sobre el compromiso de los pagadores y las discusiones activas sobre el reembolso de estrategias de prevención informadas por resultados de riesgo proteómico, lo que refleja el impulso hacia acuerdos basados en el valor. Estos patrones refuerzan el enfoque del mercado de kits de pruebas diagnósticas para parto prematuro en pruebas vinculadas a acciones clínicas claras y compensaciones de costos medibles.
Análisis del Impacto de las Restricciones
| Restricción | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Respaldos de directrices mixtos/condicionales para algunos biomarcadores y usos | -0.7% | Global, variabilidad más alta en Oriente Medio y América Latina | Mediano plazo (2-4 años) |
| Valor predictivo positivo modesto/falsos positivos que requieren evaluación confirmatoria | -0.4% | Global, carga operativa concentrada en entornos de bajos recursos | Corto plazo (≤ 2 años) |
| Restricciones operativas de muestreo (tiempo, co-interferencia) que limitan el despliegue universal | -0.3% | África Subsahariana, Asia del Sur rural, Australia remota | Mediano plazo (2-4 años) |
| El Reglamento de Diagnóstico In Vitro de la Unión Europea eleva la evidencia clínica, el costo y el tiempo de comercialización para los diagnósticos in vitro | -0.8% | Unión Europea de 27 estados, con expansión a países que reconocen el marcado CE | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Respaldos de Directrices Mixtos/Condicionales para Algunos Biomarcadores y Usos
La variabilidad de las directrices entre regiones ralentiza la adopción estandarizada y mantiene un mosaico de prácticas de pruebas dentro y entre países. Los documentos profesionales a menudo hacen referencia a clases de biomarcadores en lugar de marcas específicas, lo que deja a los equipos de adquisición decidir en función del precio, la disponibilidad y la familiaridad local. El respaldo inconsistente para casos de uso como el cribado asintomático contribuye a una adopción desigual fuera de los centros terciarios. Los clínicos también se enfrentan a reglas de pago divergentes sobre qué pruebas se reembolsan en escenarios específicos, lo que añade fricción a los pedidos rutinarios. Estos factores moderan el ritmo al que el mercado de kits de pruebas diagnósticas para parto prematuro puede pasar del uso piloto a un despliegue estable basado en protocolos.
El Reglamento de Diagnóstico In Vitro de la Unión Europea Eleva la Evidencia Clínica, el Costo y el Tiempo de Comercialización para los Diagnósticos In Vitro
Los requisitos regulatorios europeos han ampliado las obligaciones de evidencia y poscomercialización, lo que aumenta el costo y la complejidad de llevar los diagnósticos obstétricos al mercado. La capacidad de los organismos notificados y las exigencias de documentación amplían los plazos para las actualizaciones y las nuevas indicaciones, lo que puede retrasar las transiciones del uso piloto a la disponibilidad amplia. Las empresas con sistemas de calidad maduros y presentaciones anteriores tienden a navegar las revisiones de manera más predecible, mientras que los nuevos participantes enfrentan mayores necesidades de recursos. El resultado es un listón más alto para los datos de rendimiento y la vigilancia continua que puede consolidar la participación con los actores establecidos con el tiempo. Este entorno alienta a los proveedores a priorizar las indicaciones de las pruebas que se alinean estrechamente con la utilidad clínica y el valor para los pagadores, de modo que las inversiones en cumplimiento se traduzcan en tracción de adopción.
Análisis de Segmentos
Por Tipo de Producto: La Proteómica Sanguínea Reduce la Brecha del Triaje
La fibronectina fetal representó el 43,89% de la participación del tamaño del mercado de kits de pruebas diagnósticas para parto prematuro en 2025, lo que refleja el arraigo heredado antes de que un cambio en el suministro modificara el comportamiento de los pedidos. La discontinuación de los casetes cuantitativos de fFN en 2024 reemplazó el estándar cuantitativo por biomarcadores cualitativos y alternativos dentro de muchas vías hospitalarias. Se proyecta que las plataformas PAMG-1 crezcan a una CAGR del 9,67% hasta 2031 a medida que los hospitales adopten formatos binarios de descarte que agilizan las decisiones de triaje para mujeres sintomáticas. Los diagnósticos de rotura de membranas siguen siendo un pilar complementario en la vía de atención porque confirmar el estado de las membranas influye sustancialmente en la gestión del riesgo a corto plazo. El mercado de kits de pruebas diagnósticas para parto prematuro también está redefiniendo el momento oportuno, ya que las pruebas de sangre proteómicas, lideradas por PreTRM, se centran en el riesgo entre las semanas 18 y 20 con una estrategia de prevención basada en progesterona, aspirina y una navegación de atención intensificada[2]Sera Prognostics, "La Ciencia Detrás de la Prueba PreTRM," PreTRM, pretrm.com. La evidencia aleatorizada reportada en 2026 mostró una reducción en los partos muy prematuros y menos complicaciones neonatales cuando el cribado con PreTRM se combinó con intervenciones dirigidas. Estos cambios desplazan el centro de gravedad desde la gestión de crisis entre las semanas 24 y 34 hacia una estratificación de riesgo más temprana que puede evitar episodios de alto costo. Los hospitales aún valoran el valor predictivo negativo accionable para evitar traslados, mientras que los laboratorios enfatizan los flujos de trabajo centralizados para ensayos complejos. En conjunto, estas dinámicas de productos sostienen un mercado de dos velocidades en el que los kits de hisopo rápidos apoyan el triaje agudo y la proteómica sanguínea se expande hacia la atención preventiva.
La combinación de productos refleja claras compensaciones operativas que dan forma a las preferencias de los compradores. Los hisopos en el punto de atención que devuelven resultados en minutos se adaptan a las unidades de urgencias y observación que necesitan claridad inmediata para las decisiones de descarte. Las opciones de PAMG-1 e IGFBP-1 compiten en precio, disponibilidad y familiaridad con las directrices locales a medida que los equipos de adquisición buscan un suministro confiable tras las interrupciones del fFN. Los ensayos proteómicos basados en sangre requieren procesamiento centralizado, pero abren una nueva oportunidad de prevención dirigida a los muchos partos prematuros espontáneos que carecen de factores de riesgo tradicionales. El mercado de kits de pruebas diagnósticas para parto prematuro, por lo tanto, alinea los productos con el momento clínico, con el triaje sintomático anclado por kits de flujo lateral y el riesgo asintomático abordado por pruebas proteómicas que influyen en los planes de atención semanas antes de que aparezcan los síntomas. Este posicionamiento complementario ayuda a los proveedores a defenderse de la competencia basada únicamente en el precio al vincular las pruebas con los resultados y el impacto presupuestario.
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles con la compra del informe
Por Material: Los Hisopos Vaginales Anclan el Volumen, los Ensayos Sanguíneos Capturan el Valor
Las pruebas de hisopo vaginal-cervical representaron el 60,10% de la participación del mercado de kits de pruebas diagnósticas para parto prematuro en 2025, lo que refleja los flujos de trabajo hospitalarios establecidos y la velocidad de resultado que ofrecen estos formatos. La recolección con hisopo se alinea con los protocolos que priorizan la comodidad del paciente y el apoyo inmediato a la toma de decisiones para los casos sintomáticos. Las realidades operativas, como el momento de la toma de muestra y la posible interferencia, aún requieren disciplina, lo que subraya la importancia de las vías de triaje estandarizadas. Se proyecta que las plataformas basadas en sangre se expandan a una CAGR del 9,01% hasta 2031, ya que los laboratorios centralizados utilizan el procesamiento por lotes y los controles de calidad para escalar el acceso a las ventanas de cribado preventivo. Sera Prognostics ha destacado la logística de sangre total a temperatura ambiente y las operaciones centralizadas bajo CLIA como habilitadores clave de las pruebas proteómicas consistentes a escala nacional. Investigaciones independientes también han reportado prometedores paneles de proteínas plasmáticas del segundo trimestre para la predicción del parto prematuro espontáneo, lo que señala un mayor potencial para la innovación en pruebas sanguíneas. Estas diferencias de material se corresponden con momentos de atención distintos y crean un camino equilibrado para el crecimiento en entornos agudos y preventivos.
La elección del material también afecta el rendimiento y el flujo de datos hacia los equipos de atención. Los hisopos de flujo lateral ofrecen resultados en el punto de atención y apoyan las decisiones de alta en tiempo real en las salas de urgencias y las unidades de triaje de parto. La proteómica sanguínea favorece las visitas prenatales programadas y la interpretación centralizada que devuelve el riesgo individualizado en días en lugar de minutos. A medida que los sistemas de salud combinan biomarcadores con ecografía de longitud cervical, ambos materiales contribuyen a algoritmos más claros de inclusión y exclusión que optimizan el uso de recursos. El mercado de kits de pruebas diagnósticas para parto prematuro, por lo tanto, acomoda un papel duradero para los hisopos mientras expande el valor de las pruebas sanguíneas para una planificación de intervención más temprana.
Por Usuario Final: Los Laboratorios Superan a los Hospitales en Flujos de Trabajo de Alta Complejidad
Los hospitales y centros de maternidad representaron el 58,56% de la participación del mercado de kits de pruebas diagnósticas para parto prematuro en 2025, impulsados por el uso consistente de hisopos en el punto de atención en entornos de triaje donde la velocidad es fundamental. Los resultados negativos apoyan el alta el mismo día y limitan las estancias de observación que no son clínicamente necesarias. Los laboratorios de diagnóstico registraron una CAGR del 10,34% hasta 2031 al absorber los paneles de envío externo y la proteómica sanguínea que requieren flujos de trabajo centralizados e instrumentos especializados. Sera Prognostics opera un único laboratorio certificado por CLIA y acreditado por CAP para procesar todas las muestras de PreTRM a nivel nacional, lo que permite una supervisión estricta del rendimiento a escala. Esta división del trabajo se alinea con la forma en que se presta la atención, con los hospitales priorizando la inmediatez y los laboratorios avanzando en la prevención y la gestión del riesgo.
Se está generando impulso para modelos integrados que unifican las decisiones en el punto de atención con la analítica centralizada. Los hospitales mantienen un papel sólido en el triaje sintomático, mientras que los laboratorios amplían la huella de cribado previo con evaluaciones proteómicas que pueden desencadenar intervenciones dirigidas. Los pagadores que evalúan los datos de resultados pueden fomentar modelos que combinen pruebas de triaje inmediatas con estrategias preventivas que reduzcan los días en la Unidad de Cuidados Intensivos Neonatales y los costos. El mercado de kits de pruebas diagnósticas para parto prematuro, por lo tanto, refleja las fortalezas de los usuarios finales tanto en la inmediatez como en los beneficios de la atención longitudinal.
Análisis Geográfico
América del Norte concentró el 43,64% de los ingresos de 2025 y ancla el mercado de kits de pruebas diagnósticas para parto prematuro con protocolos que incorporan el uso de biomarcadores en las unidades de trabajo de parto y parto. La discontinuación en 2024 del fFN cuantitativo impulsó transiciones aceleradas hacia biomarcadores alternativos y reforzó el peso de la orientación nacional en la configuración de la práctica. Canadá y México se quedan atrás de la adopción en los Estados Unidos, ya que las reglas de adquisición y cobertura varían entre provincias y combinaciones de pagadores. El crecimiento en los Estados Unidos ahora incluye proyectos piloto de cribado asintomático bajo planes comerciales y Medicaid, lo que impulsa la adopción más allá del triaje de crisis hacia la prevención. El mercado de kits de pruebas diagnósticas para parto prematuro en América del Norte continúa equilibrando el uso rápido de hisopos con los flujos de trabajo proteómicos emergentes que pueden demostrar resultados medibles.
Se proyecta que Asia-Pacífico crezca a una CAGR del 9,45% hasta 2031, a medida que los laboratorios escalan en China, India y Corea del Sur y los proyectos piloto públicos examinan la cobertura de ensayos más nuevos. La fabricación nacional y las licitaciones sensibles al precio influyen en la adopción de hisopos en las redes públicas, mientras que las cadenas de hospitales privados se concentran en PAMG-1 e IGFBP-1 en los centros urbanos. La disminución de la tasa de natalidad de Japón y una fuerza laboral obstétrica limitada moderan el crecimiento de la demanda, aunque la adopción dirigida persiste en los centros terciarios. En Australia, los grupos clínicos monitorearon las implicaciones de los cambios en el suministro de fFN en las prácticas de traslado rural y buscaron alternativas consistentes para preservar la confianza en el triaje. En todo el Sudeste Asiático, la cadena de frío limitada y las vías regulatorias fragmentadas ralentizan la adopción de nuevos biomarcadores, lo que mantiene al mercado de kits de pruebas diagnósticas para parto prematuro anclado a opciones asequibles y robustas.
Europa mantuvo su participación a medida que las instituciones navegaron por las cambiantes expectativas regulatorias y los plazos de cumplimiento para los diagnósticos in vitro. Alemania, Francia y el Reino Unido incorporan las pruebas de biomarcadores en las vías de atención de maternidad, aunque las evaluaciones presupuestarias pueden ralentizar la inclusión en los calendarios de reembolso nacionales. El cambio de 2024 en el Reino Unido hacia pruebas de triaje alternativas tras la discontinuación del fFN destacó la sensibilidad al costo del sector público y el papel central de la orientación nacional. El sur y el este de Europa exhiben una adopción desigual debido a la administración sanitaria regionalizada y un gasto per cápita más bajo, lo que sostiene la dependencia del juicio clínico y las pruebas más antiguas en algunos entornos. El mercado de kits de pruebas diagnósticas para parto prematuro en Europa recompensa cada vez más a los proveedores que pueden cumplir con las necesidades de documentación y poscomercialización sin interrumpir el suministro.
Oriente Medio y África muestran un crecimiento incipiente con hospitales privados en el Golfo que importan plataformas de biomarcadores occidentales y centros terciarios en Sudáfrica que utilizan los diagnósticos de forma selectiva. África Subsahariana soporta una alta carga de partos prematuros, pero enfrenta restricciones de infraestructura que limitan el uso de pruebas a los centros urbanos. Los esfuerzos programáticos continúan dirigiéndose a complicaciones relacionadas como la preeclampsia, donde nuevas pruebas rápidas en desarrollo buscan ampliar el acceso en entornos de menores recursos. Los sectores privados de América del Sur en Brasil y Argentina apoyan la adopción en clínicas urbanas, mientras que los sistemas públicos enfrentan presiones presupuestarias que moderan la escala. Estos factores regionales mantienen el crecimiento del mercado de kits de pruebas diagnósticas para parto prematuro vinculado a la sofisticación de las adquisiciones, la capacidad de los laboratorios y la disposición de los pagadores a vincular las pruebas con resultados medibles.
Panorama Competitivo
El mercado de kits de pruebas diagnósticas para parto prematuro sigue siendo fragmentado, y la discontinuación del fFN en 2024 redistribuyó las oportunidades de participación entre múltiples proveedores de biomarcadores. QIAGEN aprovecha un portafolio de rotura de membranas y trabajo de parto prematuro para realizar ventas cruzadas dentro de los programas de salud de la mujer, lo que permite la contratación agrupada en redes hospitalarias. Sera Prognostics avanza en un modelo de laboratorio centralizado enfocado en ventanas de cribado preventivo y resultados para los pagadores, reforzado por la evidencia aleatorizada de 2026 que apoya reducciones en los partos muy prematuros y las complicaciones neonatales. Estas estrategias se diferencian según el momento y el entorno de atención, lo que permite a los proveedores defender el valor a pesar de la competencia de precios en las categorías de hisopos de uso común.
Los movimientos estratégicos subrayan la generación de evidencia y la cobertura como diferenciadores clave. Sera reportó compromisos con pagadores y la expansión de su presencia comercial en campo para acelerar la adopción entre las redes de prestación integrada. En los trastornos hipertensivos del embarazo, Roche obtuvo la autorización 510(k) de la Administración de Alimentos y Medicamentos de los Estados Unidos para una prueba de cociente que informa la intensidad de la vigilancia y el momento del parto, lo que amplía indirectamente el conjunto de problemas abordables vinculados al parto prematuro. Dichos avances regulatorios y datos clínicos ayudan a las empresas a articular los beneficios de los resultados más allá de la precisión predictiva, lo que importa para los contratos basados en el valor y las adquisiciones basadas en el presupuesto.
Las presiones de costo y cumplimiento dan forma a los incentivos de consolidación sin eliminar el espacio para los especialistas. Las empresas con sistemas de calidad sólidos y experiencia regulatoria en múltiples regiones están mejor posicionadas para navegar por la evidencia en evolución y las obligaciones poscomercialización, lo que estabiliza el suministro y apoya la disciplina de precios. Los nuevos participantes que dependen de productos únicos compiten enfatizando la asequibilidad, la estabilidad en almacén o las ventajas discretas del flujo de trabajo que resuelven puntos de dolor en entornos con recursos limitados. El mercado de kits de pruebas diagnósticas para parto prematuro, por lo tanto, se centra en la velocidad, la agilidad regulatoria y el valor vinculado a los resultados que en conjunto impulsan una adopción duradera.
Líderes de la Industria de Kits de Pruebas Diagnósticas para Parto Prematuro
BIOSYNEX S.A.
Laborie Medical Technologies (Clinical Innovations)
Medix Biochemica (Actim)
QIAGEN N.V.
Hologic, Inc.
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Enero de 2026: Sera Prognostics publicó el estudio PRIME en PREGNANCY, demostrando que el cribado con la prueba sanguínea PreTRM combinado con progesterona vaginal diaria, aspirina en dosis bajas y gestión de enfermería redujo los partos antes de las 32 semanas en un 56% y los ingresos a la Unidad de Cuidados Intensivos Neonatales en un 20% en 5.018 mujeres inscritas en 19 centros de los Estados Unidos. El ensayo controlado aleatorizado cumplió ambos resultados primarios y ahorró un día de Unidad de Cuidados Intensivos Neonatales por cada 4,2 pacientes cribadas, proporcionando evidencia de que el cribado de biomarcadores previo combinado con intervenciones dirigidas mejora los resultados neonatales y reduce los costos de atención médica.
- Marzo de 2026: Sera Prognostics reportó los resultados financieros completos de 2025 y señaló que el comentario europeo en The Journal of Maternal-Fetal & Neonatal Medicine respaldó el enfoque de prueba y tratamiento de PreTRM como escalable para los sistemas de financiación pública. La empresa reveló discusiones activas con pagadores de planes comerciales y Medicaid y amplió su organización comercial en los Estados Unidos para apuntar a una adopción más amplia entre las redes de prestación integrada.
- Febrero de 2025: Roche Diagnostics recibió la autorización 510(k) de la Administración de Alimentos y Medicamentos de los Estados Unidos para la prueba de cociente sFlt-1/PlGF de Elecsys para estratificar a las mujeres embarazadas hospitalizadas con trastornos hipertensivos según el riesgo a corto plazo de desarrollar preeclampsia grave, lo que puede informar decisiones de vigilancia o parto más temprano que se intersectan con el riesgo de parto prematuro.
Alcance del Informe Global del Mercado de Kits de Pruebas Diagnósticas para Parto Prematuro
Según el alcance del informe, los kits de pruebas diagnósticas para parto prematuro son ensayos rápidos, ya sea en el punto de atención o basados en laboratorio, diseñados para evaluar el riesgo de parto prematuro en mujeres embarazadas. Estos kits funcionan detectando biomarcadores específicos en el fluido cervicovaginal o en sangre, lo que permite a los proveedores de atención médica determinar si es probable que una mujer sintomática dé a luz en los próximos 7 a 14 días.
El mercado de kits de pruebas diagnósticas para parto prematuro está segmentado por tipo de producto, material, usuario final y geografía. Por tipo de producto, el mercado está segmentado en fibronectina fetal, basado en PAMG-1, basado en IGFBP-1, pruebas de rotura de membranas de marcador dual y pruebas de riesgo proteómico basadas en sangre. Por material, el mercado está segmentado en hisopo vaginal/cervical y sangre. Por usuario final, el mercado está segmentado en hospitales y centros de maternidad, laboratorios de diagnóstico, centros de parto/clínicas ambulatorias de ginecología y obstetricia, y otros. Por geografía, el mercado está segmentado en América del Norte, Europa, Asia-Pacífico, Oriente Medio y África, y América del Sur. El informe de mercado también cubre los tamaños de mercado estimados y las tendencias para 17 países en las principales regiones a nivel mundial. El informe ofrece el valor (en USD) para los segmentos anteriores.
| Fibronectina Fetal |
| Basado en PAMG-1 |
| Basado en IGFBP-1 |
| Pruebas de Rotura de Membranas de Marcador Dual |
| Pruebas de Riesgo Proteómico Basadas en Sangre |
| Hisopo Vaginal/Cervical |
| Sangre |
| Hospitales y Centros de Maternidad |
| Laboratorios de Diagnóstico |
| Centros de Parto / Clínicas Ambulatorias de Ginecología y Obstetricia |
| Otros |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | Consejo de Cooperación del Golfo |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tipo de Producto | Fibronectina Fetal | |
| Basado en PAMG-1 | ||
| Basado en IGFBP-1 | ||
| Pruebas de Rotura de Membranas de Marcador Dual | ||
| Pruebas de Riesgo Proteómico Basadas en Sangre | ||
| Por Material | Hisopo Vaginal/Cervical | |
| Sangre | ||
| Por Usuario Final | Hospitales y Centros de Maternidad | |
| Laboratorios de Diagnóstico | ||
| Centros de Parto / Clínicas Ambulatorias de Ginecología y Obstetricia | ||
| Otros | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | Consejo de Cooperación del Golfo | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño actual y las perspectivas de crecimiento del mercado de kits de pruebas diagnósticas para parto prematuro?
El tamaño del mercado de kits de pruebas diagnósticas para parto prematuro es de USD 180,78 millones en 2025 y se proyecta que alcance USD 287,57 millones en 2031 a una CAGR del 8,32% durante 2026-2031.
¿Qué segmento está creciendo más rápido dentro del mercado de kits de pruebas diagnósticas para parto prematuro?
Las plataformas PAMG-1 y los ensayos proteómicos basados en sangre son los de más rápido crecimiento, con CAGR proyectadas del 9,67% y el 9,01% hasta 2031, respectivamente.
¿Cómo afectó la discontinuación del fFN al mercado de kits de pruebas diagnósticas para parto prematuro?
La discontinuación en 2024 de los casetes cuantitativos de fFN desplazó las adquisiciones hacia biomarcadores alternativos y reforzó el papel de los protocolos hospitalarios y la orientación nacional en la selección de productos.
¿Qué evidencia respalda el cribado asintomático más temprano en este ámbito?
En 2026, un gran estudio aleatorizado reportó menos partos muy prematuros y menos complicaciones neonatales cuando se utilizó una estrategia de prevención basada en PreTRM en embarazos de bajo riesgo.
¿Qué regiones lideran y cuáles se están acelerando en el mercado de kits de pruebas diagnósticas para parto prematuro?
América del Norte lidera por participación de ingresos en 2025, mientras que Asia-Pacífico está proyectada para expandirse más rápidamente hasta 2031 a medida que los laboratorios escalan y los proyectos piloto amplían el acceso.
¿Cómo influye la combinación de usuarios finales en los patrones de adopción de las pruebas para parto prematuro?
Los hospitales dominan el triaje urgente con hisopos rápidos, mientras que los laboratorios de diagnóstico están creciendo más rápido al escalar las pruebas proteómicas centralizadas y los paneles de envío externo que requieren flujos de trabajo especializados.
Última actualización de la página el: