Tamaño y Participación del Mercado de Etiquetado de Dispositivos Médicos
Análisis del Mercado de Etiquetado de Dispositivos Médicos por Mordor Intelligence
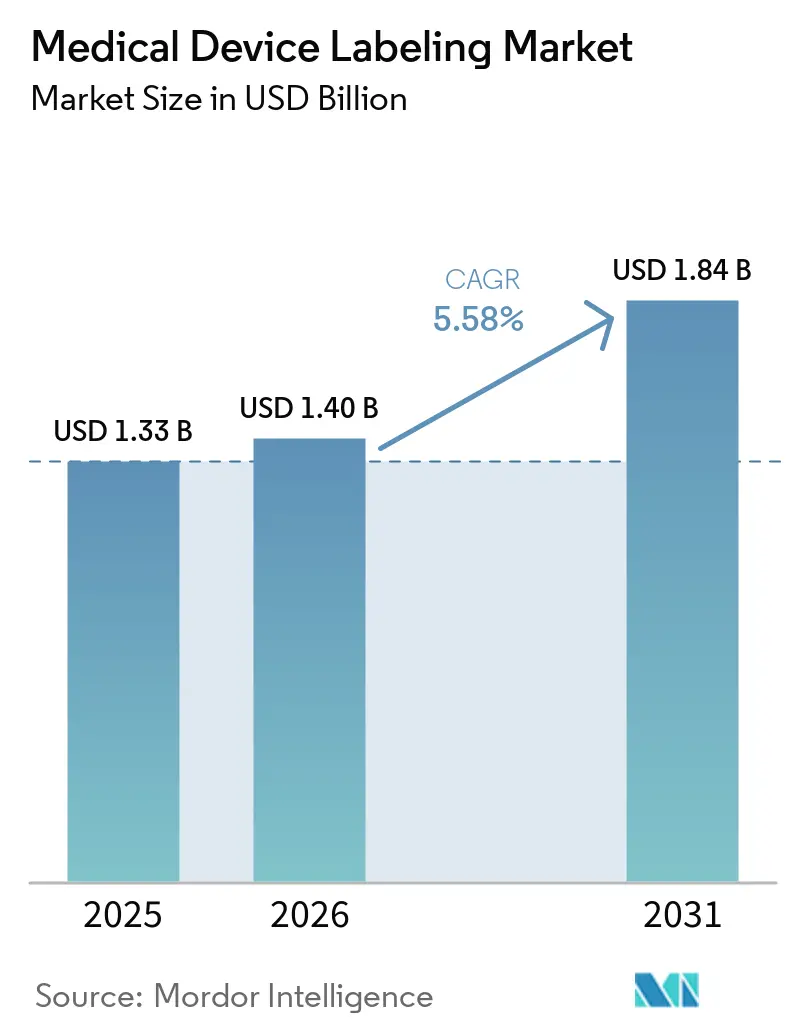
El tamaño del Mercado de Etiquetado de Dispositivos Médicos fue valorado en USD 1,33 mil millones en 2025 y se estima que crecerá desde USD 1,40 mil millones en 2026 hasta alcanzar USD 1,84 mil millones en 2031, a una CAGR del 5,58% durante el período de pronóstico (2026-2031).
El crecimiento de la demanda refleja la aceleración de los mandatos de identificación única de dispositivos (UDI), la adopción más amplia de instrucciones electrónicas de uso (eIFU) y el creciente cumplimiento multilingüe que convierte las etiquetas en portadoras críticas de datos en lugar de simples etiquetas pasivas [1]Administración de Alimentos y Medicamentos de los EE. UU., Conceptos Básicos de UDI - Sistema de Identificación Única de Dispositivos,
fda.gov. Los hospitales dependen de códigos QR o Data Matrix serializados para automatizar los flujos de trabajo de retiro del mercado, mientras que los fabricantes enfrentan un creciente número de unidades de mantenimiento de existencias a medida que cada variante de idioma necesita un diseño de etiqueta dedicado. La consolidación entre los convertidores de etiquetas está en marcha porque las empresas de dispositivos negocian descuentos por volumen y exigen impresión compatible con esterilización certificada por ISO 13485. Al mismo tiempo, el marcado directo de piezas en instrumentos reutilizables está reduciendo el uso de etiquetas externas para dispositivos ortopédicos y de endoscopia, lo que obliga a los convertidores a orientarse hacia la codificación RFID y la impresión en múltiples sustratos para defender su participación.
Conclusiones Clave del Informe
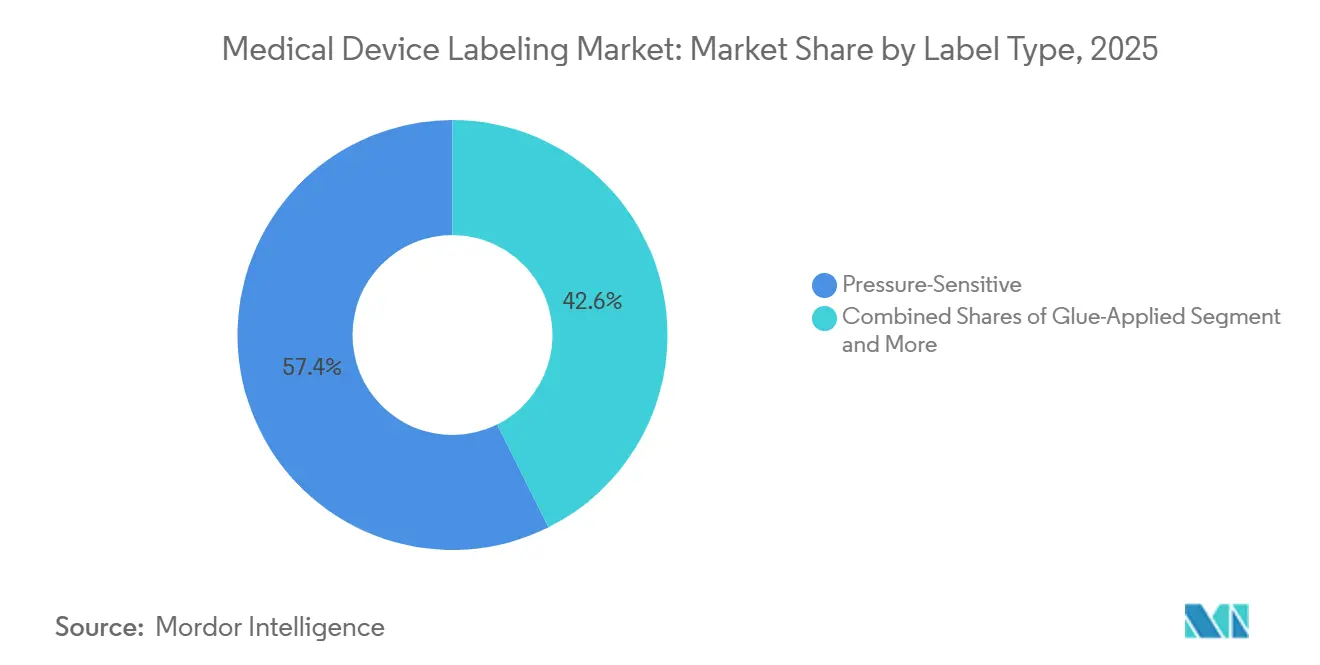
- Por tipo de etiqueta, las construcciones sensibles a la presión lideraron con el 57,37% de la participación del mercado de etiquetado de dispositivos médicos en 2025, mientras que las etiquetas de pegamento húmedo registraron la CAGR más rápida del 5,89% prevista hasta 2031.
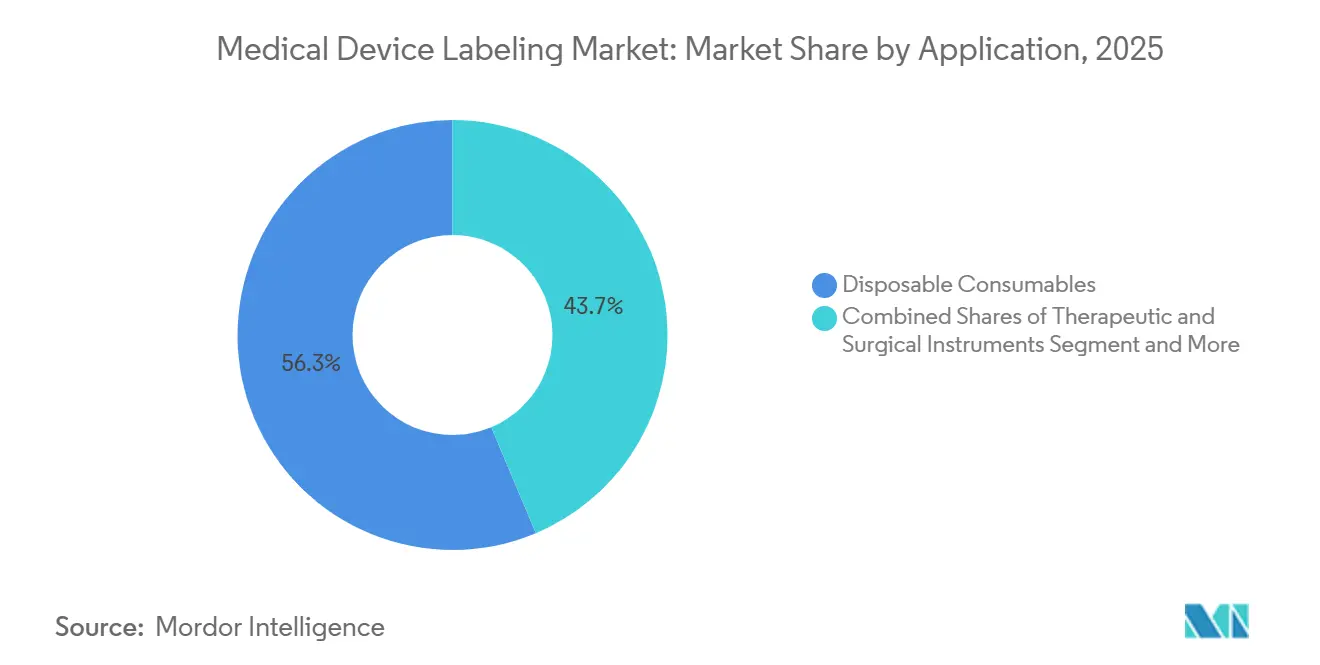
- Por aplicación, los consumibles desechables representaron el 56,34% de la participación del tamaño del mercado de etiquetado de dispositivos médicos en 2025, mientras que los instrumentos terapéuticos y quirúrgicos avanzan a una CAGR del 6,12% hasta 2031.
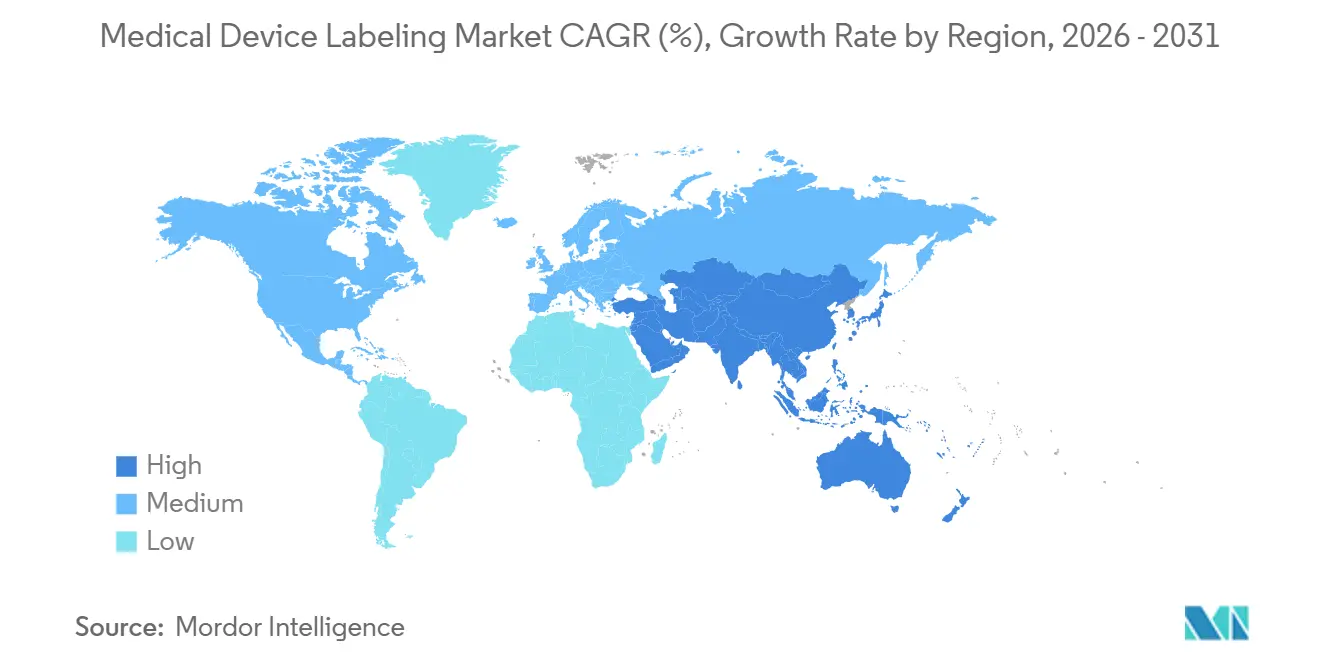
- Por geografía, América del Norte concentró el 45,85% de los ingresos en 2025, aunque se espera que Asia-Pacífico crezca a una CAGR del 6,08% hasta 2031.
Nota: Las cifras del tamaño del mercado y los pronósticos de este informe se generan utilizando el marco de estimación patentado de Mordor Intelligence, actualizado con los datos y conocimientos más recientes disponibles a partir de enero de 2026.
Tendencias e Información del Mercado Global de Etiquetado de Dispositivos Médicos
Análisis del Impacto de los Impulsores
| Impulsor | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Los mandatos globales de UDI y las presentaciones en bases de datos amplían los datos de las etiquetas y los requisitos de códigos de barras en formato dual | +1.2% | Global; América del Norte y la UE lideran | Mediano plazo (2-4 años) |
| Las reglas de traducción y multilingüismo del MDR/IVDR aumentan las unidades de mantenimiento de existencias de etiquetas y el volumen de contenido | +0.9% | Europa; efecto secundario en el Reino Unido y Suiza | Corto plazo (≤ 2 años) |
| El aumento de dispositivos de uso doméstico, portátiles y de diagnóstico en el punto de atención eleva la demanda de etiquetas duraderas y amigables para el paciente | +0.8% | América del Norte y Europa como núcleo; centros urbanos de Asia-Pacífico | Mediano plazo (2-4 años) |
| El aumento de las necesidades de retiro del mercado y rastreo acelera el etiquetado UDI enriquecido con códigos de barras 2D | +0.7% | Global; aplicación más estricta en las jurisdicciones de la FDA y la UE | Corto plazo (≤ 2 años) |
| Adopción de etiquetas inteligentes RFID/NFC para la trazabilidad a nivel de artículo en kits quirúrgicos e implantes | +0.6% | Hospitales de América del Norte y Europa; proyectos piloto en Asia-Pacífico | Largo plazo (≥ 4 años) |
| Los flujos de trabajo de procesamiento estéril impulsan el uso de etiquetas indicadoras y documentación | +0.5% | Entornos hospitalarios globales y de centros de cirugía ambulatoria | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Los Mandatos Globales de UDI y las Presentaciones en Bases de Datos Amplían los Datos de las Etiquetas y los Requisitos de Códigos de Barras en Formato Dual
La FDA de los EE. UU. intensificó la aplicación del GUDID en 2025, emitiendo cartas de advertencia cuando el contenido del código de barras y los campos de la base de datos divergían, por lo que los convertidores ahora validan símbolos 2D hasta etiquetas de 10 mm × 15 mm. China completó su implementación gradual de UDI en 2024, exigiendo que los dispositivos de Clase I lleven identificadores legibles por máquina, lo que impulsa a los exportadores a rediseñar etiquetas con texto bilingüe y simbología GS1 o HIBC [2]Administración Nacional de Productos Médicos, Sistema de Identificación Única de Dispositivos (UDI),
nmpa.gov.cn. Japón, Singapur, Malasia y Brasil adoptaron marcos similares, lo que significa que un modelo de dispositivo puede enviarse con cinco o más variantes de etiqueta regionales. Estos mandatos impulsan a las empresas de dispositivos hacia sistemas de gestión de etiquetas en la nube que automatizan el control de versiones de diseño y el seguimiento de cambios regulatorios.
Las Reglas de Traducción y Multilingüismo del MDR/IVDR Aumentan las Unidades de Mantenimiento de Existencias de Etiquetas y el Volumen de Contenido
Bajo el Reglamento de la UE 2025/1234, vigente desde julio de 2025, los dispositivos de uso profesional pueden reemplazar los folletos en papel con eIFU, pero cada idioma aún necesita un enlace QR único en la etiqueta, lo que multiplica las unidades de mantenimiento de existencias [3]Comisión Europea, Dispositivos Médicos - Nuevas Regulaciones - Orientación,
ec.europa.eu. Una sola bomba de infusión puede requerir 24 diseños de etiqueta para el bloque, lo que aumenta el riesgo de inventario porque el stock impreso en alemán no puede enviarse legalmente a España. Los proveedores de traducción reportan un aumento del 30% en proyectos de etiquetas de dispositivos desde 2024, y los convertidores que ofrecen validación de idiomas interna ganan contratos al acortar los plazos de certificación.
El Aumento de Dispositivos de Uso Doméstico, Portátiles y de Diagnóstico en el Punto de Atención Eleva la Demanda de Etiquetas Duraderas y Amigables para el Paciente
La guía de la FDA publicada en 2024 obliga a los fabricantes a probar la legibilidad con usuarios no especializados, lo que impulsa el tamaño de fuente de 6 puntos a al menos 8 puntos y exige advertencias en lenguaje sencillo. Los monitores continuos de glucosa y las bombas portátiles necesitan etiquetas que soporten el sudor, los desinfectantes y períodos de uso de 10 a 14 días sin irritación cutánea. Las ventas de dispositivos de uso doméstico en los EE. UU. aumentaron un 12% en 2025 tras la expansión del reembolso para el monitoreo remoto, lo que impulsó directamente los volúmenes de etiquetas.
El Aumento de las Necesidades de Retiro del Mercado y Rastreo Acelera el Etiquetado UDI Enriquecido con Códigos de Barras 2D
La FDA registró 87 retiros del mercado de dispositivos de Clase I en 2024, y los hospitales respondieron incorporando escaneos de códigos de barras en las rutinas de admisión y esterilización. Los identificadores de aplicación de GS1 permiten que un Data Matrix lleve número de serie, lote y fecha de vencimiento, minimizando el espacio en la etiqueta y maximizando la densidad de datos. La base de datos europea EUDAMED, obligatoria para nuevos registros desde 2024, vincula aún más las etiquetas físicas con registros en la nube para la vigilancia poscomercialización.
Análisis del Impacto de las Restricciones
| Restricción | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| La carga de cumplimiento y las frecuentes actualizaciones regulatorias aumentan el costo y el tiempo de comercialización para los etiquetadores | -0.6% | Global, con presión aguda en la UE (MDR/IVDR) y China (NMPA) | Corto plazo (≤ 2 años) |
| El panorama fragmentado de conversión de etiquetas intensifica la presión sobre los precios y el margen | -0.4% | Global, más severo en América del Norte y Europa donde la consolidación de compradores está avanzada | Mediano plazo (2-4 años) |
| El marcado directo de piezas (UDI permanente) desplaza algunas etiquetas externas para instrumentos reutilizables | -0.5% | América del Norte y Europa, impulsado por la guía de marcado directo de la FDA y el MDR de la UE | Mediano plazo (2-4 años) |
| La adopción de eIFU reduce el etiquetado de folletos/prospectos en papel para dispositivos de uso profesional | -0.3% | Europa liderando tras el Reglamento 2025/1234; América del Norte y Asia-Pacífico siguiendo | Largo plazo (≥ 4 años) |
| Fuente: Mordor Intelligence | |||
La Carga de Cumplimiento y las Frecuentes Actualizaciones Regulatorias Aumentan el Costo y el Tiempo de Comercialización para los Etiquetadores
La UE emitió 89 documentos de orientación entre 2021 y 2025, cada uno con la posibilidad de alterar el contenido de las etiquetas, mientras que los retrasos de los organismos notificados se extienden hasta 12 meses, lo que obliga a múltiples revisiones de diseño que cuestan entre USD 5.000 y USD 15.000 por iteración. China publicó 14 circulares de UDI en 2024, y la aplicación provincial inconsistente añade incertidumbre para los exportadores. Los pequeños fabricantes gastan hasta una parte notable de las ventas en asuntos regulatorios frente al 2% de las multinacionales, lo que acelera la consolidación de la industria.
El Panorama Fragmentado de Conversión de Etiquetas Intensifica la Presión sobre los Precios y el Margen
Más de 300 convertidores regionales compiten, muchos de ellos operadores de un solo sitio con poder de negociación limitado. Los contratos de compra grupal concentran una parte significativa del gasto en etiquetas en cinco convertidores, mientras que los clientes exigen reducciones de precios anuales del 2 al 3% a pesar del aumento de los costos de certificación ISO 13485 y de sala limpia. Los márgenes brutos se comprimieron del 28% en 2020 al 22% en 2025, lo que provocó salidas y consolidaciones por parte de capital privado. El marcado directo de piezas erosiona aún más la demanda de etiquetas para instrumentos reutilizables.
Análisis de Segmentos
Por Tipo de Etiqueta: La Química Adhesiva Determina la Compatibilidad con la Esterilización
Las etiquetas sensibles a la presión representaron el 57,37% del mercado de etiquetado de dispositivos médicos en 2025, impulsadas por la compatibilidad con líneas de aplicación de 300 a 600 etiquetas por minuto y la esterilización por rayos gamma, óxido de etileno y vapor. Los adhesivos acrílicos o de caucho mantienen la resistencia de unión a través de 50 kGy de irradiación sin amarillamiento. Se prevé que las etiquetas aplicadas con pegamento o pegamento húmedo crezcan al 5,89% hasta 2031, la tasa más rápida, ya que las empresas farmacéuticas envasan inyectables líquidos en viales de vidrio donde la adhesión permanente supera la conveniencia de despegar y volver a sellar. Los sistemas de pegamento húmedo crean uniones mecánicas al penetrar los sustratos, evitando el levantamiento durante la condensación de la cadena de frío, aunque requieren tiempos de permanencia de 10 a 15 segundos que ralentizan las líneas a 150-250 unidades por minuto.
Las mangas termorretráctiles representaron una parte notable del volumen en 2025, favorecidas para productos combinados como jeringas prellenadas con agujas de seguridad integradas, donde los gráficos de 360 grados justifican una prima del 30 al 40%. Las etiquetas en molde siguen siendo un nicho, aplicadas durante el moldeo por soplado o inyección de vasos de muestra, eliminando los pasos posteriores al moldeo. La Directiva de Plásticos de Uso Único de la UE, vigente en 2024, exime a los dispositivos médicos, pero ha impulsado la evaluación de materiales de cara reciclables que coincidan con la resina del envase. UPM Raflatac lanzó una construcción sin revestimiento en 2025 que reduce el desperdicio de material en un 15% y reduce los costos de flete, lo que resulta atractivo para los fabricantes orientados a la sostenibilidad.
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles al adquirir el informe
Por Aplicación: Los Instrumentos Quirúrgicos Superan a los Consumibles en Integración RFID
Los consumibles desechables concentraron el 56,34% de la participación del tamaño del mercado de etiquetado de dispositivos médicos en 2025, lo que refleja los 16 mil millones de jeringas utilizadas anualmente solo en los EE. UU. Sin embargo, los instrumentos terapéuticos y quirúrgicos se están expandiendo al 6,12% hasta 2031, el crecimiento de aplicación más rápido, ya que los hospitales adquieren equipos de capital e incorporan etiquetas RFID en bandejas reutilizables. Un solo procedimiento ortopédico consume entre 40 y 60 instrumentos, cada uno etiquetado y esterilizado entre 200 y 300 veces a lo largo de cinco años, generando una demanda recurrente que supera con creces el etiquetado único de jeringas. Los equipos de monitoreo y diagnóstico representaron participaciones notables del volumen en 2025, requiriendo etiquetas duraderas que soporten años de limpieza con alcohol isopropílico y exposición a rayos UV.
Los dispositivos de uso doméstico y portátiles están reformulando las especificaciones de los consumibles. Los monitores continuos de glucosa necesitan adhesivos de silicona o hidrocoloide que equilibren el uso de 10 a 14 días con una remoción sin dolor, reemplazando los acrílicos agresivos. La guía de etiquetado para pacientes de la FDA de 2024 exige pruebas de comprensión, lo que lleva a fuentes más grandes y advertencias en lenguaje sencillo. Los dispositivos de diagnóstico en el punto de atención crecieron significativamente en 2025 a medida que la distribución se desplazó a las farmacias, multiplicando las variantes de etiquetas porque los dispositivos de venta libre requieren instrucciones de eliminación amigables para el consumidor ausentes en los equivalentes profesionales. La convergencia de la serialización UDI, la adopción de RFID y el diseño centrado en el paciente está elevando la complejidad técnica y el valor unitario en todas las aplicaciones, incluso cuando los precios competitivos comprimen los márgenes de los convertidores.
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles al adquirir el informe
Análisis Geográfico
América del Norte concentró el 45,85% de la participación del mercado de etiquetado de dispositivos médicos en 2025, anclada por la aplicación de UDI de la FDA y los requisitos de sincronización del GUDID. La agencia emitió 14 cartas de advertencia en 2024 por incumplimiento, dirigidas a fabricantes nacionales y extranjeros. Canadá alineó sus Reglamentos de Dispositivos Médicos con los estándares de la FDA en 2024 e introdujo la notificación obligatoria de eventos adversos relacionados con etiquetas, lo que obliga al etiquetado bilingüe en francés e inglés para Quebec. La COFEPRIS de México adoptó el UDI en 2025, creando un bloque regulatorio norteamericano que simplifica el diseño pero impone obligaciones trilingües en inglés, francés y español para la distribución en el marco del T-MEC.
Europa navega las transiciones del MDR e IVDR que exigen instrucciones en el idioma local en Alemania, Francia, Italia, España y Polonia, fragmentando las unidades de mantenimiento de existencias de etiquetas. El marcado UKCA del Reino Unido, obligatorio en 2024, requiere etiquetas separadas para Gran Bretaña frente a Irlanda del Norte, que sigue el MDR de la UE, lo que obliga a inventarios paralelos. El Reglamento 2025/1234, vigente desde julio de 2025, permite el eIFU para dispositivos profesionales, pero mantiene los requisitos de código QR y URL para cada idioma, multiplicando los diseños sin reducir los costos de impresión.
Se prevé que Asia-Pacífico crezca al 6,08% hasta 2031, la CAGR regional más rápida. China completó la implementación del UDI en 2024, exigiendo identificadores de dispositivos de Clase I en la base de datos de la NMPA e impulsando la adopción de códigos de barras en formato dual. El esquema de Incentivos Vinculados a la Producción de India canaliza USD 1.400 millones hacia la fabricación nacional, favoreciendo la adquisición local de etiquetas y atrayendo inversión de convertidores multinacionales en Pune, Ahmedabad y Chennai. La PMDA de Japón aceptó el eIFU en 2024, alineándose con los precedentes de la FDA y la UE, pero mantuvo estrictos estándares de legibilidad en idioma japonés y kanji en la etiqueta. Oriente Medio y África, América del Sur y los mercados más pequeños de Asia-Pacífico representaron colectivamente una participación notable de los ingresos en 2025. La ANVISA de Brasil publicó directrices de UDI en 2024, exigiendo codificación GS1 o HIBC para dispositivos de Clase III y IV antes de 2026. La TGA de Australia armonizó los requisitos de UDI con los marcos de la FDA y la UE en 2024, simplificando el diseño en la región del Pacífico, mientras que la MFDS de Corea del Sur exigió el etiquetado en idioma coreano para las importaciones.
Panorama Competitivo
El mercado de etiquetado de dispositivos médicos sigue siendo fragmentado, con los 10 principales convertidores capturando la mayoría de los ingresos globales. CCL Industries adquirió tres convertidores de etiquetas médicas en América del Norte y Europa durante 2024-2025, integrando listas de clientes en su división de Salud y Especialidades y realizando ventas cruzadas de soluciones RFID. Avery Dennison invirtió USD 25 millones en infraestructura RFID en 2025, instalando líneas de codificación de incrustaciones en sus instalaciones de Oegstgeest, Países Bajos, y Mentor, Ohio, para atender a fabricantes de instrumentos quirúrgicos e implantes. Los convertidores más pequeños se especializan en aplicaciones de alta complejidad, como etiquetas de folleto multicapa, construcciones sin revestimiento y productos híbridos de indicador con código de barras, donde la diferenciación técnica compensa la presión de precios de los productos básicos.
Las oportunidades de espacio en blanco emergen en la intersección del etiquetado digital y los dispositivos conectados. Schreiner Group presentó cuatro patentes en 2024-2025 para construcciones RFID que sobreviven a 1.000 ciclos de esterilización y para diseños de antena optimizados para la trazabilidad de instrumentos metálicos. La integración de cadena de bloques sigue siendo incipiente, aunque los proyectos piloto de Johnson & Johnson y Medtronic en 2025 demostraron registros inmutables que vinculan el UDI serializado con los registros de fabricación y los resultados clínicos. La certificación ISO 13485 se ha convertido en un requisito básico, con los fabricantes de dispositivos exigiendo a los convertidores que demuestren un control validado de cambios de diseño, seguimiento de genealogía de lotes y garantía de esterilidad, favoreciendo a los actores de escala con equipos dedicados de asuntos regulatorios e inspección automatizada sobre los talleres más pequeños que dependen de controles de calidad manuales.
Líderes de la Industria de Etiquetado de Dispositivos Médicos
CCL Industries
Avery Dennison
Schreiner Group
Brady Corporation
All4Labels Group
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Febrero de 2026: Danaher completó una adquisición de USD 9.900 millones de Masimo, un movimiento importante hacia el monitoreo y la atención al paciente basada en datos.
- Marzo de 2025: CCL Industries completó la adquisición de CleanMark Labels, un convertidor estadounidense especializado en etiquetas sensibles a la presión para sala limpia para dispositivos de Clase II y III, añadiendo capacidad certificada por ISO 13485 en Carolina del Norte.
- Enero de 2025: La división MediPharm de Schreiner Group lanzó una etiqueta híbrida de indicador químico y código de barras 2D que integra la validación de esterilización por vapor con el seguimiento automatizado de bandejas, reduciendo el tiempo de documentación de procesamiento estéril en un 40% en implementaciones piloto en 12 hospitales europeos.
Alcance del Informe Global del Mercado de Etiquetado de Dispositivos Médicos
Según el alcance del informe, el etiquetado de dispositivos médicos es un marco de comunicación integral que va mucho más allá de las pegatinas físicas adheridas a un producto. Abarca toda la información escrita, impresa o gráfica proporcionada con un dispositivo, incluido su embalaje, instrucciones de uso (IFU), manuales de usuario e incluso materiales promocionales.
El mercado de etiquetado de dispositivos médicos está segmentado por tipo de etiqueta, aplicaciones y geografía. Por tipo de etiqueta, el mercado está segmentado en etiquetas sensibles a la presión, aplicadas con pegamento, mangas termorretráctiles y en molde. Por tipo de plataforma, el mercado está segmentado en consumibles desechables, equipos de monitoreo y diagnóstico, e instrumentos terapéuticos y quirúrgicos. Geográficamente, el mercado está segmentado en América del Norte, Europa, la región de Asia-Pacífico, Oriente Medio y África, y América del Sur. El informe de mercado también cubre los tamaños de mercado estimados y las tendencias para 17 países en las principales regiones del mundo. Para cada segmento, el tamaño del mercado y el pronóstico se proporcionan en términos de valor (USD).
| Sensibles a la presión |
| Aplicadas con pegamento |
| Mangas termorretráctiles |
| Etiquetas en molde |
| Consumibles desechables |
| Equipos de monitoreo y diagnóstico |
| Instrumentos terapéuticos y quirúrgicos |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | CCG |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tipo de Etiqueta | Sensibles a la presión | |
| Aplicadas con pegamento | ||
| Mangas termorretráctiles | ||
| Etiquetas en molde | ||
| Por Aplicación | Consumibles desechables | |
| Equipos de monitoreo y diagnóstico | ||
| Instrumentos terapéuticos y quirúrgicos | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | CCG | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Cuál es el valor proyectado para 2031?
Se espera que el mercado de etiquetado de dispositivos médicos alcance USD 1,84 mil millones en 2031, creciendo a una CAGR del 5,58% desde 2026.
¿Qué tipo de etiqueta tiene la mayor participación?
Las etiquetas sensibles a la presión concentraron el 57,37% de la participación en 2025, impulsadas por la compatibilidad con líneas de alta velocidad y ciclos de esterilización.
¿Qué segmento de aplicación crece más rápido?
Los instrumentos terapéuticos y quirúrgicos se están expandiendo al 6,12% hasta 2031, impulsados por la integración de RFID en bandejas de instrumentos reutilizables.
¿Qué región lidera en ingresos?
América del Norte representó el 45,85% de los ingresos en 2025, anclada por la aplicación de UDI de la FDA y las auditorías de presentación al GUDID.
Última actualización de la página el:



