Tamaño y Participación del Mercado de Pruebas Diagnósticas de Hepatitis E
Análisis del Mercado de Pruebas Diagnósticas de Hepatitis E por Mordor Intelligence
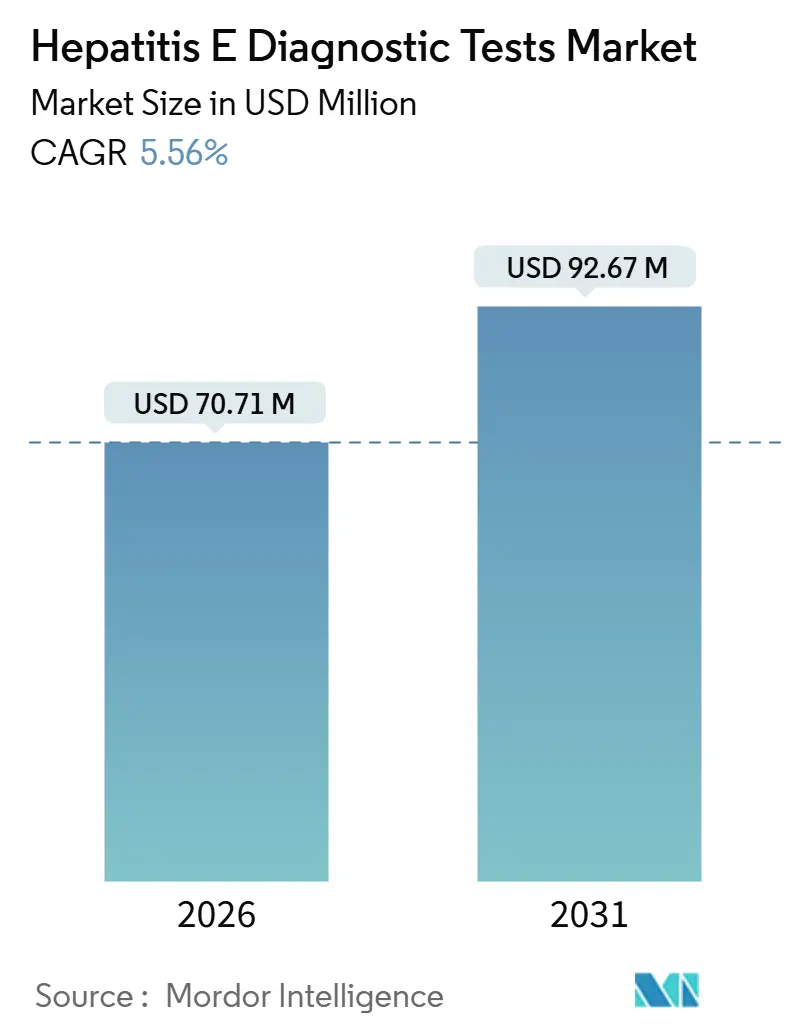
El tamaño del Mercado de Pruebas Diagnósticas de Hepatitis E se estima en 70,71 millones de USD en 2026, y se espera que alcance 92,67 millones de USD en 2031, a una CAGR del 5,56% durante el período de pronóstico (2026-2031).
El aumento de los mandatos de seguridad sanguínea en regiones de altos ingresos, los recurrentes brotes de transmisión hídrica en entornos humanitarios y los avances incrementales en la automatización de ensayos moleculares están desplazando la demanda desde el cribado de anticuerpos en un solo paso hacia plataformas de ácidos nucleicos de alto rendimiento. El ELISA sigue siendo el principal instrumento de vigilancia en los hospitales de Asia-Pacífico, pero su participación disminuye gradualmente a medida que los bancos de sangre adoptan cartuchos de NAT multiplex que detectan simultáneamente el VHE, el VIH, el VHB y el VHC, reduciendo los costos por donación. Los mercados de brotes sensibles al precio continúan favoreciendo las tiras de flujo lateral de IgM que no requieren logística de cadena de frío. Mientras tanto, los programas de vigilancia ambiental están incorporando la PCR en heces a los flujos de trabajo de aguas residuales y seguridad alimentaria, ampliando las pruebas más allá de los laboratorios clínicos. La consolidación se acelera: la adquisición de ELITechGroup por parte de Bruker en 2024 ilustra la escala de capital ahora necesaria para cumplir con las nuevas normas europeas de validación para ensayos en bancos de sangre[1]Bruker Corporation, "Adquisición de ELITechGroup," BRUKER.COM ..
Conclusiones Clave del Informe
- Por tipo de prueba, los kits de ELISA representaron el 43,55% de la participación del mercado de Pruebas Diagnósticas de Hepatitis E en 2025, mientras que se prevé que los ensayos de PCR/NAT avancen a una CAGR del 8,25% hasta 2031.
- Por tipo de muestra, el suero y el plasma representaron el 70,53% del mercado de Pruebas Diagnósticas de Hepatitis E en 2025; se prevé que las pruebas en heces se expandan a una CAGR del 9,85% hasta 2031.
- Por usuario final, los hospitales y clínicas lideraron con una participación de ingresos del 45,23% en 2025, mientras que se proyecta que los bancos de sangre y centros de transfusión crezcan a una CAGR del 8,55% durante el mismo período.
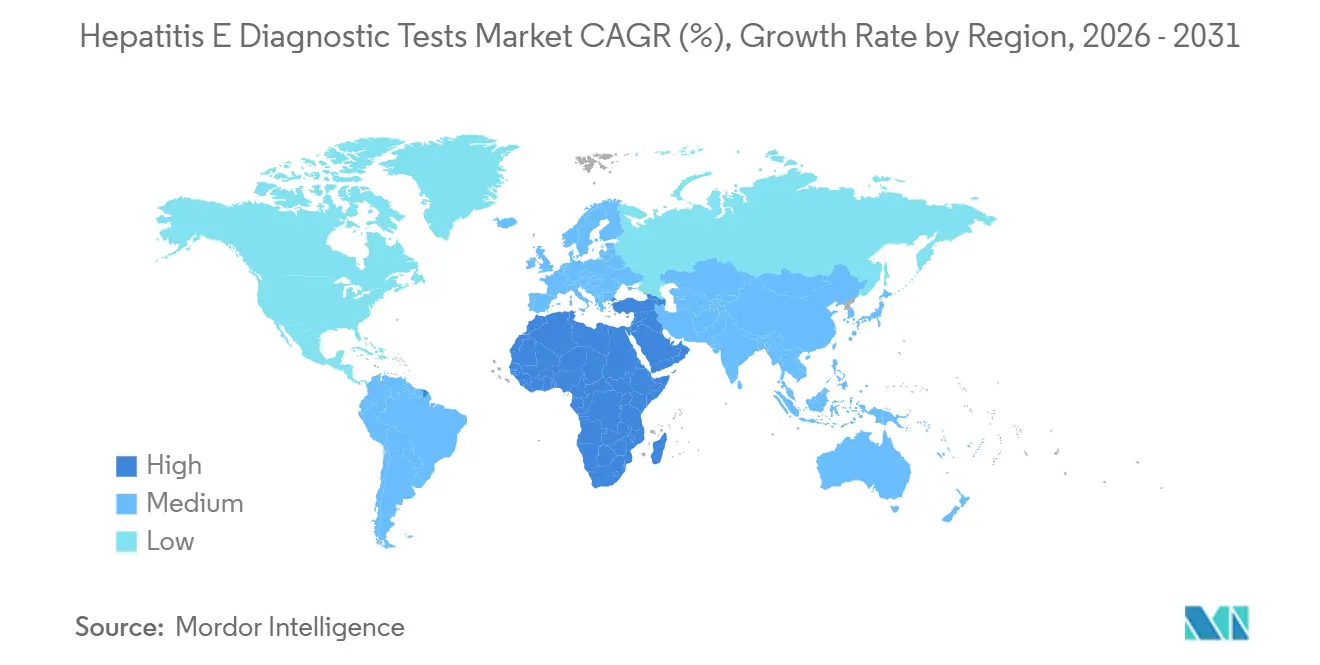
- Por geografía, Asia-Pacífico contribuyó con el 38,13% de los ingresos globales en 2025; se prevé que el segmento de Oriente Medio y África alcance una CAGR del 10,81% hasta 2031.
Nota: Las cifras del tamaño del mercado y los pronósticos de este informe se generan utilizando el marco de estimación patentado de Mordor Intelligence, actualizado con los datos y conocimientos más recientes disponibles a partir de enero de 2026.
Tendencias e Información del Mercado Global de Pruebas Diagnósticas de Hepatitis E
Análisis del Impacto de los Impulsores
| Impulsor | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Aumento de la Incidencia de Brotes de VHE en Regiones Endémicas | +1.2% | África Subsahariana, Asia Meridional, con extensión a los corredores de refugiados de Oriente Medio | Corto plazo (≤ 2 años) |
| Crecientes Mandatos de Cribado de Seguridad Sanguínea en Europa | +1.5% | Europa Occidental (Reino Unido, Irlanda, España), con expansión hacia Europa Central y Oriental | Mediano plazo (2-4 años) |
| Avances Tecnológicos en Diagnóstico Molecular | +1.0% | Global, con adopción temprana en América del Norte, Europa Occidental y Japón | Mediano plazo (2-4 años) |
| Adopción de Pruebas de VHE en Investigación de Xenotrasplante | +0.3% | América del Norte, centros de investigación seleccionados de la UE (Alemania, Países Bajos) | Largo plazo (≥ 4 años) |
| Paneles Multiplex de Medicina del Viajero que Incorporan VHE | +0.4% | América del Norte, Europa Occidental, Australia (mercados con alto volumen de viajes al exterior) | Mediano plazo (2-4 años) |
| Protocolos de Cribado Prenatal en Países de Alto Riesgo | +0.6% | Asia Meridional (India, Bangladesh), África Subsahariana | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Aumento de la Incidencia de Brotes de VHE en Regiones Endémicas
Los brotes de transmisión hídrica en campos de refugiados de Chad y Namibia desplazaron las pruebas esporádicas hacia la adquisición permanente de tiras rápidas de IgM, con más de 5.000 casos confirmados notificados entre 2024 y 2025 únicamente[2]Organización Mundial de la Salud, "Lista de Diagnósticos Esenciales de la OMS 2023," WHO.INT. Las inundaciones monzónicas en los estados indios de Bihar y Odisha produjeron aumentos localizados que desbordaron los laboratorios municipales, lo que motivó licitaciones de emergencia para diagnósticos estables en almacenamiento que no requieren electricidad ni refrigeración. La Lista de Diagnósticos Esenciales 2023 de la Organización Mundial de la Salud precalifica ahora los ensayos rápidos de VHE de Wantai y MP Diagnostics, validando un rendimiento en campo superior al 82% de sensibilidad y una especificidad casi perfecta. Los fabricantes capaces de entregar cartuchos de un solo uso en menos de 15 minutos han captado la mayor parte de los presupuestos de respuesta a brotes, reduciendo las oportunidades para los kits de ELISA procesados por lotes en entornos de bajos recursos. Se espera que la tendencia mantenga las pruebas de primera línea centradas en tiras de flujo lateral, mientras que las cargas de trabajo confirmatorias se trasladan a centros regionales equipados con instrumentos de NAT.
Crecientes Mandatos de Cribado de Seguridad Sanguínea en Europa
El Reglamento 2024/1938 de la Unión Europea obliga ahora a los establecimientos de sangre a validar los ensayos frente a las Normas Internacionales de la OMS que cubren los genotipos 1-4 del VHE[3]Comisión Europea, "Reglamento (UE) 2024/1938 sobre Sustancias de Origen Humano," EUR-LEX.EUROPA.EU. El Reino Unido, Francia y España ya realizan cribado universal de donantes; Alemania y Polonia están pilotando protocolos selectivos para receptores de alto riesgo. Los sistemas Elecsys de Roche y Procleix de Grifols dominan estos entornos de alto rendimiento al ofrecer resultados multiplex en 18 minutos o menos y reducir las rellamadas por falsos positivos[4]Roche Diagnostics, "Ensayos Elecsys Anti-VHE IgM e IgG," ROCHE.COM. Es probable que los costos de cumplimiento empujen a los bancos de sangre regionales más pequeños a externalizar la NAT o a unirse a consorcios que compartan la capacidad de los analizadores. En consecuencia, se espera que el mercado de Pruebas Diagnósticas de Hepatitis E registre colocaciones sostenidas de instrumentos hasta 2028, incluso a medida que los márgenes por prueba se ajusten bajo contratos de compra masiva.
Avances Tecnológicos en Diagnóstico Molecular
Los analizadores de bolsillo están reduciendo la brecha de infraestructura entre el ELISA y la PCR. El prototipo DASH de la Universidad Northwestern ofreció una PCR de VHE en 15 minutos mediante microfluídica y lectura por teléfono inteligente en diciembre de 2025. La autorización de la FDA en junio de 2024 del Xpert HCV de Cepheid estableció un precedente para las aprobaciones de carga viral en el punto de atención, alentando presentaciones similares para el VHE. La PCR digital de gotitas y la RT-LAMP se están adoptando para el monitoreo de aguas residuales, lo que permite a los municipios pronosticar picos días antes de la presentación clínica. Los proveedores que integran extracción, amplificación y detección en cartuchos sellados pueden sortear el cuello de botella del técnico especializado que limita la penetración de la NAT en los hospitales de distrito.
Adopción de Pruebas de VHE en Investigación de Xenotrasplante
Los estudios de transmisión vertical en piaras porcinas mostraron ARN de VHE persistente en lechones recién nacidos, lo que obligó a los programas académicos de trasplante a programar cribados de NAT en serie en las colonias de cría. La guía preliminar de la FDA sobre xenotrasplante y marcos europeos similares exigen ensayos validados y específicos de genotipo para animales donantes, lo que lleva a laboratorios especializados a pagar precios de lista superiores. Aunque los volúmenes de prueba son modestos, los ingresos por muestra son entre 5 y 8 veces superiores a los del diagnóstico clínico rutinario, creando un nicho rentable para los fabricantes de ensayos con capacidad de I+D para personalizar paneles.
Análisis del Impacto de las Restricciones
| Restricción | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Escasa Concienciación y Subnotificación en Áreas Endémicas | -0.7% | Asia Meridional (India, Bangladesh, Nepal), África Subsahariana, partes del Sudeste Asiático y América Latina | Corto plazo (≤ 2 años) |
| Sensibilidad al Precio y Reembolso Limitado | -0.5% | Global, más agudo en países de ingresos bajos y medios (África Subsahariana, Asia Meridional) y mercados de seguros comerciales de EE. UU. | Mediano plazo (2-4 años) |
| Reactividad Cruzada que Genera Preocupaciones por Falsos Positivos | -0.4% | Global, particularmente en poblaciones de baja prevalencia (América del Norte, Europa Occidental, Australia) | Mediano plazo (2-4 años) |
| Perturbaciones en la Cadena de Suministro Porcina que Limitan el Suministro de Reactivos | -0.3% | Centros de fabricación globales (Europa, América del Norte, China), con impacto descendente en la adquisición en todas las regiones | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Escasa Concienciación y Subnotificación en Áreas Endémicas
En muchos países endémicos, los médicos aún recurren por defecto a presunciones de hepatitis A cuando se enfrentan a ictericia aguda, lo que lleva a tasas de prueba que capturan menos del 20% de los casos sospechosos de VHE durante los brotes. La ausencia de notificación obligatoria de casos de VHE interrumpe los circuitos de retroalimentación de datos que de otro modo podrían justificar partidas presupuestarias para diagnósticos. Hasta que los planes de estudios médicos nacionales diferencien los genotipos del VHE y las vías de transmisión, el crecimiento del volumen de pruebas quedará por detrás de la verdadera incidencia de la enfermedad, reduciendo aproximadamente 0,7 puntos porcentuales de la CAGR prevista.
Sensibilidad al Precio y Reembolso Limitado
El boletín de Aetna de 2024 limita el reembolso de la PCR de VHE a pacientes con anticuerpos positivos, excluye el cribado prenatal o de trasplante rutinario y obliga a los laboratorios estadounidenses a facturar bajo códigos genéricos de carga viral, que frecuentemente son denegados. En los países de ingresos bajos y medios, un ELISA de 10 USD supera los ingresos diarios de muchos hogares en riesgo, y los presupuestos públicos priorizan los diagnósticos de VIH, malaria y tuberculosis. Los fabricantes enfrentan márgenes cada vez más ajustados al equilibrar las ventas moleculares de alto precio y bajo volumen en mercados de altos ingresos frente a las licitaciones de pruebas rápidas a precios de producto básico.
Análisis de Segmentos
Por Tipo de Prueba: Los Ensayos Moleculares Ganan Terreno a Pesar del Dominio del ELISA
El ELISA continuó representando el 43,55% de los ingresos del mercado de Pruebas Diagnósticas de Hepatitis E en 2025, respaldado por laboratorios hospitalarios que procesan por lotes grandes volúmenes de muestras a bajos costos variables. El Elecsys Anti-VHE IgM de Roche ofrece resultados en 18 minutos sobre una base instalada de más de 8.000 analizadores cobas en todo el mundo, lo que otorga a los proveedores establecidos un alcance de canal sustancial. El ensayo NAT Procleix de Grifols está ampliando su presencia en los centros de sangre, y su capacidad para detectar ARN de VHE junto con VIH, VHB y VHC está acelerando la adopción multiplex a una CAGR del 8,25%. Los kits de flujo lateral rápido siguen siendo indispensables para la respuesta a brotes: la tira incluida en la lista de la OMS de Wantai produce una lectura visual en 15 minutos y se vende al por mayor a cerca de 1,50 USD por unidad.
La presión sobre los fabricantes de ELISA para innovar va en aumento. Las plataformas de ELISA digital que amplían señales mediante conjugados de nanopartículas prometen un aumento cuádruple en la sensibilidad, lo que permite una detección más temprana tras la exposición; sin embargo, los costos de capital cercanos a 200.000 USD por analizador limitan la adopción a centros terciarios. La industria de Pruebas Diagnósticas de Hepatitis E se está bifurcando, por tanto: los proveedores moleculares persiguen cuentas de transfusión de alto margen, mientras que los especialistas en flujo lateral compiten en costo y vida útil para licitaciones humanitarias. La categoría "Otros" —confirmación por transferencia Western y kits de genotipado para uso exclusivo en investigación— mantiene relevancia en laboratorios de virología de referencia, pero representa menos del 5% del conjunto de valor.
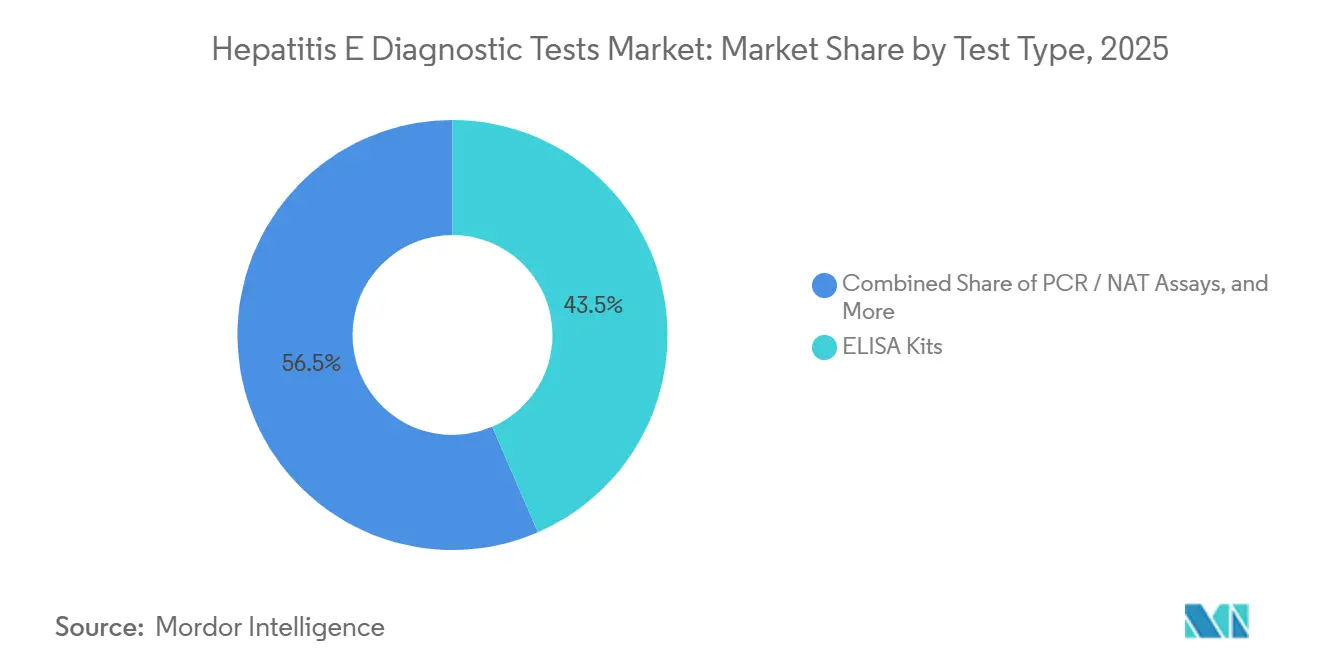
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles con la compra del informe
Por Tipo de Muestra: Las Pruebas en Heces Emergen como el Segmento de Mayor Crecimiento
El suero y el plasma representaron el 70,53% del mercado de Pruebas Diagnósticas de Hepatitis E en 2025, en consonancia con los flujos de trabajo estándar de hepatitis aguda. Los ensayos de ELISA y quimioluminiscencia se integran perfectamente en los analizadores de suero existentes, manteniendo el costo variable por prueba por debajo de 5 USD en entornos de alto volumen. Las pruebas en heces son el segmento de mayor crecimiento, expandiéndose a una CAGR del 9,85% a medida que los municipios añaden ARN de VHE a los paneles de monitoreo de aguas residuales que ya rastrean poliovirus y norovirus. Los laboratorios de seguridad alimentaria también están adoptando la PCR en matriz fecal para certificar lotes de cerdo y mariscos bajo las directrices reforzadas de la UE y el Departamento de Agricultura de EE. UU.
Los avances en los medios de estabilización de ácidos nucleicos permiten ahora que las muestras de heces permanezcan analizables hasta 72 horas a temperatura ambiente, un cambio de paradigma para las clínicas rurales sin infraestructura de cadena de frío. El mercado de Pruebas Diagnósticas de Hepatitis E, por tanto, está en condiciones de beneficiarse de la demanda intersectorial, ya que los programas ambientales adquieren los mismos cartuchos de extracción utilizados en virología clínica. La saliva y la orina siguen siendo matrices en investigación, pero los datos preliminares sugieren una sensibilidad comparable a la del suero durante la primera semana de inicio de los síntomas, lo que apunta a futuros kits de autorecogida para flujos de trabajo de telesalud.
Por Usuario Final: Los Bancos de Sangre Aceleran la Adopción ante los Mandatos de Seguridad en Transfusiones
Los hospitales y clínicas se mantuvieron como los principales generadores de ingresos, con una participación del 45,23% en 2025, apoyándose en gran medida en formatos de ELISA por lotes que aprovechan la automatización de inmunoquímica existente. Sin embargo, los bancos de sangre y centros de transfusión mostraron la trayectoria más rápida, avanzando a una CAGR del 8,55% a medida que jurisdicciones desde Japón hasta Irlanda imponen el cribado universal de NAT. El cambio obliga a los centros a instalar analizadores de alto rendimiento y asegurar cadenas de suministro de reactivos estables, favoreciendo a los proveedores multinacionales que pueden ofrecer contratos de servicio integrados e integración remota de LIMS.
Los laboratorios de referencia diagnóstica ocupan un nivel intermedio resiliente, captando pruebas enviadas externamente que los hospitales más pequeños no pueden realizar internamente. ARUP y Mayo Clinic Laboratories gestionan la genotipificación compleja y la cuantificación de carga viral, aprovechando los nichos de receptores de trasplante e infección crónica. Los laboratorios de medio ambiente y pruebas de alimentos forman el grupo de "Otros Usuarios Finales", una cohorte pequeña pero en crecimiento impulsada por los mandatos de la Autoridad Europea de Seguridad Alimentaria para certificar las cadenas de suministro de cerdo frente a la contaminación por VHE.
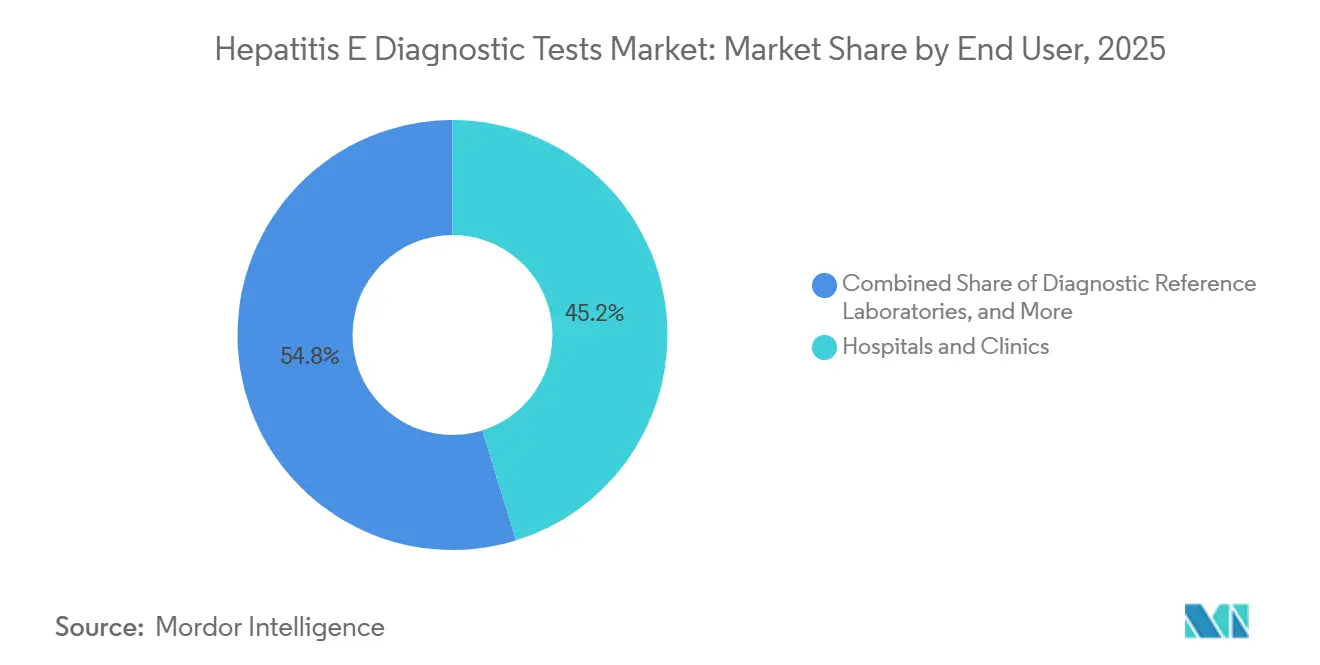
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles con la compra del informe
Análisis Geográfico
Asia-Pacífico mantuvo el liderazgo con el 38,13% de los ingresos globales en 2025, impulsado por la extensa base de ELISA de China y el cribado universal de NAT para donantes en Japón. Los kits prequalificados por la OMS de Wantai dominan las adquisiciones gubernamentales, mientras que BGI Genomics aprovecha los paneles de secuenciación de nueva generación para ganar contratos en los Centros de Control y Prevención de Enfermedades provinciales. La carga endémica de India es alta pero infradiagnosticada; menos del 20% de los casos sospechosos de hepatitis aguda recibieron serología de VHE en 2025, lo que señala una demanda latente una vez que los programas de concienciación maduren.
Europa ocupó el segundo lugar, respaldada por los servicios de sangre del Reino Unido que detectan aproximadamente 1 unidad positiva para VHE por cada 10.000 donaciones. El nuevo Reglamento 2024/1938 eleva los costos de validación de ensayos, pero armoniza la calidad de la NAT entre los estados miembros, fomentando un clima de reembolso predecible. Alemania y Francia aplican cribado selectivo de donantes, centrándose en receptores inmunodeprimidos, mientras que España e Irlanda ejecutan programas universales.
El segmento de Oriente Medio y África es el motor de crecimiento, con una CAGR prevista del 10,81% hasta 2031, ya que los brotes en campos de refugiados obligan a los Ministerios de Salud a almacenar tiras rápidas. El Servicio Nacional de Laboratorios de Salud de Sudáfrica está modernizando la capacidad de PCR provincial en respuesta a grupos urbanos vinculados a asentamientos informales. Los estados del Consejo de Cooperación del Golfo notifican casos importados de genotipo 1 entre trabajadores expatriados, lo que lleva a los hospitales privados a adoptar paneles multiplex de medicina del viajero.
América del Norte sigue siendo más pequeña, ya que Estados Unidos carece de cribado universal de donantes y la incidencia de VHE se mantiene baja fuera de las exposiciones zoonóticas de genotipo 3 en consumidores de cerdo. Canadá está revisando escenarios de costo-beneficio para el cribado selectivo de pacientes inmunodeprimidos, pero aún no existen mandatos. América Latina registra actividad episódica; las autoridades sanitarias de Brasil despliegan tiras de IgM de VHE durante brotes relacionados con inundaciones, mientras que Argentina integra la PCR de VHE en la vigilancia centinela en mataderos.
Panorama Competitivo
El mercado de Pruebas Diagnósticas de Hepatitis E muestra una fragmentación moderada: ninguna empresa supera un porcentaje significativo de los ingresos globales, aunque las ventajas de escala están inclinando el liderazgo hacia un puñado de multinacionales. La adquisición de ELITechGroup por parte de Bruker por 870 millones de EUR en mayo de 2024 señaló el aumento de los umbrales de capital para el desarrollo de ensayos bajo normas de validación de la UE más estrictas. Wantai Biological Pharmacy aprovecha el liderazgo en costos y la precalificación de la OMS para dominar las licitaciones públicas en países de ingresos bajos y medios, frecuentemente agrupando tiras rápidas y reactivos de ELISA a precios escalonados.
Roche y bioMérieux defienden los segmentos hospitalarios premium mediante la integración de analizadores y la conectividad con sistemas de información de laboratorio, ofreciendo protocolos de quimioluminiscencia de IgM/IgG en 30 minutos que se integran con las flotas existentes de cobas y VIDAS. Grifols gana participación en bancos de sangre con su NAT multiplex Procleix, y la empresa anunció recientemente un software de resolución de problemas remota que reduce el tiempo de inactividad en un 25%, consolidando aún más su base instalada.
Los disruptores emergentes se agrupan en dos campos. Las empresas chinas de secuenciación de nueva generación como BGI Genomics reducen los precios de lista occidentales hasta en un 30% al tiempo que agrupan la genotipificación de VHE con paneles de patógenos más amplios, atrayendo a laboratorios de salud pública provinciales. Los especialistas en pruebas rápidas como Biopanda y Healgen actualizaron los diseños de sus casetes en 2025, acortando el tiempo de lectura a 10-15 minutos y mejorando la sensibilidad por encima del 99%. La NAT en el punto de atención sigue siendo un área poco atendida; el prototipo DASH de la Universidad Northwestern destaca el potencial sin explotar de los cartuchos moleculares sin instrumento capaces de ofrecer precisión de nivel PCR a pie de cama.
El cumplimiento normativo está emergiendo como una barrera de entrada. El requisito de validación por genotipo de la UE y las normas de trazabilidad de la OMS favorecen a las empresas con amplios presupuestos de ensayos clínicos y sistemas globales de gestión de calidad, creando objetivos de adquisición entre los fabricantes de serología más pequeños que carecen de recursos para navegar por aprobaciones de múltiples niveles.
Líderes de la Industria de Pruebas Diagnósticas de Hepatitis E
-
Abbott Laboratories
-
Bio-Rad Laboratories Inc.
-
QIAGEN N.V.
-
Shenzhen Mindray Bio-Medical Electronics Co., Ltd.
-
Thermo Fisher Scientific Inc.
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Julio de 2025: Bioars S.A. introdujo kits de ELISA de prueba única para los sistemas Alegria y Alegria 2, que cubren los anticuerpos IgG e IgM de hepatitis E.
- Mayo de 2024: Bruker finalizó la adquisición de ELITechGroup por 870 millones de EUR, añadiendo capacidad de producción de diagnóstico molecular y ampliando su catálogo de ensayos para enfermedades infecciosas.
Alcance del Informe Global del Mercado de Pruebas Diagnósticas de Hepatitis E
Según el alcance del informe, el diagnóstico de hepatitis E se refiere a los métodos de laboratorio utilizados para detectar la infección causada por el virus de la hepatitis E (VHE), que afecta principalmente al hígado y se transmite comúnmente a través de agua o alimentos contaminados. El diagnóstico se basa principalmente en pruebas serológicas que identifican anticuerpos anti-VHE IgM e IgG en sangre, lo que indica una infección reciente o pasada. Las pruebas moleculares, como la RT-PCR, también se utilizan para detectar ARN de VHE para el diagnóstico temprano y confirmatorio. Estas pruebas ayudan a los médicos a confirmar la infección, monitorear brotes y orientar el manejo adecuado del paciente.
La segmentación del mercado de pruebas diagnósticas de hepatitis E incluye tipo de prueba, tipo de muestra, usuario final y geografía. Por tipo de prueba, el mercado se segmenta en kits de ELISA, ensayos de PCR/NAT, pruebas de flujo lateral rápido y otros. Por tipo de muestra, el mercado se segmenta en suero/plasma, heces y otros. Por usuario final, el mercado se segmenta en hospitales y clínicas, laboratorios de referencia diagnóstica, bancos de sangre y centros de transfusión, y otros usuarios finales. Por geografía, el mercado global se segmenta en América del Norte, Europa, Asia-Pacífico, Oriente Medio y África, y América del Sur. El informe de mercado también cubre los tamaños de mercado estimados y las tendencias para 17 países en las principales regiones del mundo. El informe ofrece el valor (en USD) para los segmentos anteriores.
| Kits de ELISA |
| Ensayos de PCR/NAT |
| Pruebas de Flujo Lateral Rápido |
| Otros |
| Suero/Plasma |
| Heces |
| Otros Tipos de Muestra |
| Hospitales y Clínicas |
| Laboratorios de Referencia Diagnóstica |
| Bancos de Sangre y Centros de Transfusión |
| Otros Usuarios Finales |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| India | |
| Japón | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | Consejo de Cooperación del Golfo |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tipo de Prueba | Kits de ELISA | |
| Ensayos de PCR/NAT | ||
| Pruebas de Flujo Lateral Rápido | ||
| Otros | ||
| Por Tipo de Muestra | Suero/Plasma | |
| Heces | ||
| Otros Tipos de Muestra | ||
| Por Usuario Final | Hospitales y Clínicas | |
| Laboratorios de Referencia Diagnóstica | ||
| Bancos de Sangre y Centros de Transfusión | ||
| Otros Usuarios Finales | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| India | ||
| Japón | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | Consejo de Cooperación del Golfo | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Qué impulsa el lanzamiento de nuevos productos en el mercado de Pruebas Diagnósticas de Hepatitis E?
Los mandatos de seguridad sanguínea y la creciente frecuencia de brotes recompensan los ensayos que acortan los tiempos de respuesta y multiplexan el VHE con otros patógenos.
¿Qué formato de prueba crece más rápido?
Los ensayos de PCR/NAT se están expandiendo a una CAGR del 8,25% a medida que los bancos de sangre migran hacia la detección de ARN específica de genotipo.
¿Por qué la PCR en heces está ganando atención?
Los programas de aguas residuales y seguridad alimentaria utilizan la PCR en matriz fecal para pronosticar la transmisión comunitaria, impulsando este tipo de muestra hacia una CAGR del 9,85%.
¿Cómo están afectando las regulaciones europeas a los proveedores?
El Reglamento 2024/1938 impone la validación por genotipo y la trazabilidad según las normas de la OMS, elevando los costos de cumplimiento y estimulando la consolidación.
¿Qué limita la adopción en los países endémicos?
La escasa concienciación clínica y la sensibilidad al precio de los pacientes frenan las pruebas rutinarias a pesar de la alta carga de enfermedad.
Última actualización de la página el:



