Tamaño y Participación del Mercado de TIC para Atención Médica y Dispositivos Médicos
Análisis del Mercado de TIC para Atención Médica y Dispositivos Médicos por Mordor Intelligence
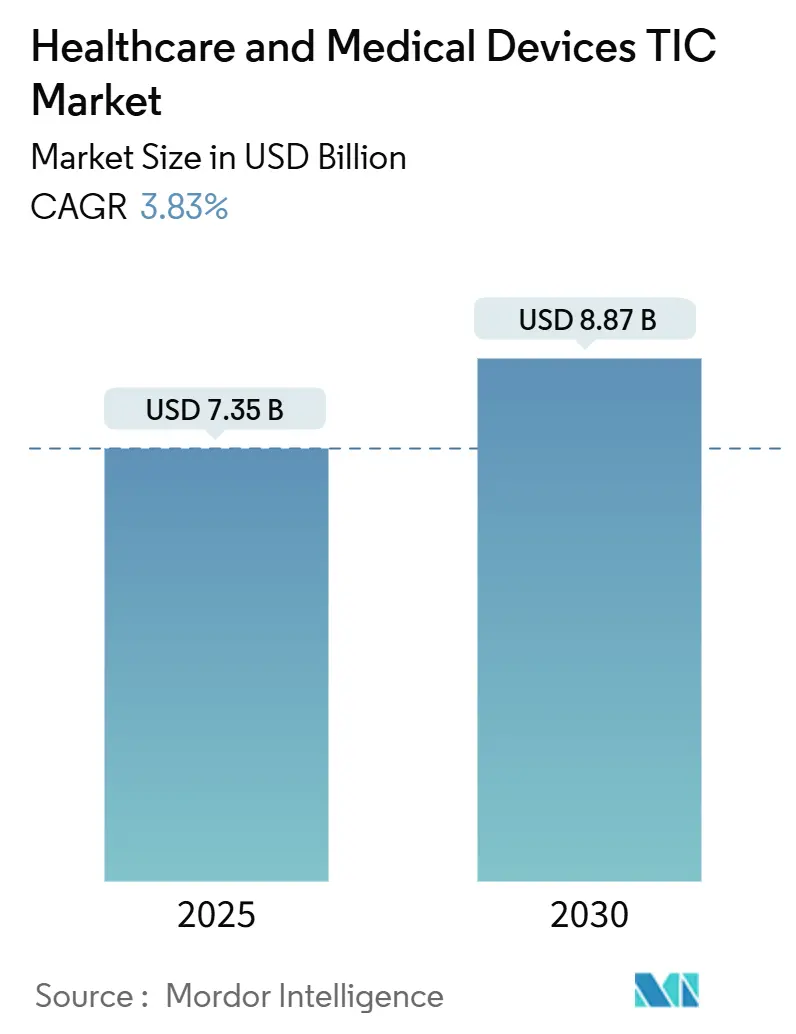
El mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos está valorado actualmente en USD 7,35 mil millones en 2025 y se proyecta que alcance los USD 8,87 mil millones en 2030, lo que refleja una CAGR del 3,83% durante el período de pronóstico. Los marcos de cumplimiento global obligatorios, la creciente complejidad de los dispositivos y la acelerada armonización regulatoria sustentan una demanda estable incluso cuando los presupuestos de atención médica se ajustan. La concentración manufacturera de Asia-Pacífico y la rápida evolución regulatoria respaldan el dominio regional, mientras que los retiros del mercado impulsados por la ciberseguridad y los diagnósticos habilitados por IA amplían el alcance de la validación. Los proveedores de TIC establecidos aprovechan las acreditaciones multijurisdiccionales y la automatización de laboratorios para mantener el poder de fijación de precios frente a los especialistas regionales fragmentados. La escasez de talento, especialmente para auditores biomédicos, y el aumento de los costos de los modelos de biocompatibilidad moderan las perspectivas de crecimiento, pero persisten oportunidades considerables de consolidación y especialización en nichos.
Conclusiones Clave del Informe
- Por tipo de servicio, los Servicios de Pruebas lideraron con el 53,6% de la participación del mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos en 2024, mientras que los Servicios de Certificación avanzan a una CAGR del 4,2% hasta 2030.
- Por tipo de abastecimiento, los modelos Externalizados representaron el 69,3% del tamaño del mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos en 2024 y se prevé que se expandan a una CAGR del 3,9% entre 2025 y 2030.
- Por geografía, Asia-Pacífico capturó el 44,7% de la participación de ingresos del mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos en 2024; se prevé que la región registre la CAGR más rápida del 4,5% hasta 2030.
Tendencias e Información del Mercado Global de TIC para Atención Médica y Dispositivos Médicos
Análisis del Impacto de los Impulsores
| Impulsor | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Aumento en la complejidad y miniaturización de dispositivos | +0.8% | Global, con concentración en América del Norte y Asia-Pacífico | Mediano plazo (2-4 años) |
| Expansión de la armonización regulatoria global (MDSAP, IVDR) | +0.7% | Global, liderado por América del Norte, la UE y la adopción en Asia-Pacífico | Largo plazo (≥ 4 años) |
| Crecimiento de diagnósticos domiciliarios y portátiles | +0.6% | América del Norte y la UE son primarios, Asia-Pacífico está emergiendo | Corto plazo (≤ 2 años) |
| El aumento de retiros del mercado impulsa el gasto en pruebas preventivas | +0.5% | Global, con el mayor impacto en América del Norte | Mediano plazo (2-4 años) |
| Protocolos de pruebas rápidas habilitados por IA | +0.4% | América del Norte y la UE son de adopción temprana, y Asia-Pacífico está siguiendo. | Largo plazo (≥ 4 años) |
| Demanda de pruebas de reacondicionamiento en economía circular | +0.3% | La UE lidera, América del Norte adopción selectiva | Largo plazo (≥ 4 años) |
| Fuente: Mordor Intelligence | |||
Aumento en la Complejidad y Miniaturización de Dispositivos
Los dispositivos portátiles ahora combinan sensores, conectividad y motores de IA que exigen la evaluación simultánea de la precisión del sensor, la compatibilidad electromagnética, la fiabilidad del software y la seguridad cutánea en diversas condiciones del mundo real. Los ciclos de validación modernos también deben verificar el aprendizaje continuo de algoritmos, lo que lleva a los fabricantes a establecer asociaciones de pruebas recurrentes en lugar de proyectos episódicos.[1]FDA, "La FDA aprueba el primer dispositivo médico habilitado por IA para pruebas domiciliarias de apnea del sueño," FDA.GOV Los protocolos que requieren mucho talento elevan los costos del proyecto, pero aseguran ingresos predecibles para los proveedores de TIC que mantienen equipos multidisciplinarios y herramientas avanzadas de simulación.
Expansión de la Armonización Regulatoria Global (MDSAP, IVDR)
El marco MDSAP permite que una sola auditoría satisfaga a cinco organismos reguladores, reduciendo los gastos de cumplimiento del fabricante en aproximadamente un 30-40%, pero aumentando la demanda de empresas de TIC con reconocimiento simultáneo en Estados Unidos, Canadá, Australia, Japón y Brasil.[2]Health Canada, "Programa de Auditoría Única para Dispositivos Médicos," CANADA.CA La adopción del IVDR en Europa refleja esta tendencia, ampliando las categorías de dispositivos sujetos a rigurosas pruebas de rendimiento diagnóstico y concentrando así el negocio en proveedores acreditados a nivel global.
Crecimiento de Diagnósticos Domiciliarios y Portátiles
La FDA aprobó más de 50 dispositivos de salud digital para uso doméstico en 2024, incluidos monitores de apnea del sueño y glucosa vinculados a teléfonos inteligentes que requieren evaluaciones de ciberseguridad, usabilidad y robustez en múltiples entornos más allá de las pruebas de banco clásicas. La economía de la atención descentralizada alienta a los pagadores a reembolsar el monitoreo remoto, ampliando los ingresos para las empresas de TIC que poseen laboratorios de simulación domiciliaria y conjuntos de habilidades de pruebas de penetración de IoT.
El Aumento de Retiros del Mercado Impulsa el Gasto en Pruebas Preventivas
Un aumento del 400% en los retiros de dispositivos entre 2013 y 2018, impulsado en gran medida por vulnerabilidades de software y redes, llevó a los fabricantes a aumentar los presupuestos de pruebas al 15-25% del gasto en desarrollo frente al histórico 8-12%. La validación preventiva ahora compensa los costos de retiro, con un promedio de USD 10-50 millones, lo que ancla compromisos más sólidos en etapas tempranas para los especialistas en TIC.
Análisis del Impacto de las Restricciones
| Restricción | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Escasez de auditores de TIC biomédicos calificados | -0.4% | Global, más aguda en América del Norte y la UE | Corto plazo (≤ 2 años) |
| Reducción de la financiación de capital de riesgo en empresas emergentes de tecnología médica | -0.3% | Global, con el mayor impacto en América del Norte | Mediano plazo (2-4 años) |
| Ciberriesgos de integridad de datos en dispositivos conectados | -0.2% | Global, concentrado en mercados digitalmente avanzados | Largo plazo (≥ 4 años) |
| Aumento de costos para modelos animales de biocompatibilidad | -0.2% | Global, con la UE liderando la adopción de alternativas | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Escasez de Auditores de TIC Biomédicos Calificados
La contratación de auditores especializados requiere de 5 a 7 años de formación interdisciplinaria; las jubilaciones superan al nuevo talento en una proporción de aproximadamente dos a uno, lo que produce una brecha de personal del 25-30% y alimenta una inflación salarial anual del 15-20%.[3]Oficina de Estadísticas Laborales, "Científicos Médicos," BLS.GOV Los proveedores están automatizando la captura de datos y las evaluaciones remotas para mitigar los cuellos de botella, pero aún no pueden capitalizar la expansión de capacidad a corto plazo.
Reducción de la Financiación de Capital de Riesgo en Empresas Emergentes de Tecnología Médica
La inversión global en tecnología médica cayó a USD 19,1 mil millones en 2024 desde un pico de USD 22,1 mil millones en 2021, reduciendo los canales de dispositivos en etapa temprana y retrasando los contratos de TIC hasta hitos posteriores. Las empresas emergentes con restricciones de efectivo ahora comprimen los alcances de validación, desplazando el calendario de ingresos para los proveedores de TIC.
Análisis de Segmentos
Por Tipo de Servicio: Los Servicios de Pruebas Mantienen la Primacía Mientras las Certificaciones se Aceleran
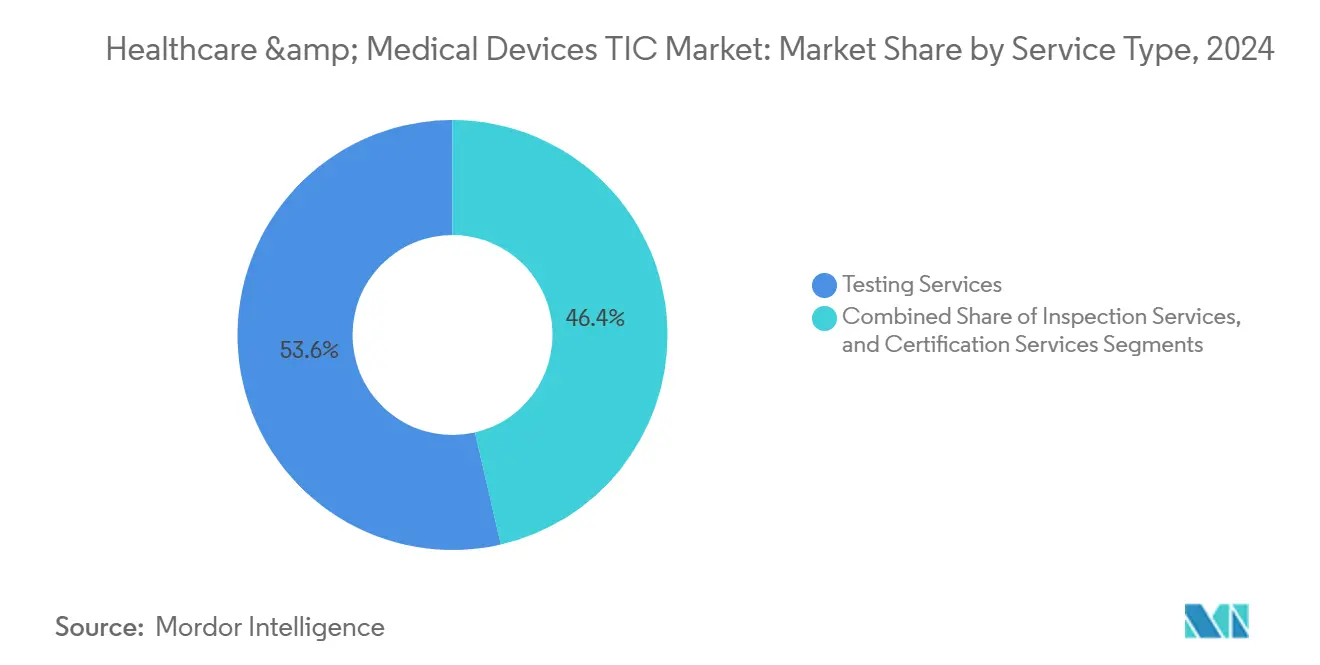
Los Servicios de Pruebas generaron la mayor participación del mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos con el 53,6% en 2024, impulsados por las evaluaciones de materiales ISO 10993 y las verificaciones obligatorias de compatibilidad electromagnética. La amplitud del segmento abarca protocolos de biocompatibilidad, seguridad eléctrica y ciberseguridad, cada uno escalando con la conectividad de los dispositivos y la adopción de IA. Aunque el crecimiento se modera a medida que algunas pruebas se consolidan bajo marcos armonizados, la creciente complejidad del diseño sostiene el volumen y la resiliencia del margen.
Los Servicios de Certificación, si bien representan una porción menor del tamaño del mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos, registraron la CAGR más rápida del 4,2%. Los fabricantes invierten cada vez más en certificaciones de fuente única que satisfacen simultáneamente el MDSAP y el IVDR, intercambiando tarifas iniciales por lanzamientos globales más rápidos. Los Servicios de Inspección, con aproximadamente una cuarta parte de los ingresos, se benefician de los mandatos de transparencia de la cadena de suministro, pero se expanden más lentamente a medida que las auditorías remotas ganan terreno.
Los efectos de segundo orden refuerzan la interacción entre segmentos: las certificaciones avanzadas a menudo incluyen pruebas previas requisito, y las auditorías exitosas alimentan inspecciones de vigilancia recurrentes. Los proveedores de TIC que integran las tres ofertas en plataformas en la nube monetizan los ciclos de vida de cumplimiento de extremo a extremo, atrayendo tanto a multinacionales como a innovadores con recursos limitados.


Por Tipo de Abastecimiento: La Externalización Continúa Superando a los Modelos Internos
La externalización representó el 69,3% de la participación del mercado de pruebas, inspección y certificación de atención médica y dispositivos médicos en 2024 y registra una CAGR del 3,9% hasta 2030. Los crecientes desembolsos de capital para cámaras especializadas, salas limpias y laboratorios de ciberseguridad, a menudo de USD 10-50 millones por instalación, hacen que las asociaciones externas sean económicas para las empresas emergentes e incluso para los grandes fabricantes de equipos originales que buscan capacidad adicional.
Las capacidades internas, aunque estratégicas para las líneas de productos principales, enfrentan restricciones de talento y rápida obsolescencia a medida que evolucionan los estándares. Algunas multinacionales ahora operan modelos híbridos en los que las pruebas de software crítico o materiales propietarios permanecen en las instalaciones, mientras que los laboratorios de terceros manejan la coexistencia inalámbrica, el sesgo de IA y las certificaciones de nicho internacionales. La dinámica alienta a los proveedores de TIC a ubicarse cerca de los principales clústeres de fabricación, ofreciendo infraestructura compartida y portales de datos en tiempo real que se integran con los ciclos de diseño de los fabricantes de equipos originales.
Análisis Geográfico
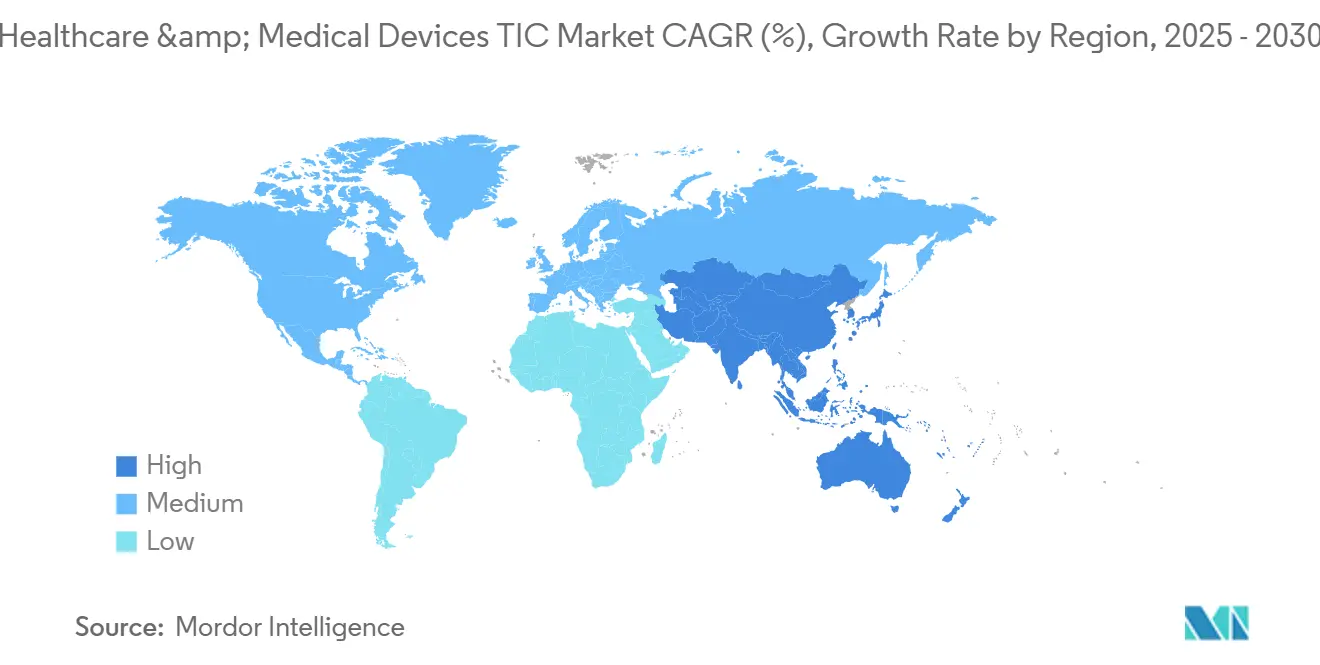
Asia-Pacífico capturó el 44,7% de los ingresos globales en 2024 y se proyecta que registre una CAGR del 4,5% hasta 2030, convirtiendo a la región en el motor de crecimiento del mercado de pruebas, inspección y certificación de dispositivos médicos. Las reformas de la Administración Nacional de Productos Médicos (NMPA) de China sincronizan las normas nacionales con los estándares ISO e IEC al tiempo que exigen informes de pruebas locales, consolidando la demanda de laboratorios acreditados internacionalmente.[4]Administración Nacional de Productos Médicos, "Actualizaciones Regulatorias," NMPA.GOV.CN Japón y Corea del Sur añaden necesidades premium de validación de ciberseguridad e IA, mientras que el Sudeste Asiático gana terreno para ensayos rutinarios de bajo costo bajo la armonización de la ASEAN.
América del Norte mantuvo una participación de mercado del 28% en 2024 y se prevé que se expanda moderadamente a una CAGR del 3,2%. Estados Unidos lidera con proyectos de alto margen en evaluaciones de riesgo de dispositivos conectados a medida que la FDA examina las divulgaciones de listas de materiales de software. La participación de Canadá en el MDSAP sostiene sinergias de auditoría transfronteriza, mientras que los laboratorios de menor costo de México atraen segmentos de pruebas básicas para las cadenas de suministro regionales.
Europa representó el 22% de los ingresos de 2024 a medida que el MDR y el IVDR transformaron las autocertificaciones heredadas en compromisos formales de TIC. Alemania y el Reino Unido dominan el volumen, con certificaciones duales UE-Reino Unido que abren oportunidades incrementales tras el Brexit. Las regulaciones de economía circular catalizan nichos de pruebas de reacondicionamiento y ciclo de vida, y el RGPD impulsa un mayor escrutinio sobre la integridad de los datos de los pacientes.


Panorama Competitivo
El liderazgo global permanece disperso, situando a la industria de pruebas, inspección y certificación de dispositivos médicos en un nivel moderadamente concentrado. SGS, Intertek, TÜV SÜD y Bureau Veritas aprovechan más de 1.000 reconocimientos gubernamentales y extensas redes de laboratorios para diferenciarse de los especialistas regionales. La reciente autorización de SGS Shanghái con cero observaciones del Formulario 483 de la FDA ejemplifica la profundidad de credenciales que genera primas de precios.
La transformación digital sustenta las ventajas competitivas. La automatización FlexLab X de Siemens Healthineers y los conjuntos de robótica de Merck ilustran el giro hacia el rendimiento impulsado por IA, mitigando la escasez de auditores y elevando la fidelidad de los datos. La ciberseguridad, las auditorías de sesgo de algoritmos y la validación de dispositivos reacondicionados constituyen espacios en blanco lucrativos donde los expertos más pequeños pueden escalar rápidamente o convertirse en objetivos de adquisición, como lo demuestra la compra de USD 405 millones de Mérieux NutriSciences del negocio de pruebas de alimentos de Bureau Veritas para duplicar su presencia en Asia-Pacífico.
Se espera que el impulso de fusiones y adquisiciones continúe, impulsado por el interés del capital privado y las operaciones intersectoriales sinérgicas que combinan carteras ambientales, farmacéuticas y de tecnología médica para la conveniencia del usuario final. Los precios siguen siendo resilientes dada la escasez de acreditaciones y los altos costos de cambio, aunque la inflación salarial y las inversiones en tecnología regulatoria comprimen los márgenes para las empresas que carecen de escala o planes de automatización.
Líderes de la Industria de TIC para Atención Médica y Dispositivos Médicos
SGS SA
Bureau Veritas SA
Intertek Group plc
TÜV SÜD AG
TÜV Rheinland AG
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial


Desarrollos Recientes de la Industria
- Marzo de 2025: Merck lanzó soluciones de automatización de laboratorios y robótica para el control de calidad farmacéutico, asociándose con empresas de ingeniería para ofrecer sistemas integrados de pruebas microbiológicas.
- Febrero de 2025: GN Store Nord reportó un gasto en I+D de DKK 1,9 mil millones, enfatizando marcos centralizados de calidad y seguridad de productos para dispositivos auditivos habilitados por IA (USD 0,29 mil millones).
- Enero de 2025: Eurofins Scientific adquirió SF Analytical Laboratories, ampliando su alcance en pruebas ambientales y de alimentos en Estados Unidos.
- Octubre de 2024: Mérieux NutriSciences acordó adquirir la división de pruebas de alimentos de Bureau Veritas por EUR 360 millones (USD 405 millones).
Alcance del Informe Global del Mercado de TIC para Atención Médica y Dispositivos Médicos
| Servicios de Pruebas |
| Servicios de Inspección |
| Servicios de Certificación |
| Interno |
| Externalizado |
| América del Norte | Estados Unidos | |
| Canadá | ||
| México | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Rusia | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Corea del Sur | ||
| Sudeste Asiático | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | Oriente Medio | Arabia Saudita |
| Emiratos Árabes Unidos | ||
| Turquía | ||
| Resto de Oriente Medio | ||
| África | Sudáfrica | |
| Nigeria | ||
| Resto de África | ||
| Por Tipo de Servicio | Servicios de Pruebas | ||
| Servicios de Inspección | |||
| Servicios de Certificación | |||
| Por Tipo de Abastecimiento | Interno | ||
| Externalizado | |||
| Por Geografía | América del Norte | Estados Unidos | |
| Canadá | |||
| México | |||
| América del Sur | Brasil | ||
| Argentina | |||
| Resto de América del Sur | |||
| Europa | Alemania | ||
| Reino Unido | |||
| Francia | |||
| Italia | |||
| España | |||
| Rusia | |||
| Resto de Europa | |||
| Asia-Pacífico | China | ||
| Japón | |||
| India | |||
| Corea del Sur | |||
| Sudeste Asiático | |||
| Resto de Asia-Pacífico | |||
| Oriente Medio y África | Oriente Medio | Arabia Saudita | |
| Emiratos Árabes Unidos | |||
| Turquía | |||
| Resto de Oriente Medio | |||
| África | Sudáfrica | ||
| Nigeria | |||
| Resto de África | |||


Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño actual del mercado global de pruebas, inspección y certificación de atención médica y dispositivos médicos?
El mercado se sitúa en USD 7,35 mil millones en 2025 y se proyecta que alcance los USD 8,87 mil millones en 2030.
¿Qué región contribuye más ingresos a los servicios de cumplimiento de dispositivos médicos?
Asia-Pacífico lidera con el 44,7% de los ingresos globales, impulsado por la escala manufacturera y la madurez regulatoria.
¿Por qué los servicios de certificación crecen más rápido que los servicios de pruebas?
Los marcos armonizados como el MDSAP y el IVDR permiten que un solo certificado abra múltiples mercados, haciendo que la certificación de terceros sea más valiosa.
¿Cuál es el principal desafío que limita el crecimiento de capacidad a corto plazo para los proveedores de TIC?
Una escasez del 25-30% de auditores biomédicos calificados está limitando la expansión del servicio a pesar de la creciente demanda.
¿Cómo se compara la externalización con las pruebas internas?
La externalización controla el 69,3% del gasto total porque los laboratorios especializados reducen los desembolsos de capital y aceleran las aprobaciones en múltiples países.
¿Qué nichos emergentes ofrecen el mayor potencial para las empresas de TIC?
Las áreas de alto margen incluyen la validación de ciberseguridad para dispositivos conectados, las auditorías de sesgo de algoritmos de IA y las pruebas de reacondicionamiento en economía circular.
Última actualización de la página el:









