Tamaño y Participación del Mercado de Organizaciones de Investigación por Contrato (CRO) para Ensayos Clínicos Descentralizados
Análisis del Mercado de Organizaciones de Investigación por Contrato (CRO) para Ensayos Clínicos Descentralizados por Mordor Intelligence
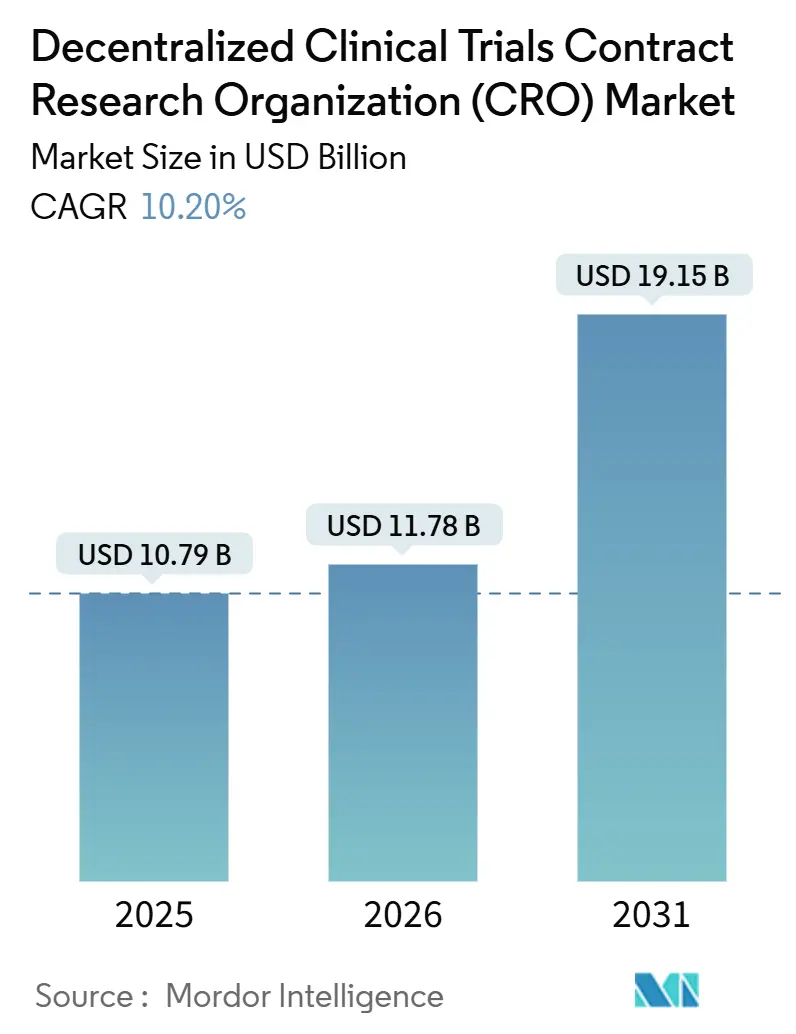
El Mercado de Organizaciones de Investigación por Contrato para Ensayos Clínicos Descentralizados fue valorado en 10,79 mil millones de USD en 2025 y se espera que crezca desde 11,78 mil millones de USD en 2026 hasta alcanzar los 19,15 mil millones de USD en 2031, a una CAGR del 10,20% durante el período de pronóstico (2026-2031).
Los patrocinadores están migrando hacia modelos de reclutamiento centrados en el paciente que comprimen los plazos y reducen los costos fijos de los sitios, mientras que los reguladores en Estados Unidos, Europa y China han emitido directrices que legitiman la captura remota de datos, las visitas por telemedicina y el consentimiento híbrido. Las CRO de servicio completo siguen siendo los mayores contribuyentes de ingresos, aunque el software eClinical modular está erosionando su participación contractual a medida que los patrocinadores licencian plataformas directamente y adquieren servicios funcionales a la carta. La inversión continua en motores de reclutamiento basados en inteligencia artificial y la integración de sensores portátiles subraya el giro tecnológico del mercado, incluso cuando los riesgos de ciberseguridad y la fragmentación de la privacidad de datos añaden cargas presupuestarias y de cumplimiento normativo. En términos generales, la creciente complejidad terapéutica y la necesidad de evidencia del mundo real mantienen el crecimiento firmemente positivo a pesar de los vientos en contra en costos y la escasez de talento.
Conclusiones Clave del Informe
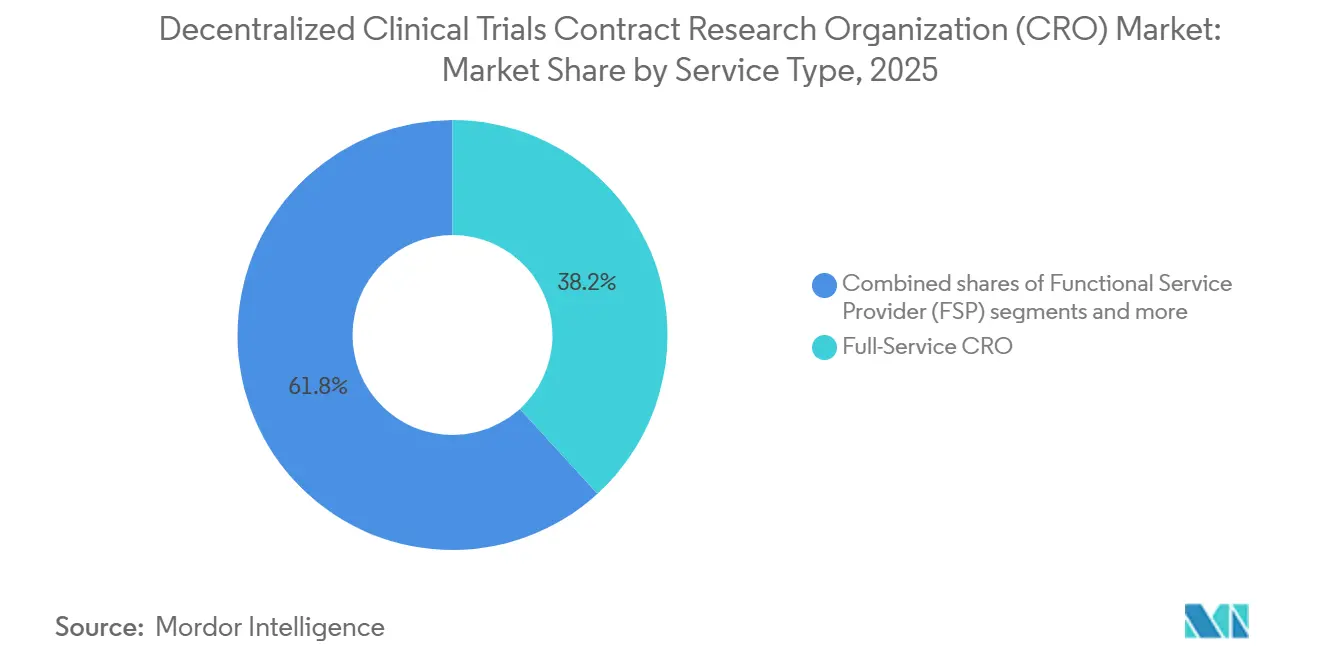
- Por tipo de servicio, las CRO de servicio completo lideraron con una participación de ingresos del 38,23% en 2025; se prevé que la provisión de plataformas eClinical se expanda a una CAGR del 12,00% hasta 2031.
- Por fase del ensayo, la Fase III representó el 55,23% de la participación de ingresos en 2025; la vigilancia poscomercialización de Fase IV avanza a una CAGR del 11,50% hasta 2031.
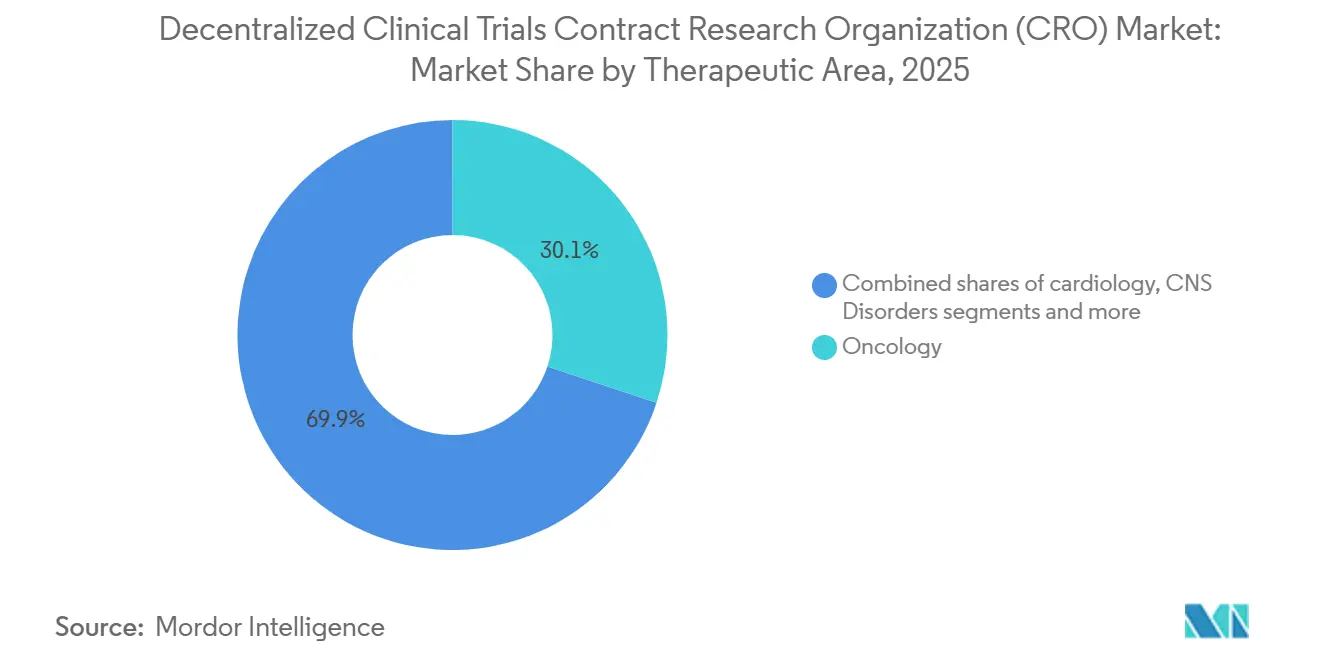
- Por área terapéutica, la oncología captó el 30,00% de los ingresos de 2025; se proyecta que las enfermedades raras crezcan a una CAGR del 11,20% hasta 2031.
- Por usuario final, las empresas farmacéuticas y de biotecnología representaron el 60,12% del gasto de 2025; se espera que los patrocinadores pequeños y medianos se expandan a una CAGR del 11,25% hasta 2031.
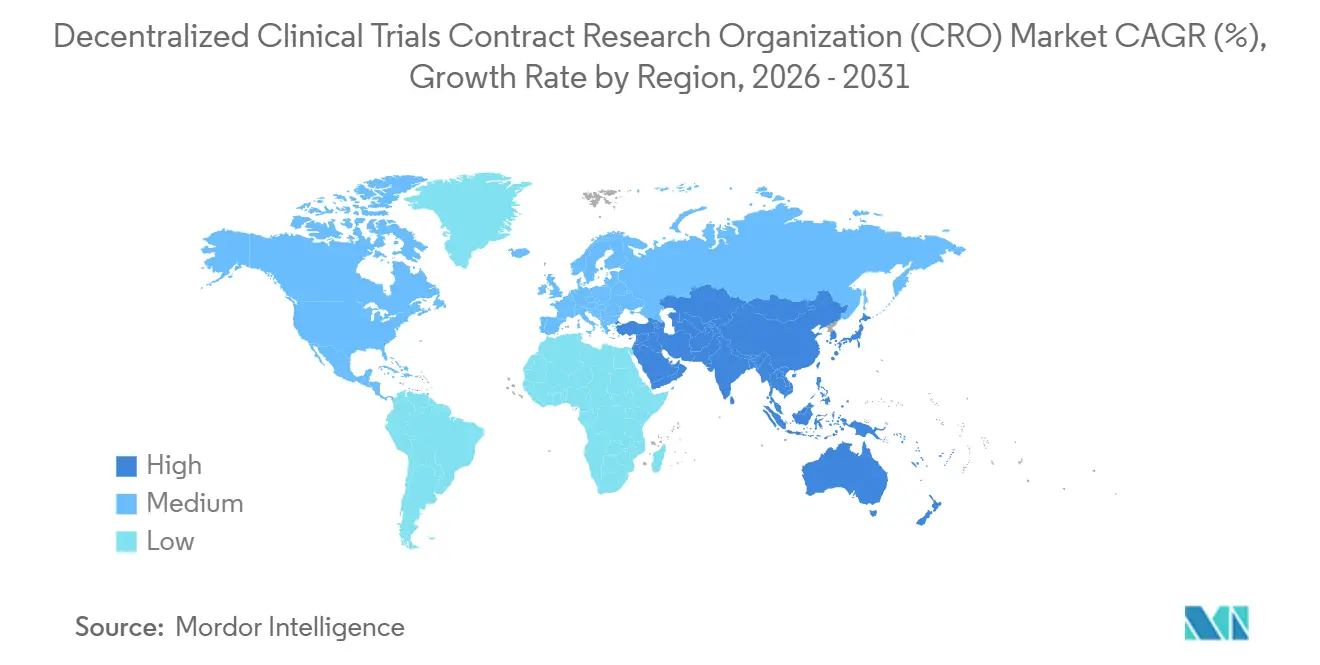
- Por geografía, América del Norte mantuvo una participación de mercado del 40,00% en 2025; Asia-Pacífico está preparada para una CAGR del 10,80% hasta 2031.
Nota: Las cifras del tamaño del mercado y los pronósticos de este informe se generan utilizando el marco de estimación patentado de Mordor Intelligence, actualizado con los datos y conocimientos más recientes disponibles a partir de enero de 2026.
Tendencias e Información del Mercado Global de Organizaciones de Investigación por Contrato (CRO) para Ensayos Clínicos Descentralizados
Análisis del Impacto de los Impulsores
| Impulsor | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Impulso de los patrocinadores hacia modelos de reclutamiento más rápidos y centrados en el paciente | +2.8% | Global, adopción temprana en América del Norte y Europa Occidental | Mediano plazo (2-4 años) |
| Adopción acelerada de plataformas eClinical en la nube | +2.3% | Global, más fuerte en los centros tecnológicos de América del Norte y Asia-Pacífico | Corto plazo (≤2 años) |
| Aprobaciones regulatorias para diseños híbridos/descentralizados | +1.9% | América del Norte, Europa y en expansión hacia Asia-Pacífico | Mediano plazo (2-4 años) |
| Inversión de las CRO en motores de reclutamiento basados en inteligencia artificial con datos del mundo real | +1.5% | América del Norte, Europa, China, India | Mediano plazo (2-4 años) |
| Redes de enfermería domiciliaria para procedimientos de última milla | +1.2% | América del Norte, Europa Occidental y Asia-Pacífico urbana | Largo plazo (≥4 años) |
| Conectividad satelital de órbita baja terrestre para transmisión de datos en zonas rurales | +0.5% | Regiones rurales a nivel mundial, pilotos en América del Norte y Australia | Largo plazo (≥4 años) |
| Fuente: Mordor Intelligence | |||
Impulso de los Patrocinadores hacia Modelos de Reclutamiento Más Rápidos y Centrados en el Paciente
La carga de las visitas al sitio es la principal causa de fracaso en el cribado y abandono a mitad del estudio, por lo que los patrocinadores están rediseñando los protocolos en torno a la conveniencia del participante. Los documentos de orientación de la FDA publicados en 2024 indican que los enfoques centrados en el paciente reducen los plazos de reclutamiento entre un 30 y un 40% en comparación con los diseños tradicionales [1]Administración de Alimentos y Medicamentos de los Estados Unidos, "Ensayos Clínicos Descentralizados para Medicamentos, Productos Biológicos y Dispositivos," fda.gov.
Las empresas farmacéuticas ahora incorporan comités asesores de pacientes durante la elaboración del protocolo, asignan entre el 20 y el 25% de los presupuestos de reclutamiento a servicios de conserjería como la flebotomía domiciliaria, y se apoyan en redes de enfermeras móviles de las CRO para entregar productos en investigación directamente a los participantes. Estas tácticas resuenan especialmente en los estudios de enfermedades crónicas donde la adherencia sustenta el poder estadístico, otorgando a las CRO con recursos establecidos de atención domiciliaria una ventaja defendible. Las biotecnológicas respaldadas por capital de riesgo que carecen de infraestructura de participación interna son las adoptantes más rápidas, lo que sustenta el pronóstico de CAGR del 11,25% para patrocinadores pequeños y medianos.
Adopción Acelerada de Plataformas eClinical en la Nube
Los entornos de nube unificados han pasado de ser opcionales a esenciales a medida que los patrocinadores exigen visibilidad de datos en tiempo real y control adaptativo del protocolo. Veeva Systems registró 676,2 millones de USD en ingresos de nube de I+D para el tercer trimestre del ejercicio fiscal 2025, un aumento interanual del 15% impulsado por migraciones desde herramientas locales hacia su suite Vault Clinical [2]Veeva Systems, "Informe de Resultados del Tercer Trimestre del Ejercicio Fiscal 2025," ir.veeva.com. Medidata, Oracle y otros proveedores ahora integran flujos de dispositivos portátiles, registros electrónicos de resultados reportados por el paciente y archivos de teleasistencia en pistas de auditoría únicas, reduciendo el trabajo de conciliación entre un 40 y un 50%. Los patrocinadores licencian cada vez más estas plataformas directamente y luego recurren a proveedores funcionales para tareas especializadas, acelerando el crecimiento de los ingresos de la plataforma a una CAGR del 12,00% y presionando a las CRO de servicio completo a formar asociaciones de marca blanca o adquirir activos tecnológicos.
Aprobaciones Regulatorias para Diseños Híbridos y Descentralizados
La orientación de la FDA de septiembre de 2024 codificó las prácticas aceptables para el consentimiento remoto, las visitas del investigador por telemedicina y la recolección de muestras en el domicilio, eliminando la ambigüedad que antes disuadía a los patrocinadores cautelosos. La Agencia Europea de Medicamentos emitió recomendaciones paralelas con salvaguardas del Reglamento General de Protección de Datos, mientras que la Administración Nacional de Productos Médicos de China redujo los tiempos de revisión medios para protocolos descentralizados a 60 días, señalando el apoyo oficial a los diseños híbridos [3]Comisión Europea, "Cumplimiento del Reglamento General de Protección de Datos," ec.europa.eu. La Organización Central de Control de Estándares de Medicamentos de India también autorizó las consultas remotas para estudios no invasivos. Estas políticas sincronizadas permiten a los patrocinadores multinacionales cumplir con diversas expectativas regulatorias a través de un protocolo armonizado, recompensando a las CRO que han desarrollado sólidas capacidades en asuntos regulatorios en todas las regiones.
Inversión de las CRO en Motores de Reclutamiento Basados en Inteligencia Artificial con Datos del Mundo Real
Los modelos de inteligencia artificial ahora extraen datos de registros médicos electrónicos, reclamaciones y registros para identificar pacientes elegibles con una precisión de hasta el 87%, muy por encima de las revisiones manuales de expedientes. IQVIA integra datos de 1.500 millones de registros de pacientes anonimizados, proporcionando a los patrocinadores velocidad de reclutamiento predictiva y control dinámico del presupuesto. Los algoritmos de riesgo de abandono de Parexel activan intervenciones de retención antes de que se produzcan las retiradas, y los clasificadores de aprendizaje automático de Labcorp reducen el tiempo de cribado en ensayos oncológicos en un 42%. Los primeros adoptantes reportan ahorros de dos dígitos en el tiempo de comercialización, reforzando la inversión en inteligencia artificial como prioridad estratégica para todas las CRO de primer nivel.
Análisis del Impacto de las Restricciones
| Restricción | (~) % de Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Horizonte Temporal del Impacto |
|---|---|---|---|
| Brechas transfronterizas en privacidad de datos y ciberseguridad | -1.8% | Global, agudo en Europa y en ensayos transfronterizos | Corto plazo (≤2 años) |
| Vías regulatorias fragmentadas en Asia-Pacífico y América Latina | -1.3% | Mercados clave de Asia-Pacífico y América Latina | Mediano plazo (2-4 años) |
| Escasez de habilidades digitales en los sitios de ensayo | -0.9% | Sitios comunitarios en todo el mundo, los mercados emergentes son los más afectados | Mediano plazo (2-4 años) |
| Inflación en el precio de los equipos de sensores portátiles | -0.7% | Global, todos los patrocinadores que utilizan dispositivos remotos | Corto plazo (≤2 años) |
| Fuente: Mordor Intelligence | |||
Brechas Transfronterizas en Privacidad de Datos y Ciberseguridad
Las violaciones de datos de salud se dispararon en el primer trimestre de 2024, con 145 incidentes que expusieron más de 90 millones de registros y retrasaron los plazos de los ensayos hasta seis meses. El Reglamento General de Protección de Datos de Europa exige que los datos permanezcan dentro de las fronteras de la Unión Europea a menos que se demuestren protecciones equivalentes, lo que obliga a los patrocinadores a operar instancias de nube separadas y añade entre un 10 y un 15% a los presupuestos de tecnología de la información. Estados Unidos opera bajo un mosaico de leyes estatales, como la Ley de Privacidad del Consumidor de California, lo que complica los flujos de trabajo de consentimiento en múltiples estados. Los patrocinadores ahora exigen pruebas de penetración, ciberseguros y cláusulas de residencia de datos dentro de los contratos con las CRO, pero el riesgo residual podría empujar a los estudios conservadores —ensayos psiquiátricos y pediátricos— de vuelta hacia diseños tradicionales basados en sitios.
Vías Regulatorias Fragmentadas en Asia-Pacífico y América Latina
A diferencia de la coordinación entre la FDA y la Agencia Europea de Medicamentos, Asia-Pacífico y América Latina siguen reglas de aprobación divergentes que extienden el inicio de los ensayos entre 6 y 12 meses. La Administración Nacional de Productos Médicos de China a menudo solicita estudios puente nacionales incluso cuando se dispone de datos globales de Fase III. La Organización Central de Control de Estándares de Medicamentos de India permite las consultas remotas, aunque los límites de telemedicina a nivel estatal añaden incertidumbre. La Agencia Nacional de Vigilancia Sanitaria de Brasil y la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica de Argentina mantienen plazos de revisión independientes y prolongados de entre 180 y 240 días. Estas fricciones favorecen a las grandes CRO con equipos maduros de asuntos regulatorios y elevan las barreras de entrada para los proveedores más pequeños que intentan expandirse fuera de sus regiones de origen.
Análisis de Segmentos
Por Tipo de Servicio: Los Proveedores de Plataformas Capturan Margen a Medida que los Patrocinadores Desagregan los Contratos
Los proveedores de servicio completo representaron el 38,23% de la participación del mercado de CRO para ensayos clínicos descentralizados en 2025, lo que refleja el sesgo histórico hacia la responsabilidad de un único proveedor. Se proyecta que el tamaño del mercado de CRO para ensayos clínicos descentralizados vinculado a la provisión de plataformas eClinical se amplíe rápidamente, ya que este nicho registra una CAGR del 12,00%, impulsado por acuerdos de licencia directa con los equipos de tecnología de la información farmacéutica. En paralelo, los especialistas funcionales en reclutamiento o análisis de datos ofrecen precios entre un 20 y un 30% más bajos que los rivales de servicio completo en paquetes de trabajo discretos, ganando terreno entre los patrocinadores sensibles a los costos. Los proveedores de plataformas, por tanto, se sitúan en el punto de inflexión de la cadena de valor, capturando tarifas de suscripción de alto margen mientras permiten a los patrocinadores seleccionar socios operativos a su conveniencia.
Los servicios de reclutamiento de pacientes ahora representan una porción significativa de los presupuestos totales de los estudios, una participación que se espera que aumente a medida que los pipelines competitivos dependan de la velocidad para llegar al primer paciente en la primera visita. Las empresas de gestión de datos incorporan inteligencia artificial para automatizar las señales de seguridad, permitiendo a los patrocinadores modificar los criterios de elegibilidad a mitad del proceso sin detener el reclutamiento. Como medida defensiva, las CRO de servicio completo han emprendido adquisiciones para asegurar tecnología propietaria, aunque los riesgos de integración amenazan los márgenes a corto plazo. Los proveedores de software independientes enfrentan su propio desafío: convencer a los patrocinadores de que un código elegante puede sustituir años de experiencia operativa cuando los ensayos se vuelven complejos.


Por Fase del Ensayo: La Vigilancia Poscomercialización Gana Terreno a Medida que los Reguladores Exigen Evidencia del Mundo Real
Los ensayos de Fase III concentraron el 55,23% de los ingresos del mercado de CRO para ensayos clínicos descentralizados en 2025, respaldados por protocolos de oncología y enfermedades raras de gran envergadura, a menudo con presupuestos superiores a los 50 millones de USD. Sin embargo, los mandatos de evidencia del mundo real están inclinando el crecimiento hacia la vigilancia de Fase IV, que avanza a una CAGR del 11,50%. Los reguladores a ambos lados del Atlántico aceptan los registros médicos electrónicos y las reclamaciones de seguros como criterios de valoración válidos, lo que permite a los patrocinadores reemplazar las costosas visitas observacionales con monitoreo remoto continuo. Este cambio eleva el tamaño del mercado de CRO para ensayos clínicos descentralizados vinculado a los estudios posaprobación y atrae el interés de los pagadores interesados en datos de seguridad longitudinales.
Los estudios en fases tempranas siguen estando parcialmente protegidos de la descentralización porque la escalada de dosis exige una vigilancia de seguridad intensiva en el sitio. Aun así, los modelos híbridos de Fase II que combinan procedimientos basados en el sitio con teleasistencia están ganando terreno a medida que los dispositivos portátiles maduran. Las CRO que dominen la coreografía operativa de sincronizar biopsias presenciales con cargas de registros electrónicos de resultados reportados por el paciente basadas en la nube tendrán una ventaja clara en las licitaciones de programas adaptativos de alto valor.
Por Área Terapéutica: Las Enfermedades Raras Aprovechan los Diseños Descentralizados para Reclutar Pacientes Dispersos
La oncología mantuvo una participación de ingresos del 30,1% en 2025 tras demostrarse que los protocolos de telemedicina para el apoyo en quimioterapia son viables a escala. El monitoreo continuo basado en dispositivos de los efectos secundarios mejora la densidad de datos y amplía el acceso para pacientes rurales y de edad avanzada, consolidando el dominio de la oncología. Sin embargo, el tamaño del mercado de CRO para ensayos clínicos descentralizados vinculado a las enfermedades raras está creciendo más rápido, con una CAGR del 11,20%, a medida que los patrocinadores de medicamentos huérfanos persiguen poblaciones geográficamente dispersas que raramente viven cerca de centros académicos. Los diagnósticos portátiles y las enfermeras de visita domiciliaria hacen factible alcanzar los objetivos de reclutamiento cuando solo existen unos pocos miles de pacientes elegibles en todo el mundo.
Los estudios de cardiología dependen cada vez más de parches de electrocardiograma remotos y manguitos de presión arterial, aunque la calibración y la duración de la batería aún generan consultas de reguladores cautelosos. Los protocolos del sistema nervioso central se retrasan en la descentralización completa porque muchas evaluaciones cognitivas requieren la observación del investigador, pero los diarios electrónicos de síntomas y los informes de cuidadores están ganando aprobación como criterios de valoración de apoyo. En todas las áreas terapéuticas, las CRO capaces de integrar telesalud, logística y gestión de dispositivos bajo un único marco de gobernanza ganarán licitaciones de manera desproporcionada.


Por Usuario Final: Las Pequeñas Biotecnológicas Impulsan la Demanda de Servicios de Ensayos Virtuales Llave en Mano
Las grandes empresas farmacéuticas y de biotecnología aportaron el 60,12% del gasto de 2025, pero sus equipos de adquisiciones están fragmentando los contratos entre múltiples proveedores para asegurar capacidades de primer nivel. Mientras tanto, el mercado de CRO para ensayos clínicos descentralizados se beneficia de una nueva cohorte de biotecnológicas respaldadas por capital de riesgo que externalizan casi el 100% de las operaciones clínicas y cuya expansión se prevé a una CAGR del 11,25%. Estas empresas ágiles buscan paquetes llave en mano que combinen estrategia regulatoria, acceso a plataformas y servicios de participación del paciente bajo una sola factura. Los fabricantes de dispositivos médicos experimentan con estudios de usabilidad en el hogar que encajan naturalmente con los diseños descentralizados, reforzando la demanda del sector de dispositivos. Los centros académicos, aunque con menor capacidad presupuestaria, se inclinan hacia herramientas eClinical de bajo costo, ampliando aún más la combinación de usuarios. Las CRO ahora calibran sus estrategias de ventas según la madurez del patrocinador: paquetes de gestión de proyectos de servicio personalizado para investigadores clínicos primerizos y portales modulares de autoservicio para las grandes farmacéuticas globales que desean control de datos. Los proveedores que no adapten su oferta corren el riesgo de ser presionados, ya sea por los nativos tecnológicos en precio o por los gigantes de servicio completo en alcance.
Análisis Geográfico
América del Norte contribuyó con el 40,00% de los ingresos del mercado de CRO para ensayos clínicos descentralizados en 2025, ya que la orientación de la FDA resolvió la incertidumbre regulatoria y la infraestructura en la nube se mantuvo sólida. Los patrocinadores estadounidenses dominan los presupuestos globales de I+D y a menudo realizan pilotos de protocolos híbridos a nivel nacional antes del despliegue global, mientras que Canadá se beneficia de la proximidad geográfica y México atrae estudios centrados en la población hispana con alivio de costos. El tamaño del mercado de CRO para ensayos clínicos descentralizados en la región crece de manera constante, aunque las primas de ciberseguros y las auditorías de la Ley de Portabilidad y Responsabilidad del Seguro Médico inflan los costos operativos.
Asia-Pacífico es el claro motor de crecimiento, con una CAGR del 10,80% proyectada hasta 2031. China acortó los plazos de revisión de protocolos descentralizados a 60 días en 2024, impulsando 1.476 registros de ensayos en 2023 y un recuento aún mayor en 2025. India aprovechó costos laborales entre un 50 y un 60% inferiores a los niveles de Estados Unidos y actualizó las normas de telemedicina para abrir sus ciudades de segundo y tercer nivel a los ensayos remotos. Japón y Australia se mantienen cautelosos, pero están pilotando marcos limitados de monitoreo remoto. Las CRO regionales como WuXi AppTec y Novotech prosperan gracias a la proximidad y las operaciones en idioma local, aunque la legislación propuesta en Estados Unidos, como la Ley de Bioseguridad, ensombrece la futura colaboración entre Estados Unidos y China.
Europa disfruta de una orientación armonizada de la Agencia Europea de Medicamentos y una adopción establecida de la telesalud, aunque el Reglamento General de Protección de Datos obliga a los patrocinadores a operar instancias de nube exclusivas para Europa, añadiendo entre un 10 y un 15% a los presupuestos de tecnología de la información. Alemania, el Reino Unido y Francia lideran la adopción, con el Instituto Federal Alemán de Medicamentos y Productos Sanitarios reembolsando las aplicaciones de salud digital. América Latina y Oriente Medio y África siguen siendo mercados incipientes. El ciclo de revisión de 180 días de la Agencia Nacional de Vigilancia Sanitaria de Brasil y la conectividad inconsistente frenan la expansión regional, mientras que los programas piloto de los estados del Golfo se centran principalmente en diabetes y oncología, lo que indica potencial pero una maduración lenta.


Panorama Competitivo
El mercado de CRO para ensayos clínicos descentralizados está moderadamente concentrado: IQVIA, Laboratory Corporation, ICON, Parexel y Syneos Health capturan la mayor parte de los ingresos globales. Para defender el margen, los gigantes de servicio completo han adquirido plataformas eClinical y especialistas en reclutamiento. Ejemplos recientes incluyen la expansión de la red de ICON en Asia-Pacífico por 150 millones de USD y el motor de emparejamiento basado en inteligencia artificial de Labcorp. El segmento de Soluciones Tecnológicas de IQVIA por 1.590 millones de USD evidencia el giro hacia los datos como servicio.
Los proveedores de software especializados como Medidata, Veeva y Oracle evitan intermediarios y se asocian directamente con los patrocinadores, capturando un porcentaje significativo del valor del contrato en suscripciones de plataforma. Los especialistas funcionales, como Premier Research en reclutamiento para enfermedades raras o Worldwide Clinical Trials con consentimiento en cadena de bloques, explotan nichos de espacio en blanco que las grandes CRO a menudo pasan por alto. La propiedad de capital privado de Parexel y la privatización de Syneos Health señalan la convicción de los inversores de que carteras más amplias y sinergias de escala pueden elevar el EBITDA.
Los competidores regionales también están activos. WuXi AppTec y Tigermed aprovechan los vientos de cola de las políticas de China, aunque los patrocinadores centrados en Estados Unidos son cautelosos ante posibles restricciones. Novotech y PSI CRO aprovechan los centros de menor costo en Asia-Pacífico, mientras que el giro de Science 37 hacia un modelo híbrido tras una sobreexpansión pone de relieve los riesgos de ejecución. En general, la diferenciación ahora depende más de los datos propietarios, el reclutamiento basado en inteligencia artificial y la amplitud de las redes de atención domiciliaria que del número de oficinas geográficas.
Líderes de la Industria de Organizaciones de Investigación por Contrato (CRO) para Ensayos Clínicos Descentralizados
IQVIA
Laboratory Corporation
ICON
Parexel
Syneos Health
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial


Desarrollos Recientes de la Industria
- Abril de 2025: Everest Group nombró a IQVIA "líder de vanguardia en inteligencia artificial generativa" para las operaciones de ciencias de la vida
- Enero de 2025: ICON plc lanzó cuatro soluciones de inteligencia artificial —iSubmit, Mapi Research Trust COA, FORWARD+ y OMR AI Navigation Assistant— para agilizar el inicio, la gestión de documentos y la previsión de recursos.
- Enero de 2025: IQVIA se asoció con una red nacional de atención domiciliaria que cubre 40 estados de Estados Unidos para apoyar procedimientos invasivos en programas oncológicos de Fase III.
Alcance del Informe Global del Mercado de Organizaciones de Investigación por Contrato (CRO) para Ensayos Clínicos Descentralizados
Según el alcance del informe, la organización de investigación por contrato para ensayos clínicos descentralizados es un socio especializado que gestiona la investigación clínica utilizando un modelo centrado en el paciente y habilitado por tecnología, en lugar de depender de sitios físicos tradicionales.
El Mercado de Organizaciones de Investigación por Contrato (CRO) para Ensayos Clínicos Descentralizados está segmentado por tipo de servicio, fase del ensayo, área terapéutica, usuarios finales y geografía. Por tipo de servicio, el mercado se categoriza en CRO de Servicio Completo, Proveedor de Servicios Funcionales, reclutamiento y retención de pacientes, gestión de datos y análisis, y provisión de plataformas eClinical. Por fase del ensayo, el mercado se divide en Fase I, Fase II, Fase III y Fase IV / Poscomercialización. Por área terapéutica, se segmenta en oncología, cardiología, trastornos del sistema nervioso central, enfermedades raras y otros. Por usuarios finales, la segmentación incluye empresas farmacéuticas y de biotecnología, empresas de dispositivos médicos, institutos académicos y de investigación, y patrocinadores pequeños y medianos. Geográficamente, el mercado está segmentado en América del Norte, Europa, la región de Asia-Pacífico, Oriente Medio y África, y América del Sur. El informe de mercado también cubre los tamaños de mercado estimados y las tendencias para 17 países en las principales regiones a nivel mundial. Para cada segmento, el tamaño del mercado y el pronóstico se proporcionan en términos de valor (USD).
| CRO de Servicio Completo |
| Proveedor de Servicios Funcionales |
| Reclutamiento y Retención de Pacientes |
| Gestión de Datos y Análisis |
| Provisión de Plataformas eClinical |
| Fase I |
| Fase II |
| Fase III |
| Fase IV / Poscomercialización |
| Oncología |
| Cardiología |
| Trastornos del Sistema Nervioso Central |
| Enfermedades Raras |
| Otros |
| Empresas Farmacéuticas y de Biotecnología |
| Empresas de Dispositivos Médicos |
| Institutos Académicos y de Investigación |
| Patrocinadores Pequeños y Medianos |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| India | |
| Japón | |
| Corea del Sur | |
| Australia | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | Consejo de Cooperación del Golfo |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tipo de Servicio | CRO de Servicio Completo | |
| Proveedor de Servicios Funcionales | ||
| Reclutamiento y Retención de Pacientes | ||
| Gestión de Datos y Análisis | ||
| Provisión de Plataformas eClinical | ||
| Por Fase del Ensayo | Fase I | |
| Fase II | ||
| Fase III | ||
| Fase IV / Poscomercialización | ||
| Por Área Terapéutica | Oncología | |
| Cardiología | ||
| Trastornos del Sistema Nervioso Central | ||
| Enfermedades Raras | ||
| Otros | ||
| Por Usuario Final | Empresas Farmacéuticas y de Biotecnología | |
| Empresas de Dispositivos Médicos | ||
| Institutos Académicos y de Investigación | ||
| Patrocinadores Pequeños y Medianos | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| India | ||
| Japón | ||
| Corea del Sur | ||
| Australia | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | Consejo de Cooperación del Golfo | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||


Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño del mercado de CRO para ensayos clínicos descentralizados en 2026?
Se espera que el tamaño del mercado de CRO para ensayos clínicos descentralizados alcance los 11,78 mil millones de USD en 2026.
¿Qué CAGR se prevé para los proveedores de CRO para ensayos descentralizados entre 2026 y 2031?
Se proyecta una CAGR del 10,20% para 2026-2031
¿Qué región se está expandiendo más rápido en servicios de ensayos descentralizados?
Se prevé que Asia-Pacífico crezca a una CAGR del 10,80% hasta 2031, superando a todas las demás regiones.
¿Qué tipo de servicio está ganando participación más rápidamente?
Se espera que la provisión de plataformas eClinical registre una CAGR del 12,00%, lo que refleja la concesión de licencias directas por parte de los patrocinadores.
¿Por qué los estudios de Fase IV son un área de crecimiento atractiva?
Los reguladores ahora exigen evidencia del mundo real, y la vigilancia descentralizada reduce los costos de monitoreo por paciente hasta en un 50%.
Última actualización de la página el: