Tamaño y Participación del Mercado de IA en el Diseño de Moléculas
Análisis del Mercado de IA en el Diseño de Moléculas por Mordor Intelligence
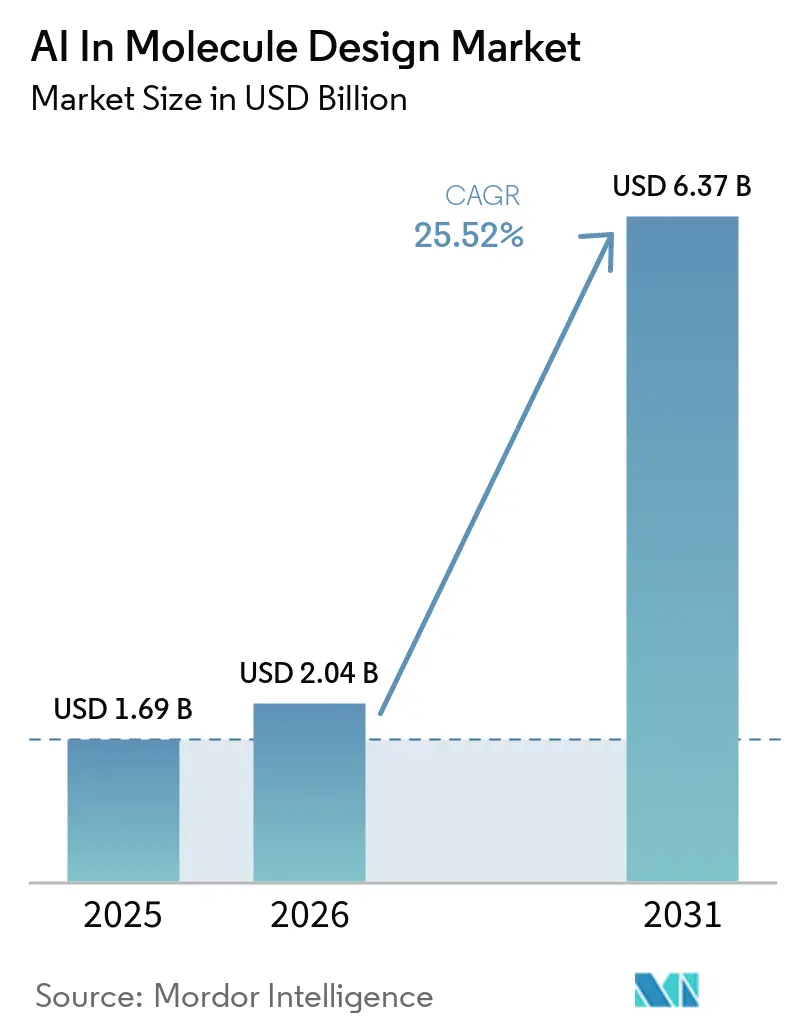
El tamaño del mercado de IA en el diseño de moléculas fue de USD 1,69 mil millones en 2025 y se prevé que alcance USD 6,37 mil millones en 2031 a una CAGR del 25,52%, lo que refleja una transición plurianual de proyectos piloto a flujos de trabajo de descubrimiento integrados en los canales farmacéuticos. Los compromisos de capital y la adopción de plataformas se están acelerando a medida que los modelos de base como AlphaFold 3 y los microservicios a escala de nube hacen que la predicción de estructuras y la química generativa sean accesibles para los equipos de I+D de gran y mediano tamaño, reduciendo las barreras para la experimentación y la iteración en el ciclo de diseño-fabricación-prueba-análisis. Los primeros adoptantes están comprimiendo los ciclos de cribado y optimización mediante la integración autónoma y semiautónoma de laboratorios que vincula la inferencia de modelos con la síntesis robótica y los análisis de alto rendimiento, lo que aumenta el rendimiento y mejora la fidelidad de los datos para ciclos sucesivos. Los avances en biología estructural están ampliando el alcance abordable para la IA, con recursos a escala de AlphaFold que permiten el diseño guiado por estructura en proteínas, ácidos nucleicos y complejos proteína-ligando, mientras que los estudios comparativos continúan aclarando dónde se necesitan flujos de trabajo híbridos de física e IA para lograr precisión en sistemas flexibles o de complejos ternarios. El enfoque competitivo está cambiando hacia activos de datos y la ejecución de laboratorio en el ciclo, a medida que las empresas formalizan canales de validación en laboratorio húmedo y conjuntos de datos propietarios que refuerzan la diferenciación de plataformas y aumentan el rendimiento del diseño de novo en modalidades de moléculas pequeñas, proteínas y ARN.
Conclusiones Clave del Informe
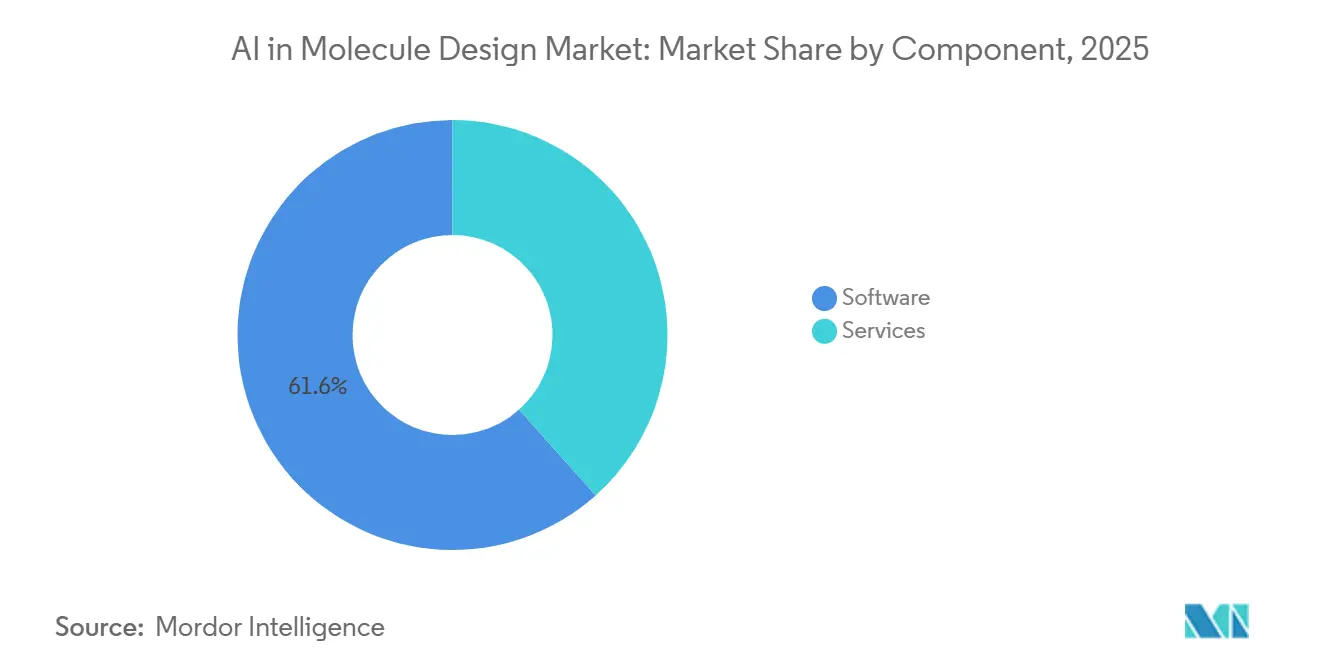
- Por componente, el software lideró con una participación del 61,56% en 2025, mientras que los servicios registraron el crecimiento proyectado más rápido con una CAGR del 26,14% hasta 2031.
- Por aplicación, el diseño de fármacos de moléculas pequeñas representó el 55,32% de la participación en 2025, y se prevé que el diseño de biológicos o proteínas se expanda a una CAGR del 27,10% hasta 2031.
- Por tipo de molécula, las moléculas pequeñas representaron el 54,34% en 2025 y las proteínas o biológicos registraron el mayor crecimiento proyectado con una CAGR del 27,32%.
- Por tecnología, los modelos generativos capturaron el 48,27% del despliegue en 2025, mientras que se proyecta que el aprendizaje profundo basado en estructura crezca a una CAGR del 27,06%.
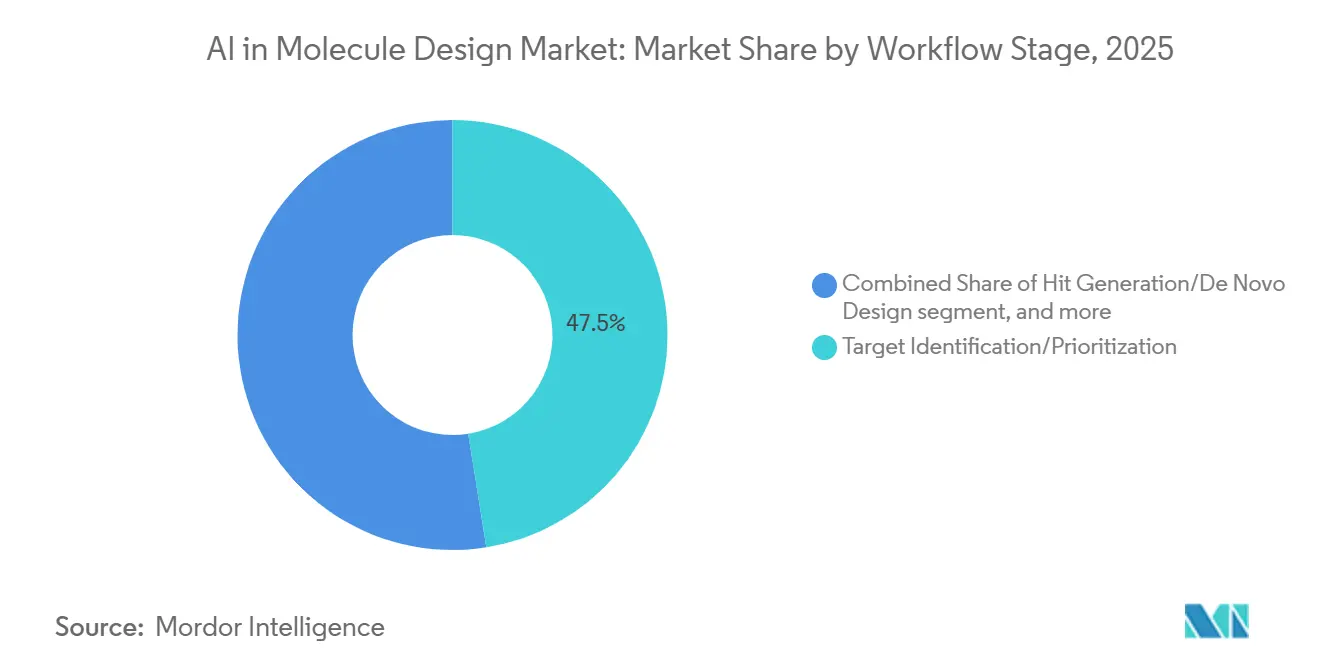
- Por etapa de flujo de trabajo, la identificación de objetivos representó el 47,48% de los despliegues en 2025 y la generación de hits o el diseño de novo avanza a una CAGR del 26,76%.
- Por usuario final, las empresas farmacéuticas y de biotecnología representaron el 65,42% en 2025, mientras que las ORC y las CDMO están proyectadas para crecer a una CAGR del 27,24%.
- Por geografía, América del Norte representó el 44,54% en 2025 y se proyecta que Asia-Pacífico se expanda a una CAGR del 26,57% hasta 2031.
Nota: Las cifras del tamaño del mercado y los pronósticos de este informe se generan utilizando el marco de estimación patentado de Mordor Intelligence, actualizado con los datos y conocimientos más recientes disponibles a partir de enero de 2026.
Tendencias e Información del Mercado Global de IA en el Diseño de Moléculas
Análisis del Impacto de los Impulsores
| Impulsor | (~) % Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Plazo de Impacto |
|---|---|---|---|
| Presión sobre la Productividad de I+D Farmacéutica e Imperativo de Reducción de Costos/Tiempo | +6.8% | Global, concentrado en centros farmacéuticos de EE. UU. y la UE | Corto plazo (≤ 2 años) |
| Modelos de Base y Cómputo a Escala de Nube que Permiten el Diseño Generativo a Escala | +5.4% | Global con ventajas de infraestructura en EE. UU. y APAC | Mediano plazo (2-4 años) |
| Datos de Estructura de la Era AlphaFold que Desbloquean el Diseño Guiado por Estructura y Codoblado | +4.2% | Global, aprovechando los recursos de AlphaFold en todo el mundo | Mediano plazo (2-4 años) |
| Flujos de Capital y Asociaciones con Grandes Farmacéuticas que Validan los Canales de Diseño con IA | +3.9% | América del Norte y la UE principalmente; expansión a APAC a través de asociaciones regionales | Corto plazo (≤ 2 años) |
| Ciclos DMTA Integrados con Automatización de Laboratorio en Bucle Cerrado que Acortan el Tiempo de Iteración | +3.1% | América del Norte y APAC como núcleo; ganancias tempranas en clústeres de la UE | Largo plazo (≥ 4 años) |
| Participación Regulatoria que Reduce el Riesgo del Uso de IA en el Descubrimiento y Desarrollo | +2.1% | Liderazgo de EE. UU. y la UE con APAC siguiendo | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Presión sobre la Productividad de I+D Farmacéutica e Imperativo de Reducción de Costos/Tiempo
Los plazos de desarrollo de fármacos y las tasas de éxito siguen bajo presión, lo que refuerza la necesidad de comprimir los ciclos de descubrimiento y mejorar la calidad de los candidatos antes de que la inversión clínica se intensifique. Las tasas de éxito clínico por debajo del 8% continúan limitando el retorno de la inversión, por lo que las funciones de descubrimiento buscan herramientas que aumenten la confianza en los objetivos y optimicen múltiples parámetros de los candidatos más temprano en el proceso. Los canales de diseño impulsados por IA apoyan pruebas de hipótesis más rápidas en cuanto a potencia, selectividad y propiedades ADMET, lo que reduce la deserción y disminuye la síntesis redundante de análogos de bajo valor cuando se combina con datos de retroalimentación de alta fidelidad. La amplia disponibilidad de modelos de base escalables y flujos de trabajo de refinamiento físico reduce los costos unitarios para el cribado y la priorización in silico, lo que lleva a un mayor rendimiento y una mejor asignación de recursos en el laboratorio húmedo. A medida que más datos estructurales y de secuencias precompetitivos ingresan a repositorios públicos, y a medida que los laboratorios de bucle cerrado recopilan mediciones propietarias de mayor calidad, el rendimiento del modelo mejora mediante un ajuste fino continuo que refleja las condiciones reales de los ensayos.
Modelos de Base y Cómputo a Escala de Nube que Permiten el Diseño Generativo a Escala
AlphaFold 3 y herramientas relacionadas amplían la capacidad predictiva en proteínas, ADN, ARN y ligandos, lo que permite la exploración computacional de modos de unión y conformaciones que históricamente dependían de métodos más lentos de biología estructural.[1]Chaim Gartenberg, "Cómo Construimos AlphaFold 3 para Predecir la Estructura e Interacción de Todas las Moléculas de la Vida," The Keyword, blog.google Los microservicios entregados en la nube, como NVIDIA BioNeMo, incorporan el acoplamiento por difusión, el plegamiento de proteínas y la generación molecular en API estandarizadas, lo que fomenta patrones de despliegue consistentes y escalables en los portafolios de descubrimiento. Las empresas reportan aceleraciones materiales y una cobertura de objetivos más amplia a medida que maduran los conjuntos de modelos preentrenados, y la optimización continua del hardware mantiene las mejoras de rendimiento sin grandes inversiones de capital en instalaciones propias. El trabajo generativo a gran escala de IBM ilustra las ganancias del entrenamiento en corpus de SMILES a escala de miles de millones, con mayor novedad y diversidad que expande las regiones químicas exploradas para el cribado virtual. Los modelos de base que aprenden reglas químicas y estructurales latentes generan candidatos que se extienden más allá de los andamiajes sobremuestreados, lo que ayuda a los equipos de descubrimiento a localizar candidatos viables de primera en clase cuando se combinan con filtros de propiedades y puntuación consciente de la síntesis. Los ecosistemas de proveedores se están consolidando en torno a servicios interoperables que integran predicción de proteínas, acoplamiento, generación y ADMET para habilitar flujos de trabajo de extremo a extremo con contratos de datos comunes y control de versiones.
Datos de Estructura de la Era AlphaFold que Desbloquean el Diseño Guiado por Estructura y Codoblado
La escala y calidad de las estructuras predichas han desplazado el diseño basado en estructura de nicho a corriente principal, ya que los investigadores pueden explorar interacciones en todos los objetivos sin esperar la determinación experimental de la estructura. AlphaFold 3 añadió capacidad para complejos proteína-ligando, lo que apoya el cribado virtual y el diseño racional de interacciones en el sitio de unión, al tiempo que guía la priorización con conformaciones predichas. Los estudios comparativos indican un rendimiento sólido para interacciones estáticas y destacan la necesidad de flujos de trabajo híbridos cuando la unión induce cambios conformacionales mayores o cuando se modelan complejos ternarios, lo que orienta a los equipos hacia el refinamiento basado en física para la clasificación de afinidad y estabilidad. Los desarrolladores de modelos están iterando rápidamente con datos sintéticos de motores físicos para mejorar la predicción de complejos, lo que reduce el error en regiones flexibles y objetivos asociados a membranas a medida que más ejemplos de entrenamiento capturan escenarios biofísicos diversos. El uso continuo de servidores centralizados para la generación de estructuras ha eliminado cuellos de botella en el descubrimiento temprano, de modo que múltiples hipótesis de objetivos pueden avanzar en paralelo con entradas estructurales consistentes. A medida que las organizaciones estandarizan estrategias de codoblado, ajuste inducido y modelado de conjuntos, los datos de estructura ahora informan tanto las etapas de generación de hits como de optimización de candidatos en moléculas pequeñas y biológicos.
Ciclos DMTA Integrados con Automatización de Laboratorio en Bucle Cerrado que Acortan el Tiempo de Iteración
Conectar los motores de diseño con la síntesis robótica y las lecturas rápidas de ensayos convierte el ciclo de diseño-fabricación-prueba-análisis en un bucle continuo, lo que reduce semanas o meses de cada iteración y amplía el número de hipótesis evaluables por unidad de tiempo. Los sistemas autónomos y semiautónomos han demostrado una optimización más rápida en métricas de potencia y eficiencia en proyectos en curso, con síntesis de alto rendimiento y análisis que proporcionan conjuntos de datos que fortalecen el reentrenamiento del modelo. En la ingeniería de proteínas, la experimentación autónoma ha generado ganancias medibles en costo y velocidad, ilustrando cómo los canales de laboratorio en el ciclo escalan cuando la inferencia del modelo dirige la experimentación en lugar de depender del procesamiento manual por lotes.[3]NVIDIA Corporation, "Ampliando el Descubrimiento de Fármacos Asistido por Computadora con Nuevos Modelos de IA," Blog de NVIDIA, blogs.nvidia.com Los gemelos digitales y los objetos de datos estandarizados reducen aún más la curación manual y permiten pruebas de hipótesis en tiempo casi real en parámetros de síntesis y proceso. Los proveedores de hardware están abordando los límites de rendimiento con celdas de trabajo modulares y escalables que se integran con la simulación para el mantenimiento predictivo y la programación, lo que aumenta el tiempo de actividad para ciclos continuos. El impacto combinado es un bucle más productivo y rico en datos que retroalimenta el rendimiento del modelo y mejora el perfil de eficiencia general del mercado de IA en el diseño de moléculas.
Análisis del Impacto de las Restricciones
| Restricción | (~) % Impacto en el Pronóstico de CAGR | Relevancia Geográfica | Plazo de Impacto |
|---|---|---|---|
| Calidad de los Datos, Sesgo y Falta de Estándares que Limitan la Generalización del Modelo | -2.8% | Global, agudo en regiones con infraestructura de datos fragmentada | Mediano plazo (2-4 años) |
| Altos Costos de Implementación y Limitaciones de Talento para Escalar Programas | -2.3% | APAC y los mercados emergentes de la UE enfrentan mayores déficits de talento; EE. UU. tiene reservas de talento en IA más sólidas | Largo plazo (≥ 4 años) |
| Brecha de Sintetizabilidad entre las Propuestas de IA y las Rutas Ejecutables | -1.7% | Global, la gravedad está inversamente correlacionada con la infraestructura de química medicinal | Mediano plazo (2-4 años) |
| Cuellos de Botella en el Suministro de Cómputo o GPU y Energía que Limitan el Entrenamiento | -1.4% | Nacional, donde el acceso a hiperescala o el suministro local de GPU es limitado | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Calidad de los Datos, Sesgo y Falta de Estándares que Limitan la Generalización del Modelo
Los datos de entrenamiento siguen siendo escasos en relación con el vasto espacio químico, y los errores o protocolos inconsistentes en los conjuntos de datos públicos introducen ruido que puede sesgar el aprendizaje del modelo y perjudicar la validez externa. Las revisiones comparativas muestran tasas de error de etiquetas no triviales en los conjuntos de datos de propiedades moleculares, lo que puede inducir correlaciones espurias y reducir la precisión en entornos de predicción prospectiva. Las condiciones heterogéneas de los ensayos complican aún más el aprendizaje, porque los modelos entrenados en fuentes agregadas pueden confundir mediciones en contextos libres de células, celulares o in vivo sin metadatos adecuados para normalizar las diferencias. El desequilibrio demográfico en la evidencia clínica plantea riesgos de generalización para las predicciones de seguridad y exposición, ya que los antecedentes genéticos subrepresentados pueden experimentar efectos adversos que los modelos entrenados en poblaciones más reducidas capturan de forma deficiente. Los acantilados de actividad y los resultados de bioensayos sensibles al contexto añaden complejidad, y la falta de reglas de notificación estandarizadas para protocolos e incertidumbre dificulta la comparación o reutilización de conjuntos de datos entre programas. Las organizaciones están abordando estas brechas generando datos experimentales propietarios a escala y enriqueciendo los metadatos para mejorar la fiabilidad del modelo, lo que apoya una mejor transferencia de dominio dentro del mercado de IA en el diseño de moléculas.
Brecha de Sintetizabilidad entre las Propuestas de IA y las Rutas Ejecutables
Los modelos generativos pueden producir moléculas con puntuaciones altas que son difíciles de sintetizar, porque muchos conjuntos de entrenamiento carecen de anotaciones de síntesis explícitas y restricciones retrosintéticas durante la generación. Los estudios que combinan filtros automatizados de calidad en química medicinal con acoplamiento y retrosíntesis muestran que solo una pequeña fracción de los candidatos generados supera todos los filtros, lo que subraya la necesidad de incorporar objetivos conscientes de la síntesis más temprano en el diseño. Incorporar planificadores de retrosíntesis en bucles de optimización ajustados mejora la tractabilidad, pero añade una carga computacional que erosiona los beneficios de velocidad de la generación de novo a gran escala. Están surgiendo nuevos marcos que aprenden de rutas retrosintéticas o ensamblaje de fragmentos para equilibrar la novedad con la viabilidad de la ruta, aunque la validación extensiva en laboratorio húmedo sigue siendo limitada en comparación con las métricas in silico. La ingeniería de recompensas y las políticas de fragmentos guiadas por síntesis pueden reducir la brecha penalizando los motivos inaccesibles, al tiempo que mantienen la diversidad del diseño para la exploración de la relación estructura-actividad. A medida que los servicios de retrosíntesis y las bibliotecas conscientes de reactivos se integran con los conjuntos de generación, los ciclos de diseño están mejorando el rendimiento desde las propuestas in silico hasta los candidatos probados en el laboratorio en el mercado de IA en el diseño de moléculas.
Análisis de Segmentos
Por Componente: El Software Domina, los Servicios se Aceleran a Medida que la Integración se Profundiza
El software representó el 61,56% del mercado de IA en el diseño de moléculas en 2025, respaldado por el acceso basado en la nube a modelos de plegamiento, acoplamiento y generativos que permiten a los equipos escalar sin grandes inversiones en instalaciones propias. Los microservicios de plataforma como BioNeMo exponen modelos para acoplamiento, predicción de estructura y generación de moléculas a través de API estándar, lo que concentra el valor en flujos de trabajo de software que pueden orquestarse en múltiples programas de descubrimiento. Las principales cadenas de herramientas en refinamiento basado en física continúan actualizando funciones para la escala, incluidas mejoras en los cálculos de energía libre y el manejo de ensayos categóricos que se alinean con los flujos de trabajo de los equipos de descubrimiento. El resultado es una mayor penetración del software en el mercado de IA en el diseño de moléculas para pasos rutinarios como la expansión de hits y el filtrado temprano de ADMET, que ahora son accesibles para usuarios multifuncionales a través de interfaces unificadas.
Los servicios son el componente de crecimiento más rápido con una CAGR proyectada del 26,14%, impulsados por la ejecución de DMTA de extremo a extremo que vincula el diseño de secuencias o moléculas con la síntesis y caracterización internas. Los proveedores enfocados en ARN ilustran este cambio con ofertas integradas que abarcan el diseño asistido por IA, la fabricación escalable y la secuenciación profunda que validan la expresión y la función dentro de un ciclo. Los modelos liderados por servicios comprimen el tiempo y reducen la fricción de coordinación entre proveedores, mientras que la captura de datos estructurados apoya el reentrenamiento continuo del modelo para la siguiente iteración. A medida que las organizaciones de descubrimiento escalan programas y estandarizan procedimientos operativos, la capa de servicios se convierte en un socio de ejecución clave que gestiona la automatización del laboratorio, el rendimiento de los ensayos y la documentación para apoyar las necesidades de calidad y cumplimiento del mercado de IA en el diseño de moléculas.
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles con la compra del informe
Por Aplicación: El Dominio de las Moléculas Pequeñas Cede Paso al Auge del Diseño de Biológicos y Proteínas
El diseño de fármacos de moléculas pequeñas representó el 55,32% de las aplicaciones en 2025, lo que refleja las vías establecidas para el cribado virtual, el refinamiento basado en física y la optimización de candidatos que siguen siendo centrales en el descubrimiento temprano. Los motores generativos y de física se utilizan ampliamente en conjunto para equilibrar la novedad con la predicción de afinidad de unión, lo que crea un filtro eficiente para priorizar candidatos antes de la síntesis. El conjunto de herramientas para moléculas pequeñas es ahora más interoperable entre objetivos y propiedades, con formatos de datos compartidos que permiten enfoques de conjunto que intercalan acoplamiento, generación y ADMET para impulsar la clasificación temprana a escala en el mercado de IA en el diseño de moléculas. Esta densidad de herramientas mantiene a las moléculas pequeñas como una modalidad de trabajo incluso cuando nuevas clases atraen inversión y atención.
El diseño de biológicos o proteínas es la aplicación de crecimiento más rápido con una CAGR proyectada del 27,10%, respaldada por avances en predicción de estructura, plegamiento inverso y optimización de secuencias que reducen la necesidad de un cribado exhaustivo de bibliotecas. Los desarrolladores con enfoque en IA han reportado avances clínicos en programas de anticuerpos diseñados con modelos de lenguaje de gran escala conscientes de secuencia y estructura, lo que proporciona evidencia externa de que los flujos de trabajo de diseño primero pueden generar candidatos adecuados para el desarrollo. Las plataformas de diseño de secuencias de ARN y ARNm ahora integran la optimización impulsada por IA con síntesis escalable y análisis, lo que acorta el camino desde las propuestas in silico hasta los constructos de expresión validados. A medida que la validación de laboratorio en el ciclo se vuelve rutinaria, los programas de biológicos aprovechan los ciclos de diseño que mejoran la desarrollabilidad y la potencia en menos iteraciones, remodelando la combinación de aplicaciones dentro del mercado de IA en el diseño de moléculas.
Por Tipo de Molécula: Las Proteínas y los Biológicos Avanzan Rápidamente a Medida que los Modelos de Base Maduran
Las moléculas pequeñas representaron el 54,34% del mercado de IA en el diseño de moléculas en 2025, respaldadas por la disponibilidad de grandes bibliotecas virtuales y estrategias de cribado escalables que se ejecutan en infraestructura de nube estándar. Los marcos de recuperación y cribado informados por estructura han logrado aceleraciones de órdenes de magnitud, ampliando el espacio de búsqueda factible por objetivo y mejorando las tasas de hits cuando se combinan con filtros de propiedades. Esta base mantiene un alto rendimiento para los canales de química medicinal, que aún se benefician de los modelos estándar de ADMET y la familiaridad clínica.
Las proteínas y los biológicos tienen el crecimiento proyectado más rápido con una CAGR del 27,32%, impulsado por una mejor modelización de secuencia-estructura, predicción de desarrollabilidad y experimentación autónoma que aumenta el rendimiento de los diseños funcionales. Las modalidades centradas en ARN también están ganando terreno a través de plataformas de laboratorio en el ciclo que optimizan características codificantes y no codificantes para mejorar la expresión y la durabilidad, lo que amplía el espacio de diseño práctico para aplicaciones terapéuticas. El avance clínico en edición génica y terapia celular apoya la inversión continua en motores de diseño a nivel de secuencia que se integran con flujos de trabajo de validación y análisis de calidad. A medida que las cadenas de herramientas maduran, la combinación de tipos de moléculas se inclina hacia los programas más sensibles a las ganancias en el aprendizaje de estructura y secuencia, acelerando los cambios de participación dentro del mercado de IA en el diseño de moléculas.
Por Tecnología: Los Modelos Generativos Lideran, el Aprendizaje Profundo Basado en Estructura Gana Impulso
Los modelos generativos representaron el 48,27% del despliegue tecnológico en 2025, lo que refleja su utilidad para proponer candidatos diversos y conscientes de propiedades para el filtrado y la optimización posteriores. Los generadores basados en difusión y transformadores están desplazando a los métodos heredados para el diseño de novo debido a la estabilidad del entrenamiento y la calidad de las muestras, mientras que la integración con ADMET y el acoplamiento aumenta la confianza en las decisiones para las selecciones de síntesis. Las actualizaciones de los modelos de base continúan ampliando la cobertura de objetivos y el alcance de las modalidades, lo que permite una aplicación más amplia en moléculas pequeñas y terapéuticos basados en proximidad en el mercado de IA en el diseño de moléculas.
El aprendizaje profundo basado en estructura es la tecnología de crecimiento más rápido con una CAGR proyectada del 27,06%, anclada por mejoras en la predicción de complejos y el modelado conformacional que apoyan el diseño guiado por estructura. Los constructores de modelos están combinando datos sintéticos generados por física con representaciones aprendidas para cerrar las brechas de precisión en sistemas flexibles, lo que aumenta la utilidad de las estructuras predichas para el diseño y la priorización. Las cadenas de herramientas que integran la retrosíntesis y la viabilidad de rutas en las funciones de puntuación refinan aún más el conjunto de candidatos, mejorando la transición desde el diseño in silico al laboratorio. Este conjunto complementa los enfoques generativos y apoya flujos de trabajo de extremo a extremo que conectan objetivos, estructuras, generación y conciencia de síntesis en el mercado de IA en el diseño de moléculas.
Por Etapa de Flujo de Trabajo: La Identificación de Objetivos Domina, la Generación de Hits se Acelera
La identificación o priorización de objetivos representó el 47,48% de los despliegues en 2025, ya que seleccionar objetivos de alta confianza es el punto de decisión más apalancado para el descubrimiento y desarrollo posteriores. La integración de datos multimodales y el modelado predictivo elevan la solidez de las hipótesis de objetivos y permiten a los equipos alinear el esfuerzo con la biología más prometedora, lo que reduce la deserción en etapas tardías. Los recursos de estructura y secuencia ahora permiten una clasificación más rápida de las clases de objetivos y la viabilidad del sitio de unión, lo que crea un camino más claro para la generación de hits posterior en el mercado de IA en el diseño de moléculas.
La generación de hits o el diseño de novo es el paso de crecimiento más rápido con una CAGR proyectada del 26,76%, impulsado por conjuntos de modelos que proponen grandes lotes de candidatos químicamente diversos condicionados en propiedades de potencia y desarrollabilidad. Cuando se integra con laboratorios de bucle cerrado, esta etapa produce retroalimentación inmediata que perfecciona las generaciones posteriores y reduce el tiempo hasta los hits calificados. La optimización de candidatos se beneficia entonces del refinamiento basado en física y las predicciones calibradas de energía libre, que apoyan síntesis más pequeñas y específicas para la expansión de la relación estructura-actividad. Los flujos de trabajo de extremo a extremo agrupan cada vez más microservicios de ADMET, retrosíntesis y predicción de estructura para que los equipos de descubrimiento puedan operar ciclos continuos dentro de canales de datos estandarizados en el mercado de IA en el diseño de moléculas.
Nota: Las participaciones de segmento de todos los segmentos individuales están disponibles con la compra del informe
Por Usuario Final: Farmacéutica o Biotecnología Lidera, las ORC o CDMO Surgen a Medida que la Externalización se Acelera
Las empresas farmacéuticas y de biotecnología representaron el 65,42% en 2025, lo que refleja la concentración de presupuestos de descubrimiento y la necesidad estratégica de reponer los canales a medida que evoluciona la combinación de modalidades. Los equipos de descubrimiento dentro de las grandes organizaciones despliegan conjuntos de IA estandarizados en objetivos y modalidades para alinear el diseño computacional con la capacidad del laboratorio, lo que mejora el rendimiento y la calidad de los datos para los ciclos iterativos en el mercado de IA en el diseño de moléculas.
Las ORC y las CDMO son los usuarios finales de crecimiento más rápido con una CAGR proyectada del 27,24%, ya que las empresas patrocinadores trasladan el trabajo a socios capaces de ejecutar química y biología aumentadas por IA con automatización de laboratorio integrada. Los proveedores que agrupan motores de diseño con síntesis y análisis reducen la carga del patrocinador y aceleran los ciclos, mientras que la documentación estandarizada apoya la transferencia tecnológica y la preparación regulatoria. El efecto es un ecosistema de servicios más escalable que amplía el acceso a flujos de trabajo avanzados dentro del mercado de IA en el diseño de moléculas.
Análisis Geográfico
América del Norte representó el 44,54% del mercado de IA en el diseño de moléculas en 2025, respaldada por una masa crítica de presupuestos de descubrimiento, talento computacional e infraestructura de laboratorio que integra la IA con la experimentación automatizada. La región cuenta con un despliegue activo de microservicios de modelos de base y cadenas de herramientas de física, lo que permite un cribado y priorización más rápidos en objetivos y modalidades. Los ecosistemas de proveedores que abarcan plataformas de nube aceleradas por GPU y centros de modelos han aumentado el acceso a herramientas de alto rendimiento, lo que apoya la experimentación a gran escala en áreas terapéuticas en el mercado de IA en el diseño de moléculas.
Asia-Pacífico es la región de crecimiento más rápido con una CAGR proyectada del 26,57% hasta 2031, anclada por iniciativas respaldadas por el gobierno y plataformas académico-industriales que amplían el acceso al análisis de objetivos, el diseño generativo y las herramientas de evaluación. China lanzó una plataforma de IA de proceso completo que ofrece acceso gratuito para el análisis de objetivos, la generación de moléculas y la optimización de ADMET, lo que reduce las barreras para los laboratorios académicos y las empresas emergentes. Los programas vinculados a Tsinghua reportaron aceleraciones de un millón de veces en el cribado virtual y abrieron grandes bases de datos de proteína-ligando para la comunidad, lo que amplía el espacio de búsqueda para los proyectos de descubrimiento en el mercado de IA en el diseño de moléculas. El Ministerio de Economía, Comercio e Industria y la Agencia de Nuevas Energías y Tecnología Industrial de Japón apoyaron el trabajo en modelos de base a gran escala para el diseño de fármacos, lo que señala el compromiso del sector público con el escalado del descubrimiento con enfoque en IA.
Europa se beneficia de la financiación pública coordinada y de una densa red de centros farmacéuticos, biotecnológicos y académicos que conectan el modelado de descubrimiento con la infraestructura traslacional. Los programas nacionales han introducido financiación específica para acelerar el descubrimiento de fármacos habilitado por IA, con una sólida infraestructura en países que albergan importantes instituciones farmacéuticas y de investigación. En toda la región, el mercado de IA en el diseño de moléculas se expande a medida que las partes interesadas conectan modelos de base, automatización de laboratorio y análisis de procesos para apoyar el descubrimiento y el desarrollo temprano en múltiples modalidades.
Panorama Competitivo
La competencia en el mercado de IA en el diseño de moléculas está moderadamente fragmentada entre conjuntos tecnológicos, modalidades terapéuticas y modelos de comercialización, con la diferenciación desplazándose hacia los activos de datos y la ejecución de laboratorio en el ciclo que mejoran el rendimiento del diseño con el tiempo. La consolidación está remodelando las capacidades mediante la combinación de química generativa, fenómica e identificación de objetivos bajo un mismo techo, lo que apoya el descubrimiento escalado en todos los portafolios. Los activos de datos son fundamentales a medida que las empresas invierten en conjuntos de datos propietarios de alta calidad y automatización que crean bucles de retroalimentación para mejorar el rendimiento del modelo en el mercado de IA en el diseño de moléculas.
Los líderes del ecosistema también están estandarizando el acceso a los modelos a través de microservicios en la nube, lo que crea efectos de red a medida que más usuarios contribuyen al ajuste y la evaluación. Las plataformas de ingeniería de ARN y proteínas están emergiendo como nichos de alto crecimiento, reforzadas por el interés de los inversores y las capacidades de laboratorio en el ciclo que conectan el diseño con la síntesis y el análisis en un entorno. Las empresas también están enfatizando la explicabilidad y la procedencia para apoyar los requisitos de los patrocinadores en materia de gobernanza interna y documentación lista para la regulación, lo que alinea la diferenciación tecnológica con las necesidades operativas en el descubrimiento y el desarrollo.
Algunos movimientos estratégicos selectos ilustran el arco competitivo del mercado de IA en el diseño de moléculas a medida que escala. Una combinación biotecnológica de alto perfil integró grandes conjuntos de datos propietarios y motores de descubrimiento multimodalidad bajo una estructura corporativa única para acelerar el descubrimiento industrializado. Los centros de acceso a modelos de base aseguraron una adopción amplia en más de cien empresas, confirmando el papel central de las API estandarizadas y la nube de GPU para la generación molecular, el acoplamiento y el plegamiento a escala. Los estudios comparativos de experimentación autónoma en ingeniería de proteínas demostraron ganancias de costo y velocidad a partir de flujos de trabajo de laboratorio dirigidos por IA, validando la integración de la inferencia de modelos con sistemas de laboratorio automatizados en entornos comerciales.
Líderes de la Industria de IA en el Diseño de Moléculas
Schrödinger
Exscientia
Insilico Medicine
Recursion
XtalPi
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Abril de 2026: Isomorphic Labs, la empresa derivada de DeepMind, está avanzando el diseño de moléculas impulsado por IA hacia una nueva fase al preparar sus primeros ensayos clínicos en humanos de candidatos a fármacos diseñados por IA. Utilizando sus sistemas de IA construidos sobre AlphaFold y modelos generativos, la empresa diseña y optimiza moléculas novedosas para enfermedades como el cáncer y los trastornos inmunológicos. Tras asegurar importantes asociaciones y financiación con grandes farmacéuticas, ahora está transitando de la generación de moléculas in silico a la validación en el mundo real, con ensayos en humanos previstos para alrededor de 2026. Esto marca un hito clave en el que las moléculas diseñadas por IA pasan del descubrimiento computacional a las pruebas clínicas en humanos.
- Marzo de 2026: Roche lanzó una "fábrica" de IA para el desarrollo de fármacos en colaboración con NVIDIA para escalar el diseño de moléculas impulsado por IA y el descubrimiento de fármacos. El sistema utiliza infraestructura de GPU a gran escala para ejecutar modelos de IA generativa que ayudan a diseñar nuevas moléculas de fármacos, identificar objetivos y simular el comportamiento biológico de manera más eficiente. Integra estas capacidades en el canal de I+D y fabricación de Roche, lo que permite un enfoque más automatizado y basado en datos para el desarrollo de medicamentos.
- Marzo de 2026: Eli Lilly celebró un acuerdo de USD 2,75 mil millones con Insilico Medicine para avanzar en el diseño de moléculas impulsado por IA para el descubrimiento de fármacos. La colaboración se centró en el uso de IA generativa para crear y optimizar nuevas moléculas de fármacos, que Lilly desarrolla en posibles terapias, particularmente en áreas como la oncología y las enfermedades metabólicas. Este acuerdo destaca la creciente confianza de la industria farmacéutica en las moléculas diseñadas por IA como candidatos a fármacos preclínicos viables.
Alcance del Informe Global del Mercado de IA en el Diseño de Moléculas
Según el alcance del informe, la IA en el diseño de moléculas se refiere al uso de modelos de aprendizaje automático y generativos para predecir, crear y optimizar estructuras moleculares aprendiendo de grandes conjuntos de datos químicos, lo que permite una exploración más rápida del espacio químico y acelera el ciclo de diseño-fabricación-prueba. Apoya tareas como la predicción de propiedades, la generación de moléculas de novo y la optimización automatizada, ayudando a los científicos a diseñar nuevos candidatos a fármacos y materiales de manera más eficiente.
El mercado de IA en el diseño de moléculas está segmentado en componente, aplicación, tipo de molécula, tecnología, etapa de flujo de trabajo, usuario final y geografía. Por componente, el mercado está segmentado en software y servicios. Por aplicación, el mercado está segmentado en diseño de fármacos de moléculas pequeñas, diseño de biológicos/proteínas, diseño de materiales y productos químicos especiales, y diseño de agroquímicos. Por tipo de molécula, el mercado está segmentado en moléculas pequeñas, péptidos, proteínas/biológicos, ARN/oligonucleótidos y moléculas de materiales/polímeros. Por tecnología, el mercado está segmentado en modelos generativos, aprendizaje profundo basado en estructura, predicción de propiedades/ADMET con aprendizaje automático, y planificación de síntesis e IA de retrosíntesis. Por etapa de flujo de trabajo, el mercado está segmentado en identificación/priorización de objetivos, generación de hits/diseño de novo, de hit a candidato, optimización de candidatos y otros. Por usuario final, el mercado está segmentado en empresas farmacéuticas y de biotecnología, ORC y CDMO, fabricantes de productos químicos y materiales, y otros. Por geografía, el mercado está segmentado en América del Norte, Europa, Asia-Pacífico, Oriente Medio y África, y América del Sur. El informe también cubre los tamaños de mercado estimados y las tendencias para 17 países en las principales regiones del mundo. El informe ofrece valores (USD) para todos los segmentos anteriores.
| Software |
| Servicios |
| Diseño de Fármacos de Moléculas Pequeñas |
| Diseño de Biológicos/Proteínas |
| Diseño de Materiales y Productos Químicos Especiales |
| Diseño de Agroquímicos |
| Moléculas Pequeñas |
| Péptidos |
| Proteínas/Biológicos |
| ARN/Oligonucleótidos |
| Moléculas de Materiales/Polímeros |
| Modelos Generativos |
| Aprendizaje Profundo Basado en Estructura |
| Predicción de Propiedades/ADMET con Aprendizaje Automático |
| Planificación de Síntesis e IA de Retrosíntesis |
| Identificación/Priorización de Objetivos |
| Generación de Hits/Diseño de Novo |
| De Hit a Candidato |
| Optimización de Candidatos |
| Otros |
| Empresas Farmacéuticas y de Biotecnología |
| ORC y CDMO |
| Fabricantes de Productos Químicos y Materiales |
| Otros |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | CCG |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Componente | Software | |
| Servicios | ||
| Por Aplicación | Diseño de Fármacos de Moléculas Pequeñas | |
| Diseño de Biológicos/Proteínas | ||
| Diseño de Materiales y Productos Químicos Especiales | ||
| Diseño de Agroquímicos | ||
| Por Tipo de Molécula | Moléculas Pequeñas | |
| Péptidos | ||
| Proteínas/Biológicos | ||
| ARN/Oligonucleótidos | ||
| Moléculas de Materiales/Polímeros | ||
| Por Tecnología | Modelos Generativos | |
| Aprendizaje Profundo Basado en Estructura | ||
| Predicción de Propiedades/ADMET con Aprendizaje Automático | ||
| Planificación de Síntesis e IA de Retrosíntesis | ||
| Por Etapa de Flujo de Trabajo | Identificación/Priorización de Objetivos | |
| Generación de Hits/Diseño de Novo | ||
| De Hit a Candidato | ||
| Optimización de Candidatos | ||
| Otros | ||
| Por Usuario Final | Empresas Farmacéuticas y de Biotecnología | |
| ORC y CDMO | ||
| Fabricantes de Productos Químicos y Materiales | ||
| Otros | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | CCG | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño actual y las perspectivas de crecimiento del mercado de IA en el diseño de moléculas?
El tamaño del mercado de IA en el diseño de moléculas fue de USD 1,69 mil millones en 2025 y se proyecta que alcance USD 6,37 mil millones en 2031 a una CAGR del 25,52%, lo que señala un impulso plurianual en los flujos de trabajo de descubrimiento.
¿Qué regiones impulsarán la expansión más rápida hasta 2031?
Asia-Pacífico es la región de crecimiento más rápido con una CAGR proyectada del 26,57%, respaldada por plataformas respaldadas por el gobierno y programas académico-industriales que amplían el acceso a herramientas de diseño habilitadas por IA.
¿Qué aplicaciones y tipos de moléculas están proyectados para crecer más?
El diseño de biológicos o proteínas es la aplicación de crecimiento más rápido con una CAGR del 27,10%, mientras que las proteínas o biológicos lideran el crecimiento por tipo de molécula con el 27,32%, con modelos de laboratorio en el ciclo y conscientes de estructura que mejoran el rendimiento.
¿Qué tecnologías se utilizan más ampliamente hoy en el diseño habilitado por IA?
Los modelos generativos lideran con un despliegue del 48,27%, y el aprendizaje profundo basado en estructura es el de crecimiento más rápido con una CAGR del 27,06%, apoyado por avances en la predicción de complejos y microservicios entregados en la nube.
Última actualización de la página el: