Marktgröße und Marktanteil für mRNA-Synthesedienstleistungen
Marktanalyse für mRNA-Synthesedienstleistungen von Mordor Intelligence
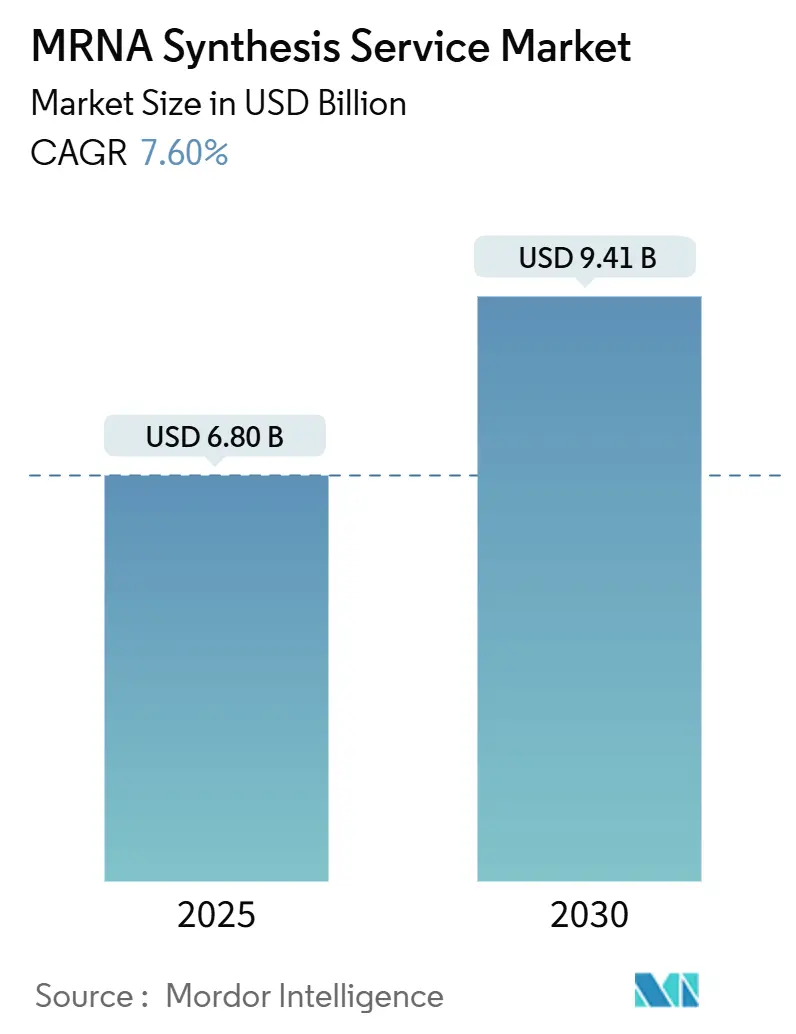
Die Marktgröße für mRNA-Synthesedienstleistungen wird im Jahr 2025 auf 6,80 Milliarden USD geschätzt und soll bis 2030 bei einer CAGR von 7,60 % während des Prognosezeitraums (2025–2030) einen Wert von 9,41 Milliarden USD erreichen.
Die wachsenden Impfstoff-Pipelines nach der Pandemie, die rasche Diversifizierung in Onkologie- und Gentherapien sowie anhaltende Venture- und staatliche Finanzierungen halten die Nachfrage nach ausgelagerten mRNA-Synthesedienstleistungen auf einem hohen Niveau. Große Pharmaunternehmen verlagern ihr Kapital zunehmend auf Forschung und Entwicklung und verlassen sich dabei auf spezialisierte Auftragsherstellungsorganisationen (CDMOs) für die Prozessentwicklung und cGMP-Produktion – ein Wandel, der durch steigende Validierungsanforderungen und die hohen Kosten interner Anlagen verstärkt wird. Technologische Fortschritte – insbesondere hocheffiziente In-vitro-Transkription (IVT), co-transkriptionelle Capping-Verfahren und KI-gestützte Sequenzgestaltung – steigern die Ausbeuten, verkürzen Entwicklungszyklen und senken die Kosten pro Dosis. Neue modulare „Drucker”-Systeme unterstützen die dezentrale Produktion, verbessern die Resilienz der Lieferkette und ermöglichen schnelle regionale Reaktionen auf Nachfrageschübe. Der Wettbewerb verschärft sich, da etablierte Biologika-Hersteller Anlagen für mRNA erwerben oder umrüsten. Gleichzeitig differenzieren sich spezialisierte CDMOs durch durch geistiges Eigentum geschützte Plattformen wie CleanCap, fortschrittliche Analytik und integrierte Formulierungsangebote für Lipid-Nanopartikel (LNP).
Wesentliche Erkenntnisse des Berichts
- Nach Dienstleistungsart führte die GMP-konforme Herstellung mit einem Umsatzanteil von 46,4 % im Jahr 2024; die individuelle Synthese wird bis 2030 voraussichtlich mit einer CAGR von 9,1 % wachsen.
- Nach Maßstab entfiel auf die klinische GMP im Jahr 2024 ein Anteil von 38,9 % am Markt für mRNA-Synthesedienstleistungen; die standortgebundene modulare Produktion wird voraussichtlich mit der höchsten Rate von 8,4 % CAGR bis 2030 wachsen.
- Nach Anwendung hielten Impfstoffe im Jahr 2024 einen Marktanteil von 67,1 % am Markt für mRNA-Synthesedienstleistungen; Gen-Editierung/CRISPR wird bis 2030 voraussichtlich mit einer CAGR von 10,7 % wachsen.
- Nach Endnutzer hielten Pharmaunternehmen im Jahr 2024 einen Anteil von 41,7 % am Markt für mRNA-Synthesedienstleistungen, während Biotechnologieunternehmen mit einer CAGR von 7,3 % wachsen.
- Nach Geografie erzielte Nordamerika im Jahr 2024 einen Umsatzanteil von 42,4 %, und der Asien-Pazifik-Raum wächst mit einer CAGR von 6,4 %.
Globale Trends und Erkenntnisse zum Markt für mRNA-Synthesedienstleistungen
Analyse der Treiberwirkung
| Treiber | (~) % Auswirkung auf die CAGR-Prognose | Geografische Relevanz | Zeithorizont der Auswirkung |
|---|---|---|---|
| Ausweitung der Impfstoff-Pipeline nach COVID-19 | +2.10% | Global; frühe Gewinne in Nordamerika und Europa | Mittelfristig (2–4 Jahre) |
| Auslagerungsboom zu mRNA-fokussierten CDMOs | +1.80% | Global | Kurzfristig (≤ 2 Jahre) |
| Hocheffiziente IVT- und Capping-Innovationen | +1.40% | Nordamerika und EU; Ausstrahlungseffekte auf den Asien-Pazifik-Raum | Mittelfristig (2–4 Jahre) |
| Zufluss von Venture- und staatlichen Fördermitteln | +1.20% | USA, China, EU | Kurzfristig (≤ 2 Jahre) |
| Modulare „mRNA-Drucker”-Mikrofabriken | +0.90% | Asien-Pazifik-Raum als Kern; Ausweitung auf den Nahen Osten und Afrika | Langfristig (≥ 4 Jahre) |
| KI-gestützte Sequenzoptimierung und Kostensenkungen | +0.20% | Nordamerika und EU | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Ausweitung der Impfstoff-Pipeline nach COVID-19 treibt therapeutische Diversifizierung voran
Der bewiesene Erfolg der nukleosidmodifizierten COVID-19-Impfstoffe lenkt den Fokus auf Onkologie-, RSV- und Seltene-Krankheiten-Programme, die nun auf die Zulassung zusteuern. Moderna verfolgt bis zu 10 Kandidaten in der Spätphase, darunter personalisierte Krebsimpfstoffe, RSV-Prophylaktika und eine kombinierte Influenza/COVID-19-Impfung. Positive Daten zu mRNA-4157 in Kombination mit Pembrolizumab zeigten eine 44-prozentige Reduktion des Melanom-Rückfalls und validierten die Plattform für die Immuno-Onkologie.[1]Chen-Yi Chang, „Spiralmikrofluidik-Chips ermöglichen die Hochdurchsatz-Herstellung von Lipid-Nanopartikeln für die mRNA-Verabreichung”, Micromachines, mdpi.com CDMOs reagieren darauf mit der Einrichtung dedizierter Bereiche für hochwirksame und personalisierte Chargen; TriLink BioTechnologies hat kürzlich eine großmaßstäbliche cGMP-Linie für die Wirkstoffproduktion in der Spätphase eröffnet.
Auslagerungsboom verändert die Wettbewerbsdynamik bei CDMOs
Große Pharmaunternehmen bauen interne Kapazitäten ab, da biologische Komplexität und Kapitalintensität steigen. Pfizers mehrjähriges Programm zielt auf Einsparungen von 1,5 Milliarden USD in der Herstellung ab und verlagert Mittel auf klinische Vermögenswerte, während externe Experten als Partner eingebunden werden. Jüngste Transaktionen – Agilents Übernahme von BIOVECTRA für 925 Millionen USD und Maravai LifeSciences' Erwerb der Nukleinsäureeinheit von Officinae Bio – verdeutlichen die Konsolidierung rund um durchgängige mRNA-Fähigkeiten.
Hocheffiziente IVT- und Capping-Innovationen reduzieren Herstellungsengpässe
CleanCap-Reagenzien erzielen eine Capping-Effizienz von mehr als 95 % und können die Kosten pro Gramm mRNA um 20–40 % senken. Die neue M6-Variante steigert die Proteinexpression um weitere 30 %. Prozessverbesserungen, einschließlich optimierter T7-Promotoren, treiben die Ausbeuten auf 14 g/L und senken die dsRNA-Kontamination um 30 %.[2]Xiaoyu Huang, „Durch künstliche Intelligenz gestütztes rationales Design ionisierbarer Lipide für die mRNA-Verabreichung”, Nature Communications, nature.com Die CDMO-Lizenzierung dieser Technologien bietet Kunden schnellere Durchlaufzeiten und höhere Wirksamkeiten und stärkt langfristige Serviceverträge.
Zufluss von Venture- und staatlichen Fördermitteln beschleunigt den Kapazitätsausbau
Staatliche Budgets für die Pandemievorsorge konvergieren mit Venture-Fonds, die auf mRNA-Plattformen abzielen. Die US-Regierung hat 75 Millionen USD zugesagt, um die Lipidanlage von Croda auszubauen und die lokale Versorgung mit kritischen Hilfsstoffen zu stärken. Unterdessen hat GenScript 224 Millionen USD aufgenommen, um CDMO-Linien in China zu skalieren. Australien hat 200 Millionen USD bereitgestellt, um Aurora Biosynthetics zu gründen und regionale GMP-Optionen zu schaffen.
Analyse der Hemmnisse
| Hemmnis | (~) % Auswirkung auf die CAGR-Prognose | Geografische Relevanz | Zeithorizont der Auswirkung |
|---|---|---|---|
| GMP-Konformität und Validierungsengpässe | –1.3% | EU und USA | Mittelfristig (2–4 Jahre) |
| Lieferkettenengpass bei hochreinen Reagenzien | –0.8% | Global | Kurzfristig (≤ 2 Jahre) |
| Gegenwind durch die Wahrnehmung der Impfstoffsicherheit | –0.6% | Global; regional unterschiedlich | Mittelfristig (2–4 Jahre) |
| Umweltbelastung durch enzymatische Reagenzien | –0.4% | EU und Nordamerika; aufkommend im Asien-Pazifik-Raum | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
GMP-Konformität und Validierungsengpässe hemmen die Skalierung
Überarbeitete EMA-Leitlinien für ATMP und neue USP-Kapitel zu mRNA-Impfstoffen verschärfen die Freigabekriterien und schreiben fortschrittliche Analysemethoden wie Sequenzierung der nächsten Generation und orthogonale Reinheitsassays vor. Das Rahmenwerk der FDA für fortschrittliche Herstellungstechnologien erfordert nun eine umfangreiche Dokumentation für neuartige Prozesse.[3]US-amerikanische Behörde für Lebens- und Arzneimittel, „Bezeichnungsprogramm für fortschrittliche Herstellungstechnologien; Leitfaden für die Industrie”, federalregister.gov CDMOs investieren in automatisierte Qualitätssysteme und digitale Chargenprotokolle; Moderna senkte die Forschungs- und Entwicklungsausgaben durch Prozessvalidierungseffizienzen um 1,1 Milliarden USD.
Lieferkettenengpass bei hochreinen Reagenzien erzeugt Kostendruck
Globale Engpässe bei T7-Polymerase, Capping-Enzymen und Nukleotiden haben die Vorlaufzeiten verlängert und die Kosten erhöht. Hersteller reagieren mit Dual-Sourcing, der Bevorratung kritischer Einsatzstoffe und der Erprobung enzymatischer RNA-Synthese, die chemische Schritte durch wasserbasierte Reaktionen ersetzt, den ökologischen Fußabdruck reduziert und die Abhängigkeit von knappen Reagenzien verringert.
Segmentanalyse
Nach Dienstleistungsart: Individuelle Synthese treibt Plattforminnovation voran
Die GMP-konforme Herstellung behielt mit 46,4 % im Jahr 2024 den größten Anteil, was ihre etablierte Infrastruktur und die Präferenz der Regulierungsbehörden für validierte Plattformen widerspiegelt. Gleichzeitig wächst die individuelle Synthese mit einer CAGR von 9,1 %, angetrieben durch die Nachfrage nach individualisierten Krebsimpfstoffen und Therapien für seltene Krankheiten. CDMOs integrieren KI-Werkzeuge, um Sequenzkonstrukte schnell zu iterieren und Kunden zu ermöglichen, innerhalb von weniger als sechs Monaten vom Design bis zur IND-Einreichung voranzuschreiten. Design-Optimierungs- und Analysepakete sind mittlerweile Standard, wie die Zusammenarbeit zwischen AmplifyBio und RNAV8 zeigt, die Sequenzdesign, IVT, LNP-Formulierung und Freigabetests unter einem Dach bündelt. Die Marktgröße für mRNA-Synthesedienstleistungen bei maßgeschneiderten Projekten wird voraussichtlich wachsen, da leistungsbasierte Vergütungsmodelle verbreiteter werden. Vorteile beim geistigen Eigentum – wie TriLinks CleanCap und Aldeverons hochpräzise Plasmide – schaffen dauerhafte Wettbewerbsvorteile und ermöglichen Premiumpreise.
Die Erweiterung der Dienstleistungsangebote spiegelt die allgemeine Reifung des Marktes für mRNA-Synthesedienstleistungen wider. Rohstoffliefervereinbarungen sichern die Verfügbarkeit von Enzymen und Nukleotiden, während hybride Gebührenstrukturen (Kapazitätsreservierung plus Kosten pro Charge) CDMOs helfen, makroökonomische Volatilität abzufedern. Da Kunden beschleunigte Zulassungswege anstreben, integrieren Anbieter Beratung zu regulatorischen Angelegenheiten und die Entwicklung von Begleitdiagnostika und verankern sich so noch stärker in den Arbeitsabläufen der Auftraggeber.
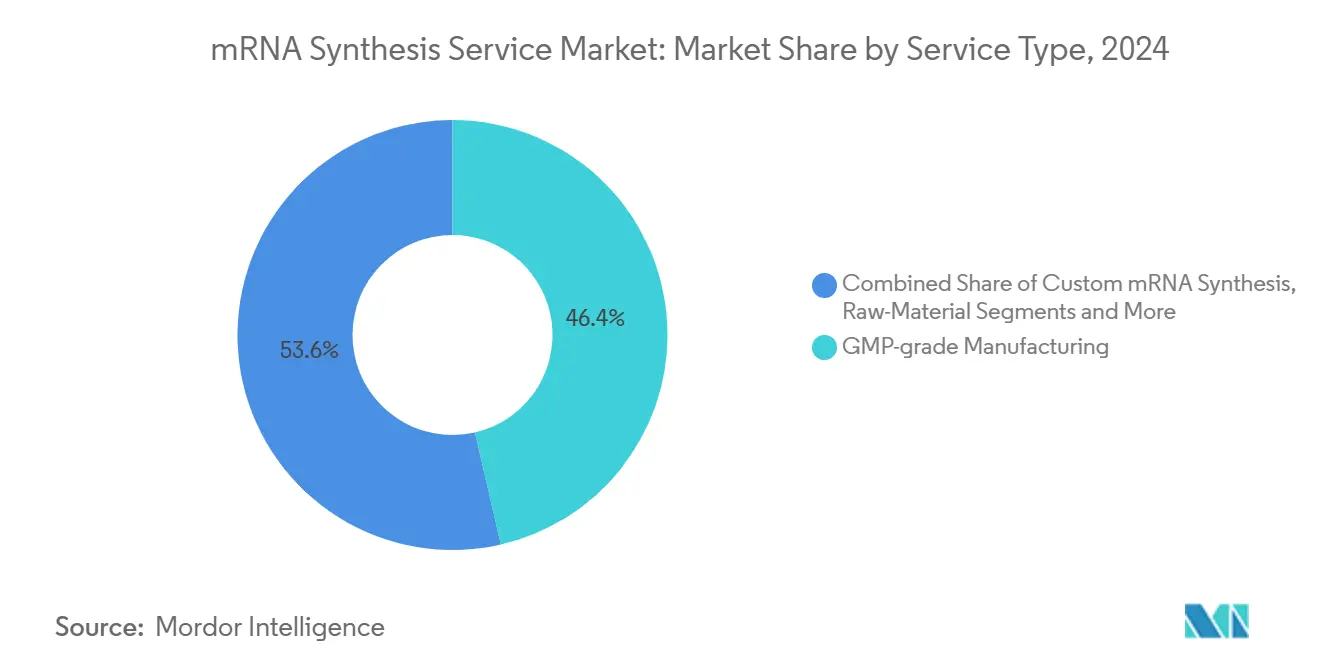
Notiz: Segmentanteile aller einzelnen Segmente sind nach dem Kauf des Berichts verfügbar
Nach Maßstab: Modulare Produktion revolutioniert Herstellungsparadigmen
Klinische GMP-Chargen machen 38,9 % des Umsatzes aus und decken Zulassungsstudien und frühe Markteinführungen ab. Der Marktanteil für mRNA-Synthesedienstleistungen bei modularen Anlagen wächst jedoch am schnellsten mit einer CAGR von 8,4 %. Containerisierte Reinräume können auf einem einzigen Lastwagen transportiert werden, erfordern minimale Bauarbeiten und können innerhalb von Tagen zwischen 50-mg-präklinischen Läufen und mehrere Kilogramm schweren kommerziellen Chargen wechseln. BioNTech schätzt, dass eine Zwei-Einheiten-BioNTainer-Anlage jährlich 50 Millionen Dosen liefern kann, bei einem um 70 % niedrigeren Investitionsaufwand (Capex) als eine herkömmliche Anlage. Für kleinere Indikationen produzieren Durchfluss-Mikroreaktoren Chargen auf Abruf und reduzieren so die Lagerkosten.
Bestehende kommerzielle Großanlagen konsolidieren sich rund um die Nutzung mehrerer Produkte. Lonzas Übernahme von Roches Vacaville-Werk fügte 330.000 L Säugetierkapazität hinzu, die nun teilweise für die mRNA-LNP-Endbearbeitung umgerüstet wurde – ein Beispiel für die Umwidmung von Anlagen zur Bewältigung von Pipeline-Unsicherheiten. Hybridmodelle – zentrale Bulk-RNA gefolgt von regionaler Abfüllung und Endbearbeitung – erhöhen die Resilienz gegenüber Lieferkettenunterbrechungen.
Nach Anwendung: Gen-Editierung entwickelt sich zur wachstumsstarken therapeutischen Grenze
Impfstoffe dominieren weiterhin mit einem Anteil von 67,1 %, doch Gen-Editierungs- und CRISPR-Therapien verzeichnen das stärkste Wachstum, begünstigt durch die wegweisende FDA-Zulassung der ersten ex-vivo-CRISPR-Sichelzelltherapie im Jahr 2024 und wachsende Pipelines für seltene Krankheiten. Aldevron und Integrated DNA Technologies produzierten innerhalb von sechs Monaten das erste patientenspezifische mRNA-CRISPR-Medikament für eine Harnstoffzyklusstörung und demonstrierten damit die Machbarkeit der Behandlung von extrem seltenen Erkrankungen. Onkologieprogramme nutzen Neoantigen-Impfstoffe in Kombination mit Checkpoint-Inhibitoren, während Proteinersatzanwendungen bei Stoffwechselstörungen an Bedeutung gewinnen. Die Marktgröße für mRNA-Synthesedienstleistungen bei Gen-Editierungs-Nutzlasten wird bis 2030 voraussichtlich verdoppelt, da sich regulatorische Wege klären und Verabreichungschemien verbessern.
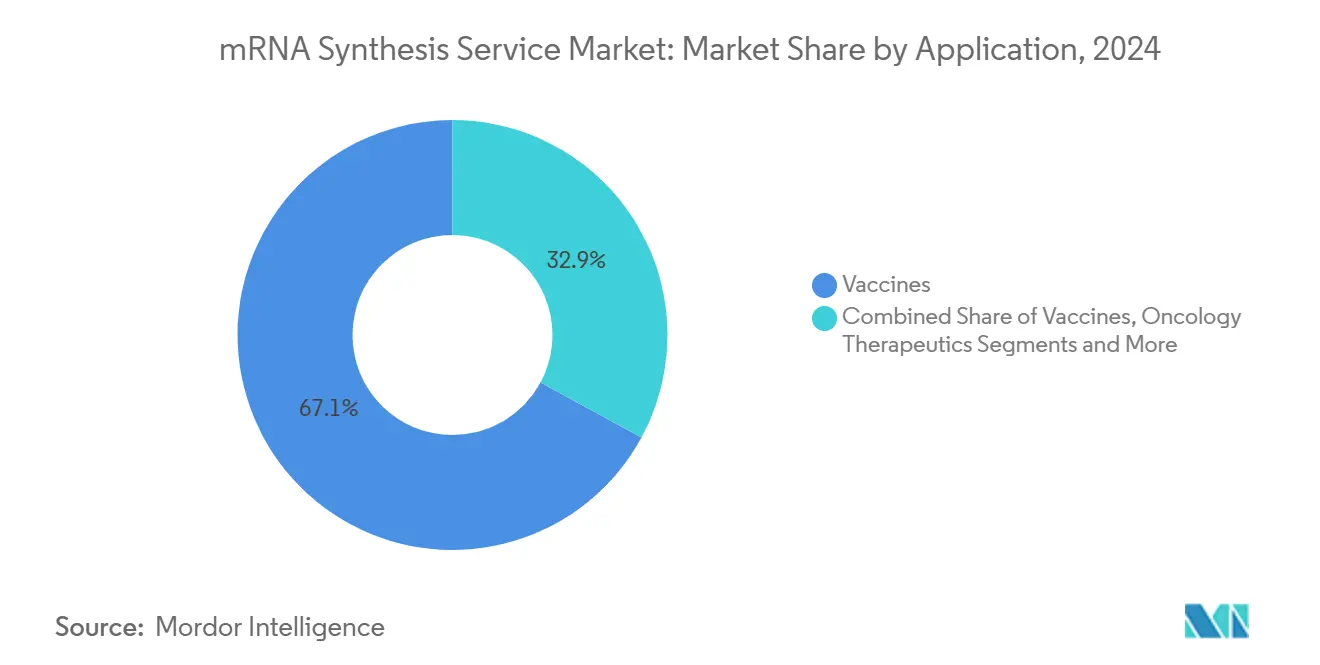
Notiz: Segmentanteile aller einzelnen Segmente sind nach dem Kauf des Berichts verfügbar
Nach Endnutzer: Biotechnologieunternehmen treiben die Innovationsbeschleunigung voran
Pharmaunternehmen hielten im Jahr 2024 41,7 % der Auslagerungsausgaben, hauptsächlich für Hochvolumen-Impfstoffe und Onkologieprojekte in der Spätphase. Biotechnologieunternehmen steigen jedoch mit einer CAGR von 7,3 % auf, angetrieben durch Risikokapital und schlüsselfertige CDMO-Angebote, die den Bedarf an eigenen Produktionsstätten überflüssig machen. Radar Therapeutics, Innovac Therapeutics und andere Start-ups nutzen meilensteinbasierte Verträge, um Liquidität zu schonen und gleichzeitig auf erstklassige Technologieplattformen zuzugreifen. Akademische Ausgründungen und staatliche Labore schaffen inkrementelle Nachfrage nach präklinischen Versorgungsgütern und unterstreichen die Demokratisierung der mRNA-Forschung und -Entwicklung.
Geografische Analyse
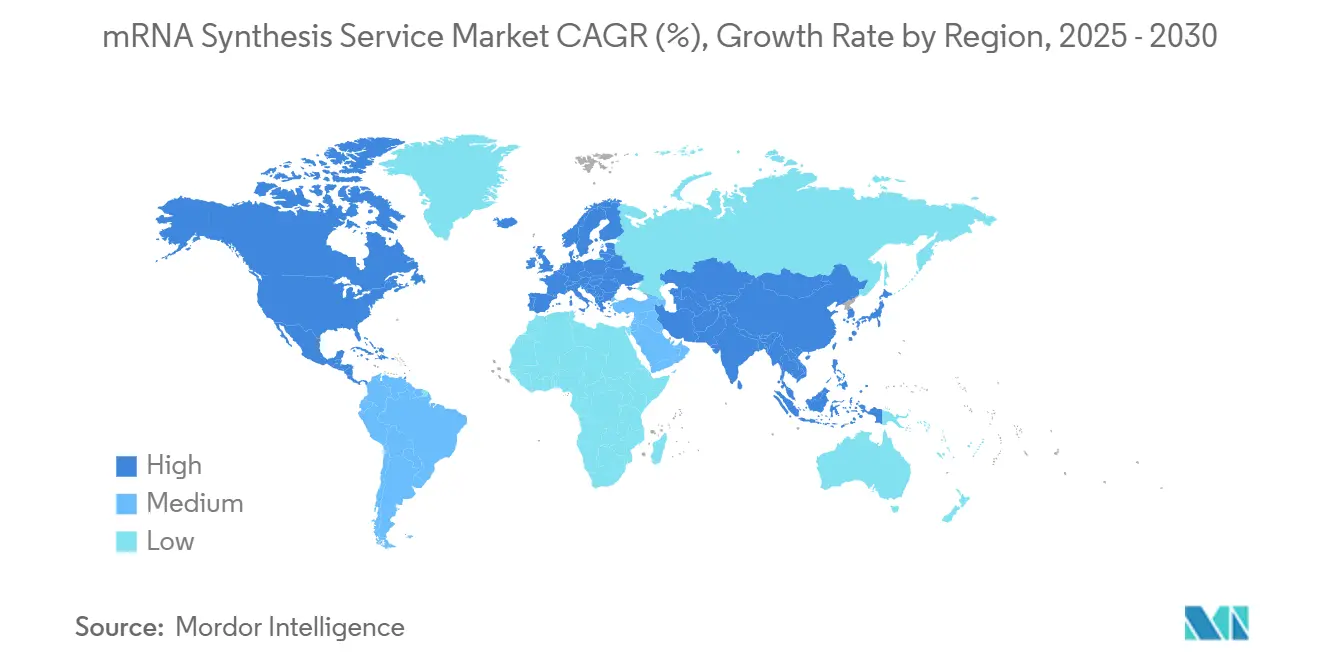
Nordamerika kontrollierte im Jahr 2024 42,4 % des Umsatzes, gestützt durch einen tiefen Talentpool, robusten Schutz des geistigen Eigentums und aggressive öffentlich-private Finanzierung. Drei Moderna-Werke, die 2025 in Betrieb gehen sollen – in Kanada, dem Vereinigten Königreich und Australien – werden jeweils bis zu 100 Millionen Dosen jährlich produzieren und so regionsübergreifende Lieferketten stärken, während kritische Schritte in den USA verbleiben. Die US-amerikanische Behörde für biomedizinische Forschung und Entwicklung (BARDA) vergibt weiterhin mehrjährige „Warm-Base”-Verträge, die Kapazitätsreserven für Bedarfsspitzen garantieren.
Europa profitiert von kohärenten regulatorischen Rahmenbedingungen und strategischen Herstellungszentren. Wackers Kompetenzzentrum in Deutschland im Wert von 102 Millionen USD fügt vier RNA-Linien hinzu, von denen die Hälfte für föderale Pandemievorräte reserviert ist. Das neue allgemeine Kapitel des Europäischen Arzneibuches zur mRNA-Qualität legt Referenzstandards fest, die die Chargenfreigabe in den Mitgliedstaaten vereinfachen.
Der Asien-Pazifik-Raum ist die am schnellsten wachsende Region mit einer CAGR von 6,4 %. Chinas WuXi Biologics und GenScript-Expansionen, Südkoreas Moderna-Partnerschaft und Singapurs Rolle als ASEAN-Hauptsitz von BioNTech verdeutlichen konzertierte staatliche Strategien. Aurora Biosynthetics in Australien zielt auf eine durchgängige GMP-Produktion vom Plasmid bis zur Abfüllung und Endbearbeitung ab und nutzt dabei 200 Millionen USD an staatlicher Förderung. Taiwan Bio-Manufacturing Corp strebt an, das Halbleiter-Foundry-Modell für die Biopharmazie zu replizieren, was langfristige regionale Ambitionen signalisiert.
Der Nahe Osten und Afrika nutzen modulare Systeme, um Infrastrukturlücken zu schließen. Der Einsatz von KeyPlants PODs durch HT-Bio in Saudi-Arabien markiert eine frühe Übernahme. Südamerika expandiert durch Technologietransfervereinbarungen in Brasilien und Argentinien und verbessert so die regionale Impfstoffautonomie.
Wettbewerbslandschaft
Der Markt für mRNA-Synthesedienstleistungen weist eine moderate Konzentration auf. Die fünf führenden Unternehmen – Lonza, TriLink BioTechnologies, Aldevron, Wacker Biotech und WuXi Biologics – halten zusammen rund 45–50 % des Umsatzes, was einem Marktkonzentrationsindex von 6 entspricht. Lonzas Vacaville-Transaktion im Wert von 1,2 Milliarden USD schafft Flexibilität für Säugetier- und mRNA-Produktion, während eine neue Divisionsstruktur mRNA mit Zell- und Genangeboten bündelt.
TriLinks nicht-exklusive CleanCap-Lizenzen erzeugen einen Netzwerkeffekt; über 250 IND-Einreichungen stützen sich auf die Technologie und festigen ihre Position als „Gatekeeper” für hochwertiges 5′-Capping. Aldevron erweitert die Plasmidkapazität und LNP-Dienste und sichert sich mehrjährige Lieferverträge für CRISPR-Anwendungen.
Wacker skaliert Schnellreaktionslinien mit EU-Pandemieaufträgen, die eine Mindestauslastung garantieren. Kleinere Spezialisten differenzieren sich durch KI-Plattformen, modulare Biofoundries oder regionale Ausrichtung.
Marktführer im Bereich mRNA-Synthesedienstleistungen
Thermo Fisher Scientific
Lonza
TriLink BioTechnologies
Danaher Corporation
Catalent Inc.
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- November 2024: Maravai LifeSciences übernahm das DNA- und RNA-Geschäft von Officinae Bio und stärkte damit seine KI-gestützten mRNA-Synthesefähigkeiten für die schnelle Prototypenentwicklung von mRNA-Kandidaten.
- November 2024: Maravai LifeSciences initiierte die mRNA-Synthese für eine Phase-II-klinische Studie eines Kunden in seiner GMP-Anlage Flanders 2 und stellte CleanScribe RNA-Polymerase vor, um die Qualität der mRNA-Synthese zu verbessern.
- Mai 2024: Aldevron kooperierte mit Acuitas Therapeutics und erweiterte die mRNA-Dienste um die Einkapselung in Lipid-Nanopartikel, um einen ganzheitlichen Ansatz von der Synthese bis zur Formulierung zu gewährleisten.
- April 2024: AmplifyBio und RNAV8 Bio schlossen eine Partnerschaft, die Sequenzdesign mit GMP-Synthese verbindet und umfassende mRNA-Dienste vom Design bis zur Produktion liefert.
Berichtsumfang des globalen Marktes für mRNA-Synthesedienstleistungen
| Individuelle mRNA-Synthese |
| GMP-konforme Herstellung |
| Rohstoff- und Enzymversorgung |
| Design- und Optimierungsdienstleistungen |
| Analytische Dienstleistungen und Qualitätskontrolle |
| Forschungsqualität (RUO) |
| Präklinische Qualität |
| Klinische GMP (Phase I–III) |
| Kommerzielle GMP |
| Standortgebundene modulare Produktion |
| Impfstoffe |
| Onkologietherapeutika |
| Seltene Krankheiten / Proteinersatz |
| Gen-Editierung / CRISPR |
| Sonstige Therapeutika |
| Biotechnologieunternehmen |
| Pharmaunternehmen |
| CDMOs und CROs |
| Sonstige |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Übriges Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Übriger Asien-Pazifik-Raum | |
| Naher Osten und Afrika | Golfkooperationsrat |
| Südafrika | |
| Übriger Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Übriges Südamerika |
| Nach Dienstleistungsart | Individuelle mRNA-Synthese | |
| GMP-konforme Herstellung | ||
| Rohstoff- und Enzymversorgung | ||
| Design- und Optimierungsdienstleistungen | ||
| Analytische Dienstleistungen und Qualitätskontrolle | ||
| Nach Maßstab | Forschungsqualität (RUO) | |
| Präklinische Qualität | ||
| Klinische GMP (Phase I–III) | ||
| Kommerzielle GMP | ||
| Standortgebundene modulare Produktion | ||
| Nach Anwendung | Impfstoffe | |
| Onkologietherapeutika | ||
| Seltene Krankheiten / Proteinersatz | ||
| Gen-Editierung / CRISPR | ||
| Sonstige Therapeutika | ||
| Nach Endnutzer | Biotechnologieunternehmen | |
| Pharmaunternehmen | ||
| CDMOs und CROs | ||
| Sonstige | ||
| Nach Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Übriges Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Australien | ||
| Übriger Asien-Pazifik-Raum | ||
| Naher Osten und Afrika | Golfkooperationsrat | |
| Südafrika | ||
| Übriger Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Übriges Südamerika | ||
Im Bericht beantwortete Schlüsselfragen
Wie groß ist der Markt für mRNA-Synthesedienstleistungen im Jahr 2025?
Der Markt hatte im Jahr 2025 einen Wert von 6,80 Milliarden USD und wird bis 2030 voraussichtlich 9,41 Milliarden USD erreichen.
Welches Dienstleistungssegment wächst bei der mRNA-Auslagerung am schnellsten?
Die individuelle mRNA-Synthese wächst mit einer CAGR von 9,1 %, angetrieben durch personalisierte Medizin und KI-gestütztes Design.
Warum gewinnen modulare „Drucker”-Anlagen an Bedeutung?
Containerisierte GMP-Einheiten ermöglichen dezentrale Produktion, verkürzen Bauzeiten und erhöhen die Resilienz gegenüber Lieferunterbrechungen.
Welche Region verzeichnet das schnellste Wachstum?
Der Asien-Pazifik-Raum wächst mit einer CAGR von 6,4 % dank staatlicher Förderung und Kostenvorteilen.
Welche Technologie verbessert die mRNA-Ausbeuten am stärksten?
Hocheffiziente IVT in Kombination mit CleanCap-Capping treibt die Ausbeuten auf 14 g/L und steigert die Proteinexpression.
Wie konzentriert ist das Wettbewerbsfeld?
Die fünf führenden Unternehmen kontrollieren rund die Hälfte des Umsatzes, was auf eine moderate Konzentration hinweist.
Seite zuletzt aktualisiert am:



