Größe und Marktanteil des Healthcare & Medical Devices TIC-Markts
Analyse des Healthcare & Medical Devices TIC-Markts von Mordor Intelligence
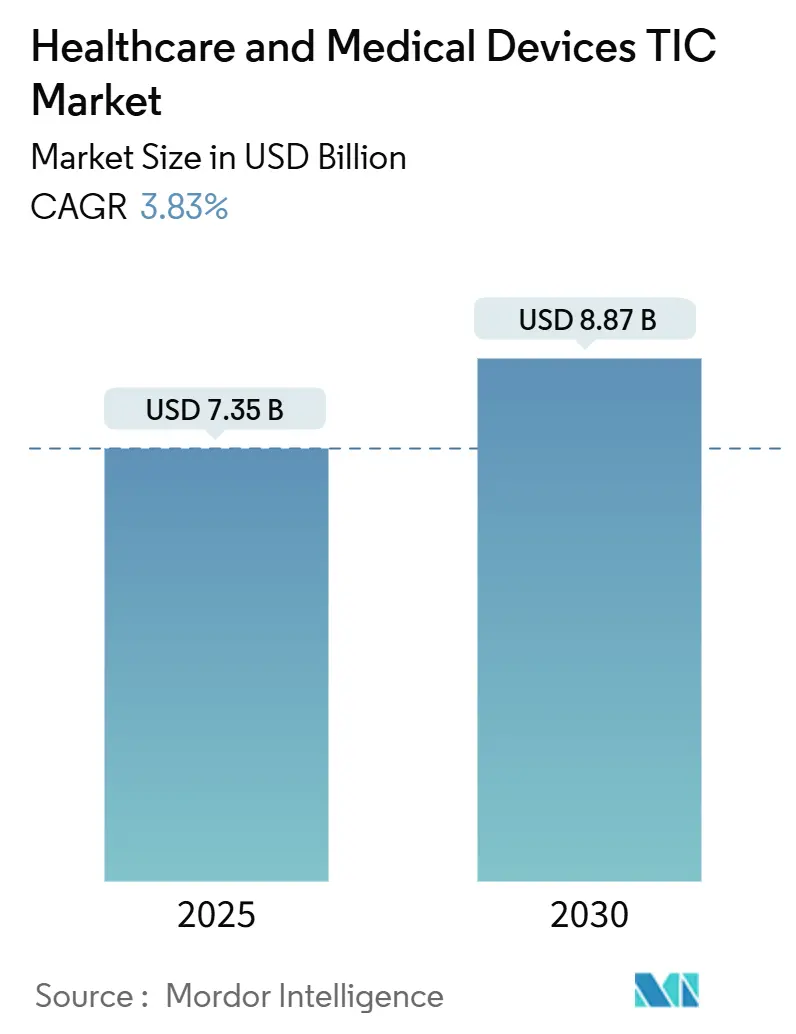
Der Markt für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte wird im Jahr 2025 auf 7,35 Milliarden USD geschätzt und soll bis 2030 einen Wert von 8,87 Milliarden USD erreichen, was einer CAGR von 3,83 % im Prognosezeitraum entspricht. Verbindliche globale Compliance-Rahmenwerke, zunehmende Gerätekomplexität und eine beschleunigte regulatorische Harmonisierung sichern eine stabile Nachfrage, auch wenn die Gesundheitsbudgets enger werden. Die Fertigungskonzentration im Asien-Pazifik-Raum und die rasche regulatorische Entwicklung stützen die regionale Dominanz, während durch Cybersicherheit ausgelöste Rückrufe und KI-gestützte Diagnostik den Validierungsumfang erweitern. Etablierte Anbieter von Prüfung, Inspektion und Zertifizierung nutzen multinationale Akkreditierungen und Laborautomatisierung, um ihre Preissetzungsmacht gegenüber fragmentierten regionalen Spezialisten zu behaupten. Erheblicher Fachkräftemangel, insbesondere bei biomedizinischen Auditoren, sowie steigende Kosten für Biokompatibilitätsmodelle dämpfen die Wachstumsaussichten, doch erhebliche Konsolidierungs- und Nischenspezialisierungsmöglichkeiten bleiben bestehen.
Wichtigste Erkenntnisse des Berichts
- Nach Serviceart führten Prüfdienstleistungen mit einem Marktanteil von 53,6 % im Markt für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte im Jahr 2024, während Zertifizierungsdienstleistungen bis 2030 mit einer CAGR von 4,2 % wachsen.
- Nach Beschaffungsart entfielen auf ausgelagerte Modelle 69,3 % der Marktgröße für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte im Jahr 2024, und sie sollen zwischen 2025 und 2030 mit einer CAGR von 3,9 % wachsen.
- Nach Geografie erzielte der Asien-Pazifik-Raum im Jahr 2024 einen Umsatzanteil von 44,7 % im Markt für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte; für die Region wird bis 2030 die höchste CAGR von 4,5 % prognostiziert.
Globale Trends und Erkenntnisse im Healthcare & Medical Devices TIC-Markt
Analyse der Treiberwirkung
| Treiber | (~) % Auswirkung auf die CAGR-Prognose | Geografische Relevanz | Zeithorizont der Auswirkung |
|---|---|---|---|
| Zunahme der Gerätekomplexität und Miniaturisierung | +0.8% | Global, mit Schwerpunkt in Nordamerika und Asien-Pazifik | Mittelfristig (2–4 Jahre) |
| Ausweitung der globalen regulatorischen Harmonisierung (MDSAP, IVDR) | +0.7% | Global, angeführt von Nordamerika, der EU und dem Asien-Pazifik-Raum | Langfristig (≥ 4 Jahre) |
| Wachstum der Heimgesundheits- und tragbaren Diagnostik | +0.6% | Nordamerika und die EU sind primär, Asien-Pazifik ist aufstrebend | Kurzfristig (≤ 2 Jahre) |
| Zunehmende Rückrufe treiben präventive Prüfausgaben | +0.5% | Global, mit der höchsten Auswirkung in Nordamerika | Mittelfristig (2–4 Jahre) |
| KI-gestützte schnelle Prüfprotokolle | +0.4% | Nordamerika und die EU sind frühe Anwender, Asien-Pazifik folgt. | Langfristig (≥ 4 Jahre) |
| Nachfrage nach Prüfung im Rahmen der Kreislaufwirtschaft und Aufarbeitung | +0.3% | EU führend, Nordamerika selektive Übernahme | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Zunahme der Gerätekomplexität und Miniaturisierung
Tragbare Geräte kombinieren heute Sensorik, Konnektivität und KI-Engines, die eine gleichzeitige Bewertung von Sensorgenauigkeit, Elektromagnetik, Softwarezuverlässigkeit und Hautsicherheit unter verschiedenen realen Bedingungen erfordern. Moderne Validierungszyklen müssen zudem das kontinuierliche Algorithmenlernen verifizieren, was Hersteller dazu veranlasst, wiederkehrende Prüfpartnerschaften anstelle von episodischen Projekten einzugehen.[1]FDA, „FDA gibt erstes KI-gestütztes Medizinprodukt für den Heimgebrauch bei Schlafapnoe-Tests frei”, FDA.GOV Talentintensive Protokolle erhöhen die Projektkosten, sichern jedoch vorhersehbare Einnahmen für Anbieter von Prüfung, Inspektion und Zertifizierung, die multidisziplinäre Teams und fortschrittliche Simulationswerkzeuge vorhalten.
Ausweitung der globalen regulatorischen Harmonisierung (MDSAP, IVDR)
Das MDSAP-Rahmenwerk ermöglicht es, mit einem einzigen Audit fünf Regulierungsbehörden zu erfüllen, was die Compliance-Ausgaben der Hersteller um etwa 30–40 % senkt, gleichzeitig aber die Nachfrage nach Prüfungs-, Inspektions- und Zertifizierungsunternehmen mit gleichzeitiger Anerkennung in den USA, Kanada, Australien, Japan und Brasilien erhöht.[2]Health Canada, „Medical Device Single Audit Program”, CANADA.CA Die IVDR-Einführung in Europa spiegelt diesen Trend wider, erweitert die Gerätekategorien, die strengen Leistungsprüfungen für die Diagnostik unterliegen, und konzentriert das Geschäft bei global akkreditierten Anbietern.
Wachstum der Heimgesundheits- und tragbaren Diagnostik
Die FDA hat im Jahr 2024 mehr als 50 digitale Gesundheitsgeräte für den Heimgebrauch zugelassen, darunter mit Smartphones verbundene Schlafapnoe- und Glukosemonitore, die Cybersicherheits-, Benutzerfreundlichkeits- und Robustheitsbewertungen in verschiedenen Umgebungen erfordern, die über klassische Labortests hinausgehen. Die Wirtschaftlichkeit der dezentralisierten Versorgung veranlasst Kostenträger, die Fernüberwachung zu erstatten, was die Einnahmen für Anbieter von Prüfung, Inspektion und Zertifizierung steigert, die über Heimsimulationslabore und IoT-Penetrationstestkompetenz verfügen.
Zunehmende Rückrufe treiben präventive Prüfausgaben
Ein Anstieg der Geräterückrufe um 400 % zwischen 2013 und 2018, der größtenteils auf Software- und Netzwerkschwachstellen zurückzuführen ist, veranlasste Hersteller, ihre Prüfbudgets auf 15–25 % der Entwicklungsausgaben zu erhöhen, gegenüber historisch 8–12 %. Präventive Validierung kompensiert nun Rückrufkosten von durchschnittlich 10–50 Millionen USD und sichert robustere Frühphasenengagements für Spezialisten im Bereich Prüfung, Inspektion und Zertifizierung.
Analyse der Hemmnisse
| Hemmnis | (~) % Auswirkung auf die CAGR-Prognose | Geografische Relevanz | Zeithorizont der Auswirkung |
|---|---|---|---|
| Mangel an qualifizierten biomedizinischen Auditoren im Bereich Prüfung, Inspektion und Zertifizierung | -0.4% | Global, am stärksten in Nordamerika und der EU | Kurzfristig (≤ 2 Jahre) |
| Rückgang der Risikokapitalfinanzierung für Medizintechnik-Start-ups | -0.3% | Global, mit der höchsten Auswirkung in Nordamerika | Mittelfristig (2–4 Jahre) |
| Cyberrisiken für die Datenintegrität bei vernetzten Geräten | -0.2% | Global, konzentriert in digital fortgeschrittenen Märkten | Langfristig (≥ 4 Jahre) |
| Steigende Kosten für Biokompatibilitäts-Tiermodelle | -0.2% | Global, mit der EU als Vorreiter bei Alternativen | Mittelfristig (2–4 Jahre) |
| Quelle: Mordor Intelligence | |||
Mangel an qualifizierten biomedizinischen Auditoren im Bereich Prüfung, Inspektion und Zertifizierung
Die Rekrutierung spezialisierter Auditoren erfordert 5–7 Jahre interdisziplinäre Ausbildung; Pensionierungen übersteigen den Nachwuchs im Verhältnis von etwa zwei zu eins, was zu einer Personallücke von 25–30 % führt und eine jährliche Lohninflation von 15–20 % antreibt.[3]Bureau of Labor Statistics, „Medizinische Wissenschaftler”, BLS.GOV Anbieter automatisieren die Datenerfassung und Fernbewertungen, um Engpässe zu mindern, können jedoch kurzfristige Kapazitätserweiterungen noch nicht vollständig nutzen.
Rückgang der Risikokapitalfinanzierung für Medizintechnik-Start-ups
Die globalen Medizintechnikinvestitionen sanken im Jahr 2024 auf 19,1 Milliarden USD, gegenüber einem Höchststand von 22,1 Milliarden USD im Jahr 2021, was frühe Gerätepipelines reduziert und Prüfungs-, Inspektions- und Zertifizierungsverträge auf spätere Meilensteine verschiebt. Kapitalknappen Start-ups komprimieren nun den Validierungsumfang, was den Umsatzzeitpunkt für Anbieter von Prüfung, Inspektion und Zertifizierung verändert.
Segmentanalyse
Nach Serviceart: Prüfdienstleistungen behalten die Führung, während Zertifizierungen an Fahrt gewinnen
Prüfdienstleistungen erzielten im Jahr 2024 mit 53,6 % den größten Anteil am Markt für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte, angetrieben durch ISO-10993-Materialbewertungen und obligatorische elektromagnetische Verträglichkeitsprüfungen. Die Breite des Segments umfasst Biokompatibilität, elektrische Sicherheit und Cybersicherheitsprotokolle, die jeweils mit der Gerätekonnektivität und der KI-Einführung skalieren. Obwohl das Wachstum nachlässt, da einige Prüfungen unter harmonisierten Rahmenwerken konsolidiert werden, stützt die steigende Designkomplexität das Volumen und die Margenstabilität.
Zertifizierungsdienstleistungen, die zwar einen kleineren Anteil an der Marktgröße für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte ausmachen, verzeichneten die höchste CAGR von 4,2 %. Hersteller investieren zunehmend in Einzelquellen-Zertifizierungen, die MDSAP und IVDR gleichzeitig erfüllen, und tauschen Vorabgebühren gegen schnellere globale Markteinführungen. Inspektionsdienstleistungen, die etwa ein Viertel des Umsatzes ausmachen, profitieren von Transparenzmandaten in der Lieferkette, wachsen jedoch langsamer, da Fernaudits an Bedeutung gewinnen.
Sekundäreffekte verstärken das Zusammenspiel der Segmente: Fortgeschrittene Zertifizierungen bündeln häufig vorausgesetzte Prüfungen, und erfolgreiche Audits speisen wiederkehrende Überwachungsinspektionen. Anbieter von Prüfung, Inspektion und Zertifizierung, die alle drei Angebote über Cloud-Plattformen integrieren, monetarisieren End-to-End-Compliance-Lebenszyklen und ziehen sowohl multinationale Konzerne als auch ressourcenschwache Innovatoren an.
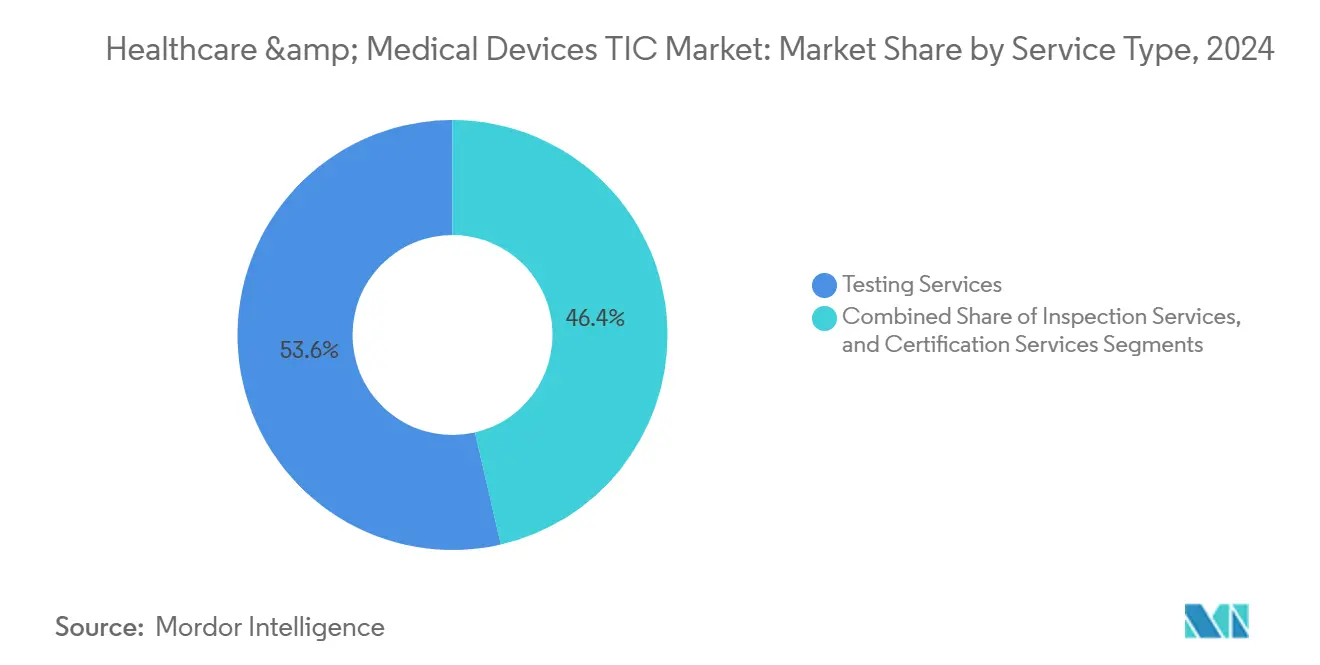
Notiz: Segmentanteile aller einzelnen Segmente sind nach dem Kauf des Berichts verfügbar
Nach Beschaffungsart: Auslagerung übertrifft weiterhin interne Modelle
Die Auslagerung dominierte im Jahr 2024 mit 69,3 % des Marktanteils für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte und verzeichnet bis 2030 eine CAGR von 3,9 %. Steigende Kapitalaufwendungen für spezialisierte Kammern, Reinräume und Cybersicherheitslabore – oft 10–50 Millionen USD pro Einrichtung – machen externe Partnerschaften für Start-ups und sogar große Erstausrüster wirtschaftlich, die Kapazitätsspitzen abdecken müssen.
Interne Kapazitäten sind zwar strategisch für Kernproduktlinien, stehen jedoch vor Talentengpässen und rascher Veralterung, da sich Standards weiterentwickeln. Einige multinationale Konzerne betreiben nun hybride Modelle, bei denen kritische Software- oder proprietäre Materialprüfungen intern verbleiben, während Drittlabore die drahtlose Koexistenz, KI-Verzerrungen und internationale Nischenzertifizierungen übernehmen. Diese Dynamik ermutigt Anbieter von Prüfung, Inspektion und Zertifizierung, sich in der Nähe großer Fertigungscluster anzusiedeln und gemeinsame Infrastruktur sowie Echtzeit-Datenportale anzubieten, die sich in die Designzyklen der Erstausrüster einfügen.
Geografische Analyse
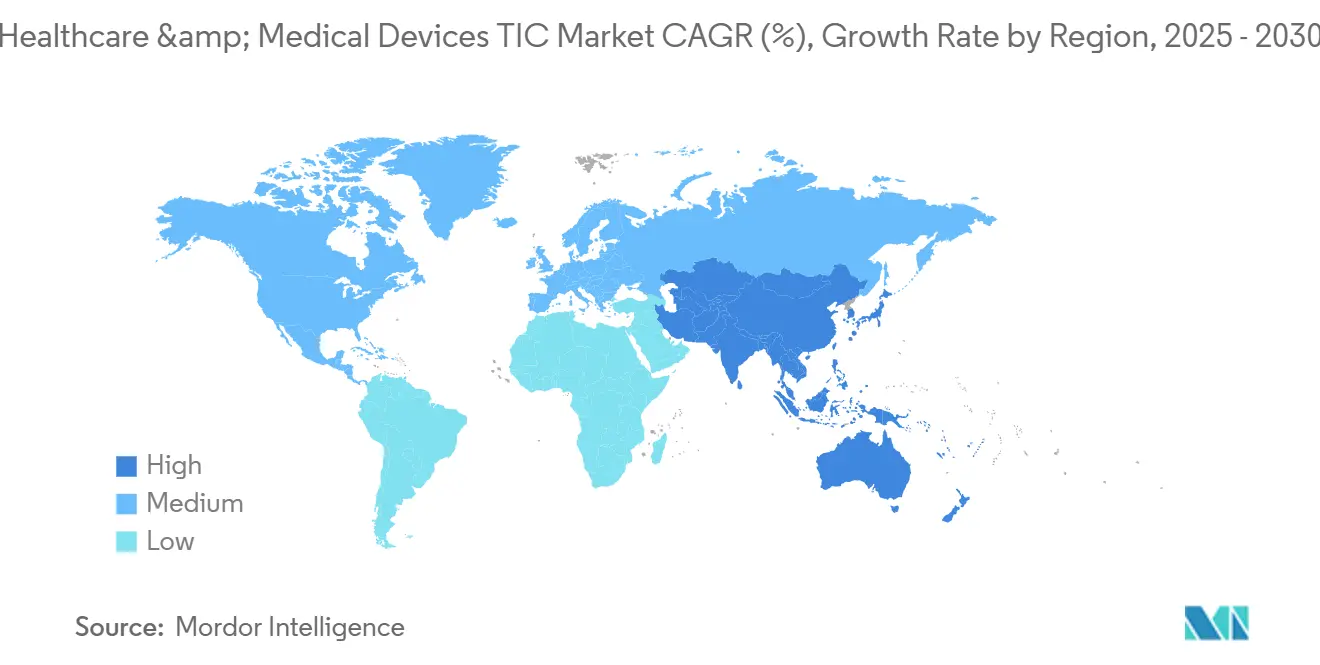
Der Asien-Pazifik-Raum erzielte im Jahr 2024 einen Anteil von 44,7 % am globalen Umsatz und soll bis 2030 eine CAGR von 4,5 % verzeichnen, was die Region zum Wachstumsmotor des Markts für Prüfung, Inspektion und Zertifizierung von Medizinprodukten macht. Die Reformen der Nationalen Medizinprodukteadministration (NMPA) Chinas synchronisieren die inländischen Vorschriften mit ISO- und IEC-Standards und schreiben gleichzeitig lokale Prüfberichte vor, was die Nachfrage nach international akkreditierten Laboren festigt.[4]Nationale Medizinprodukteadministration, „Regulatorische Aktualisierungen”, NMPA.GOV.CN Japan und Südkorea ergänzen dies durch hochwertige Cybersicherheits- und KI-Validierungsanforderungen, während Südostasien unter der ASEAN-Harmonisierung für kosteneffiziente Routineanalysen an Bedeutung gewinnt.
Nordamerika hielt im Jahr 2024 einen Marktanteil von 28 % und soll moderat mit einer CAGR von 3,2 % wachsen. Die Vereinigten Staaten führen mit hochmargigen Projekten bei der Risikobewertung vernetzter Geräte, da die FDA die Offenlegung von Software-Stücklisten prüft. Kanadas MDSAP-Beteiligung stützt grenzüberschreitende Audit-Synergien, während Mexikos kostengünstigere Labore Standardprüfsegmente für regionale Lieferketten anziehen.
Europa entfiel im Jahr 2024 auf 22 % des Umsatzes, da die MDR und IVDR bisherige Selbstzertifizierungen in formelle Prüfungs-, Inspektions- und Zertifizierungsengagements umwandelten. Deutschland und das Vereinigte Königreich dominieren das Volumen, wobei doppelte EU-UK-Zertifizierungen nach dem Brexit inkrementelle Chancen eröffnen. Kreislaufwirtschaftsvorschriften katalysieren Nischen für Aufarbeitungs- und Lebenszyklustests, und die DSGVO treibt eine verstärkte Prüfung der Patientendatenintegrität voran.
Wettbewerbslandschaft
Die globale Führungsposition bleibt verteilt, was die Branche für Prüfung, Inspektion und Zertifizierung von Medizinprodukten in ein moderat konzentriertes Segment einordnet. SGS, Intertek, TÜV SÜD und Bureau Veritas nutzen mehr als 1.000 behördliche Anerkennungen und umfangreiche Labornetzwerke, um sich gegenüber regionalen Spezialisten zu differenzieren. Die jüngste SGS-Shanghai-Zulassung ohne FDA-Formular-483-Beobachtungen veranschaulicht die Akkreditierungstiefe, die Preisaufschläge rechtfertigt.
Die digitale Transformation bildet die Grundlage für Wettbewerbsvorteile. Die FlexLab-X-Automatisierung von Siemens Healthineers und die Robotiklösungen von Merck verdeutlichen den Schwenk hin zu KI-getriebenem Durchsatz, der den Auditormangel mindert und die Datenqualität erhöht. Cybersicherheit, Algorithmus-Bias-Audits und die Validierung aufgearbeiteter Geräte stellen lukrative Nischen dar, in denen kleinere Spezialisten schnell skalieren oder zu Übernahmezielen werden können, wie der Kauf des Lebensmitteltestgeschäfts von Bureau Veritas durch Mérieux NutriSciences für 405 Millionen USD zur Verdoppelung der Präsenz im Asien-Pazifik-Raum zeigt.
Die Fusionen- und Übernahmedynamik dürfte anhalten, gestützt durch das Interesse von Private-Equity-Gesellschaften und synergetische branchenübergreifende Transaktionen, die Umwelt-, Pharma- und Medizintechnikportfolios für den Endnutzerkomfort bündeln. Die Preisgestaltung bleibt stabil angesichts der Akkreditierungsknappheit und hoher Wechselkosten, doch Lohninflation und Investitionen in regulatorische Technologien komprimieren die Margen für Unternehmen ohne Skalierung oder Automatisierungsfahrpläne.
Branchenführer im Healthcare & Medical Devices TIC-Bereich
SGS SA
Bureau Veritas SA
Intertek Group plc
TÜV SÜD AG
TÜV Rheinland AG
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- März 2025: Merck führte Laborautomatisierungs- und Robotiklösungen für die pharmazeutische Qualitätskontrolle ein und kooperierte mit Ingenieurbüros zur Lieferung integrierter mikrobiologischer Prüfsysteme.
- Februar 2025: GN Store Nord meldete F&E-Ausgaben von 1,9 Milliarden DKK und betonte zentralisierte Qualitäts- und Produktsicherheitsrahmen für KI-gestützte Hörgeräte (0,29 Milliarden USD).
- Januar 2025: Eurofins Scientific erwarb SF Analytical Laboratories und erweiterte damit seine Reichweite im US-amerikanischen Umwelt- und Lebensmitteltestbereich.
- Oktober 2024: Mérieux NutriSciences vereinbarte die Übernahme der Lebensmitteltestsparte von Bureau Veritas für 360 Millionen EUR (405 Millionen USD).
Umfang des globalen Healthcare & Medical Devices TIC-Marktberichts
| Prüfdienstleistungen |
| Inspektionsdienstleistungen |
| Zertifizierungsdienstleistungen |
| Intern |
| Ausgelagert |
| Nordamerika | Vereinigte Staaten | |
| Kanada | ||
| Mexiko | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Übriges Südamerika | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Russland | ||
| Übriges Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Südostasien | ||
| Übriger Asien-Pazifik-Raum | ||
| Naher Osten und Afrika | Naher Osten | Saudi-Arabien |
| Vereinigte Arabische Emirate | ||
| Türkei | ||
| Übriger Naher Osten | ||
| Afrika | Südafrika | |
| Nigeria | ||
| Übriges Afrika | ||
| Nach Serviceart | Prüfdienstleistungen | ||
| Inspektionsdienstleistungen | |||
| Zertifizierungsdienstleistungen | |||
| Nach Beschaffungsart | Intern | ||
| Ausgelagert | |||
| Nach Geografie | Nordamerika | Vereinigte Staaten | |
| Kanada | |||
| Mexiko | |||
| Südamerika | Brasilien | ||
| Argentinien | |||
| Übriges Südamerika | |||
| Europa | Deutschland | ||
| Vereinigtes Königreich | |||
| Frankreich | |||
| Italien | |||
| Spanien | |||
| Russland | |||
| Übriges Europa | |||
| Asien-Pazifik | China | ||
| Japan | |||
| Indien | |||
| Südkorea | |||
| Südostasien | |||
| Übriger Asien-Pazifik-Raum | |||
| Naher Osten und Afrika | Naher Osten | Saudi-Arabien | |
| Vereinigte Arabische Emirate | |||
| Türkei | |||
| Übriger Naher Osten | |||
| Afrika | Südafrika | ||
| Nigeria | |||
| Übriges Afrika | |||
Im Bericht beantwortete Schlüsselfragen
Wie groß ist der globale Markt für Prüfung, Inspektion und Zertifizierung im Bereich Gesundheitswesen und Medizinprodukte heute?
Der Markt beläuft sich im Jahr 2025 auf 7,35 Milliarden USD und soll bis 2030 einen Wert von 8,87 Milliarden USD erreichen.
Welche Region trägt am meisten zum Umsatz bei Compliance-Dienstleistungen für Medizinprodukte bei?
Der Asien-Pazifik-Raum führt mit 44,7 % des globalen Umsatzes, angetrieben durch Fertigungskapazitäten und regulatorische Reife.
Warum wachsen Zertifizierungsdienstleistungen schneller als Prüfdienstleistungen?
Harmonisierte Rahmenwerke wie MDSAP und IVDR ermöglichen es, mit einem einzigen Zertifikat mehrere Märkte zu erschließen, was die Drittanbieter-Zertifizierung wertvoller macht.
Was ist die größte Herausforderung, die das kurzfristige Kapazitätswachstum für Anbieter von Prüfung, Inspektion und Zertifizierung begrenzt?
Ein Mangel von 25–30 % an qualifizierten biomedizinischen Auditoren schränkt die Serviceerweiterung trotz steigender Nachfrage ein.
Wie verhält sich die Auslagerung im Vergleich zur internen Prüfung?
Die Auslagerung kontrolliert 69,3 % der Gesamtausgaben, da spezialisierte Labore die Kapitalaufwendungen reduzieren und multinationale Zulassungen beschleunigen.
Welche aufstrebenden Nischen bieten das größte Potenzial für Unternehmen im Bereich Prüfung, Inspektion und Zertifizierung?
Hochmargige Bereiche umfassen die Cybersicherheitsvalidierung für vernetzte Geräte, KI-Algorithmus-Bias-Audits und Prüfungen im Rahmen der Kreislaufwirtschaft und Aufarbeitung.
Seite zuletzt aktualisiert am:



