Tendencias del Mercado de Pruebas y certificación globales de dispositivos médicos Industria
Se espera que el segmento de servicios de pruebas experimente un rápido crecimiento durante el período de pronóstico
A nivel mundial, los dispositivos médicos están regulados por diversas autoridades regulatorias y cumplimientos. Esto se debe principalmente a que los usuarios finales de estos dispositivos esperan un rendimiento, eficacia y seguridad excepcionales de estos dispositivos médicos. Por lo tanto, es obligatorio que los fabricantes definan e implementen adecuadamente una estrategia de prueba de dispositivos médicos, lo que hace que el dispositivo sea efectivo y la producción sea más fácil debido a la confirmación de la calidad
En abril de 2020, debido a la pandemia de COVID-19, la Comisión Europea (CE) adoptó una propuesta para posponer la fecha de aplicación del Reglamento de Dispositivos Médicos (MDR) por un año porque la pandemia de COVID-19 aumentó la demanda de ciertos dispositivos médicos. que eran cruciales para evitar riesgos o dificultades de posible escasez de dichos dispositivos. Además, la pandemia de COVID-19 ha retrasado los ensayos clínicos y ha interrumpido los procesos de los dispositivos médicos
Algunos de los dispositivos médicos experimentaron un aumento repentino en la demanda durante la pandemia de COVID-19 de 2020. Por ejemplo, los ventiladores tuvieron una gran demanda para los pacientes de COVID-19, ya que son una herramienta importante en los hospitales que puede mantener con vida a los pacientes en condiciones críticas.. Por ejemplo, en marzo de 2020, Medtronic PLC anunció que había aumentado la producción en más de un 40 % hasta la fecha y estaba en camino de duplicar con creces su capacidad para fabricar y suministrar ventiladores en respuesta a las necesidades urgentes de los pacientes y los sistemas sanitarios en todo el mundo. mundo frente al COVID-19
En junio de 2020, Intertek Group PLC anunció la expansión de los servicios de equipos de protección personal para incluir pruebas de respiradores N95 según los requisitos establecidos por el Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH). Con esta expansión, la empresa también amplió sus soluciones y recursos para apoyar a los clientes y a la comunidad global durante la pandemia de COVID-19
Una estrategia eficaz de prueba de dispositivos médicos necesita varios conjuntos de requisitos de prueba. Los conjuntos de requisitos son necesarios para facilitar la implementación de las pruebas, ya que las pruebas se llevan a cabo continuamente en diferentes etapas del proceso de fabricación completo, desde la selección de componentes hasta el ensamblaje final de un dispositivo médico. Cada etapa tiene diferentes requisitos y diferentes parámetros a satisfacer. Por lo tanto, el aumento de los dispositivos médicos también puede aumentar estos servicios de prueba, lo que se espera que aumente el crecimiento general del mercado
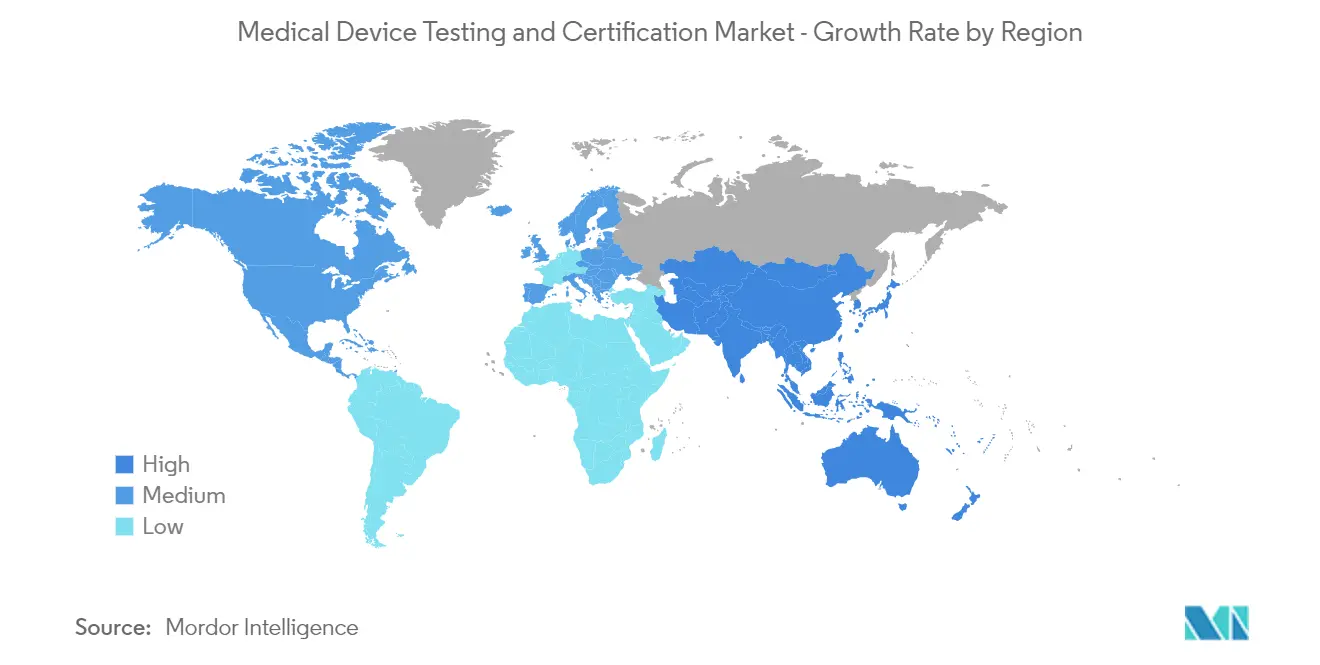
América del Norte domina el mercado y se espera que haga lo mismo durante el período de pronóstico
Algunos de los factores que impulsan el crecimiento del mercado en la región de América del Norte incluyen un mayor enfoque en la calidad de los dispositivos médicos y la presencia de una gran cantidad de empresas que prestan servicios en la industria de dispositivos médicos, junto con la presencia de atención médica bien desarrollada y la presencia de las principales empresas multinacionales de dispositivos médicos
Según un artículo de investigación de A. Chandimal Nicholas publicado en mayo de 2020, en Canadá, durante la pandemia de COVID-19 de 2020, el Ministro de Salud firmó la Orden provisional sobre la importación y venta de dispositivos médicos para su uso en relación con el COVID-19. , que permitió un acceso acelerado a los dispositivos médicos COVID-19 para uso de los proveedores de atención médica. Además, según Health Canada, la Orden Provisional ayudó a aprobar rápidamente la importación y venta de dispositivos médicos COVID-19
Además, durante la pandemia de COVID-19 de 2020, en los Estados Unidos, la Administración de Alimentos y Medicamentos (FDA) emitió Autorizaciones de uso de emergencia (EUA) para dispositivos médicos para diagnosticar COVID-19 y equipos de protección personal necesarios para proteger a los proveedores de atención médica que interactúan con los pacientes.
En Estados Unidos, los dispositivos médicos son gestionados por la Administración de Alimentos y Medicamentos (FDA) para garantizar la seguridad y eficacia de los dispositivos. El Centro de Dispositivos y Salud Radiológica (CDRH) es un segmento de la Administración de Alimentos y Medicamentos (FDA). Los dispositivos de Clase II requieren controles notables para 'etiquetado, orientación, seguimiento, planificación, estándares de desempeño y observación posterior a la comercialización', y la mayoría requiere notificación previa a la comercialización 510(k) para evaluar la equivalencia sustancial con un dispositivo comercializado legalmente
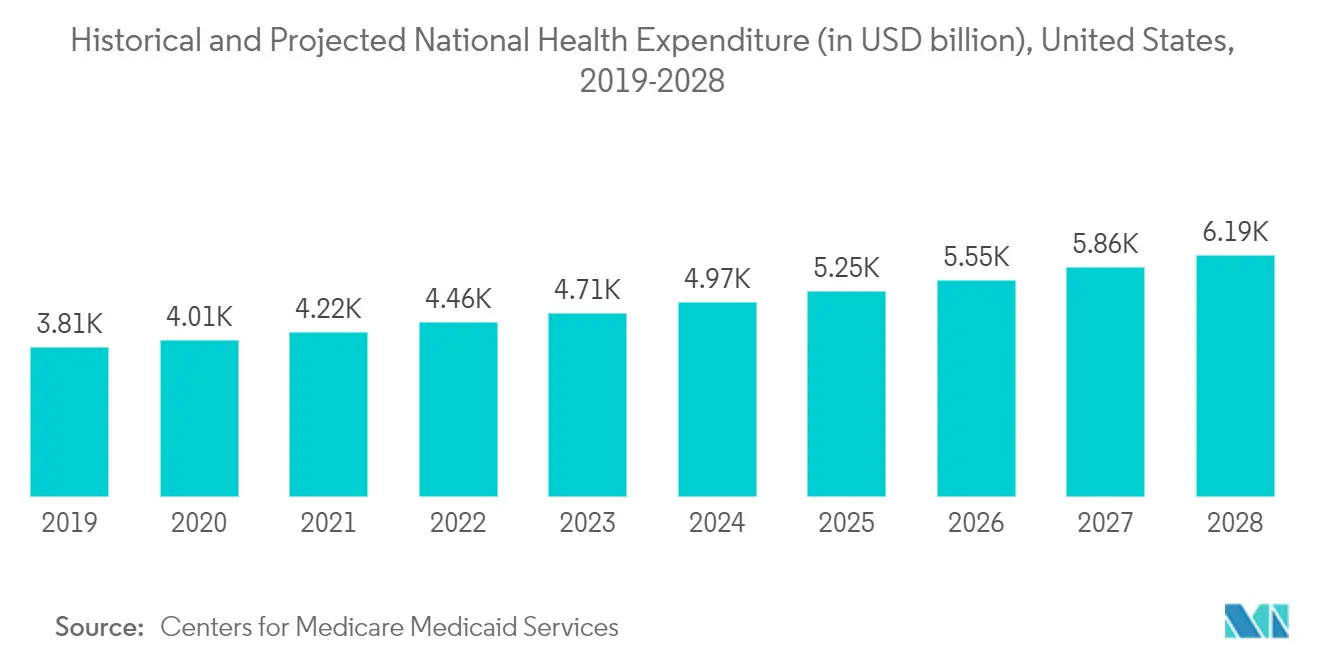
Según el Centro de Servicios de Medicare y Medicaid, el gasto sanitario de Estados Unidos creció un 4,6% en 2018, alcanzando los 3,6 billones de dólares o 11.172 dólares por persona. Como porcentaje del Producto Interno Bruto del país, el gasto en salud representó el 17,7%. Además, con la creciente aprobación de dispositivos médicos en la región, la creciente demanda de servicios de pruebas de dispositivos médicos puede impulsar el crecimiento del mercado. Por lo tanto, teniendo en cuenta los factores mencionados anteriormente, se espera que impulse el crecimiento del mercado en la región de América del Norte durante el período previsto