Tendances du marché de Immunothérapie cellulaire mondiale Industrie
La thérapie par cellules T à base de récepteurs d'antigènes chimériques (CAR) devrait connaître une croissance significative au cours de la période de prévision
La thérapie par cellules T du récepteur dantigène chimérique (CAR) constitue une avancée significative dans le traitement du cancer. Dans cette thérapie, les cellules T du patient sont génétiquement modifiées pour exprimer un récepteur artificiel qui se lie à un antigène tumoral. La thérapie cellulaire CAR-T agit contre les antigènes cancéreux codés par CD19 pour traiter les cancers à cellules B. La prévalence croissante du cancer, les progrès technologiques dans le développement de thérapies anticancéreuses basées sur des cibles et ladoption croissante de thérapies cellulaires à des fins thérapeutiques sont les principaux facteurs déterminants du segment de la thérapie par cellules T du récepteur dantigène chimérique (CAR)
Par exemple, selon une mise à jour 2022 de lAmerican Cancer Society, environ 10 470 enfants (âgés de 0 à 14 ans) et 5 480 adolescents (âgés de 15 à 19 ans) étaient susceptibles de recevoir un diagnostic de cancer aux États-Unis en 2022
Les progrès en matière de thérapie, dapprobations, de lancements, de partenariats et dacquisitions par les principaux acteurs du marché sont également susceptibles de stimuler la croissance du segment. Par exemple, en mai 2022, la Commission européenne (CE) a approuvé la thérapie CAR-T de Janssen, Carvykti, pour les adultes atteints de myélome multiple lourdement prétraité, en rechute et réfractaire, marquant la première approbation du traitement en dehors des États-Unis. De plus, en mars 2021, la FDA a approuvé Abecma (idecabtagene vicleucel), la première thérapie génique cellulaire destinée à traiter les patients adultes atteints de myélome multiple qui n'ont pas répondu à au moins quatre cycles de thérapie antérieurs. Il sagit dune thérapie par cellules T du récepteur dantigène chimérique (CAR) génétiquement modifiée dirigée par lantigène de maturation des cellules B (BCMA)
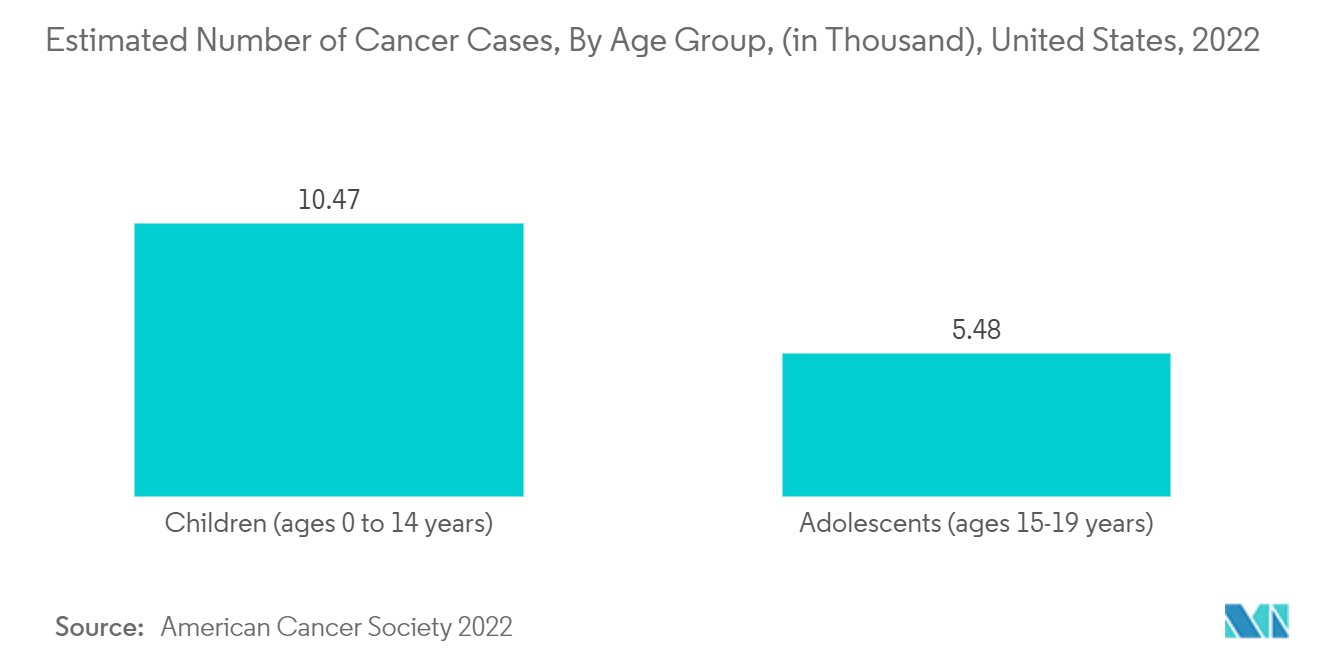
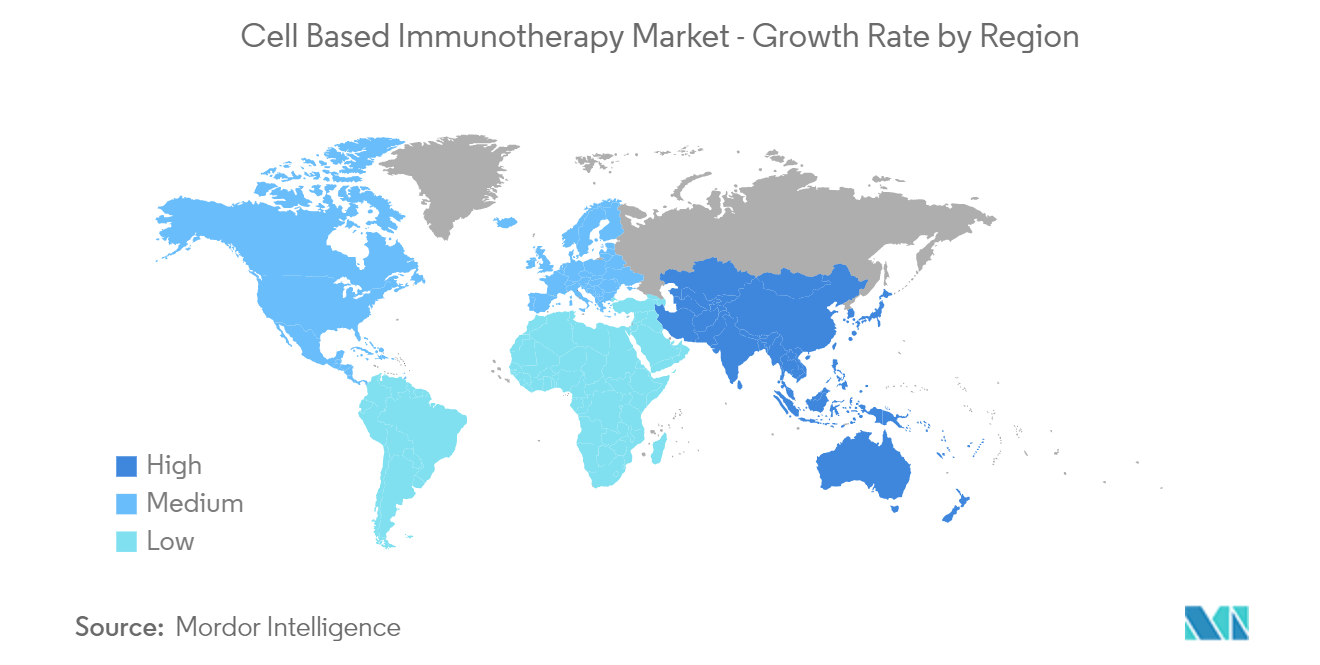
LAmérique du Nord devrait connaître une croissance du marché de limmunothérapie cellulaire au cours de la période de prévision
LAmérique du Nord devrait détenir une part de marché importante sur le marché mondial de limmunothérapie cellulaire en raison de la prévalence croissante du cancer, de la sensibilisation croissante aux thérapies cellulaires, de la forte présence des acteurs de lindustrie et de lamélioration des infrastructures de soins de santé dans cette région. Par exemple, selon une mise à jour 2022 de l'American Cancer Society, aux États-Unis, 290 560 nouveaux cas de cancer du sein, 89 010 cas de lymphome, 62 210 cas de cancer du pancréas, 106 180 cas de cancer du côlon et 44 850 cas de cancer du rectum étaient attendus. être diagnostiqué en 2022
En outre, la recherche en cours sur le traitement du cancer, les progrès technologiques, les approbations de produits, les lancements, les partenariats et les acquisitions par les principaux acteurs du marché alimentent également dans une large mesure la croissance de lensemble du marché régional. Par exemple, en mai 2022, la Food and Drug Administration (FDA) des États-Unis a élargi son approbation pour une thérapie cellulaire personnalisée développée au Abramson Cancer Center de l'Université de Pennsylvanie, cette fois pour le traitement des adultes atteints d'un lymphome folliculaire (FL) en rechute ou réfractaire. après deux lignes ou plus de thérapie systémique. L'approbation accélérée a été accordée à Novartis pour la thérapie par cellules T du récepteur d'antigène chimérique (CAR) Kymriah (tisagenlecleucel), ce qui en fait la troisième indication pour la thérapie cellulaire personnalisée contre le cancer. Il sagit de la seule thérapie cellulaire CAR-T approuvée pour les patients adultes et pédiatriques